Αζιριδίνη

| Αζιριδίνη | |
|---|---|
 | |
 | |
| Γενικά | |
| Όνομα IUPAC | Αζιριδίνη |
| Άλλες ονομασίες | Επαζαιθάνιο Αιθυλενιμίνη Αζακυκλοπροπάνιο |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C2H5N |
| Μοριακή μάζα | 43,07 amu |
| Σύντομος συντακτικός τύπος | |
| Αριθμός CAS | 151-56-4 |
| SMILES | N1CC1 |
| InChI | InChI=1/C2H5N/c1-2-3-1/h3H,1-2H2 |
| Αριθμός EINECS | 205-793-9 |
| ChemSpider ID | 8682 |
| Δομή | |
| Διπολική ροπή | 1,9 D[1] |
| Μήκος δεσμού | C-C: 148 pm C-N: 147 pm C-H: 109 pm N-H: 108 pm |
| Γωνία δεσμού | CCN, CNC, NCC: 60° CNH: 109,5° |
| Μοριακή γεωμετρία | τριγωνική ως προς C-C-N. |
| Ισομέρεια | |
| Ισομερή θέσης | 3 Αιθεναμίνη Αιθανιμίνη Ν-μεθυλομεθανιμίνη |
| Φυσικές ιδιότητες | |
| Σημείο τήξης | -77,9 °C |
| Σημείο βρασμού | 56 °C |
| Πυκνότητα | 832,1 kg/m3 (20 °C) |
| Διαλυτότητα στο νερό | Αναμείξιμο σε όλες τις αναλογίες |
| Χημικές ιδιότητες | |
| pKa | 7,9 |
| Σημείο αυτανάφλεξης | -11 °C |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
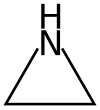
Γενικότερα, οι αζιριδίνες (αγγλικά aziridines) αποτελούν ομάδα οργανικών χημικών ενώσεων, που εμπεριέχουν μία (1) τουλάχιστον αζιριδινική ομάδα, η οποία αποτελείται από έναν τριμελή ετεροκυκλικό δακτύλιο, που περιέχει ένα (1) άτομο αζώτου και δύο (2) άτομα άνθρακα.[2][3] Αν περιέχουν μόνο μία αζιριδινική ομάδα, τότε έχουν γενικό τύπο C2R5Ν, όπου κάθε ένα από τα όχι απαραίτητα ίδια R, παριστάνουν άτομα υδρογόνου ή αλογόνου ή μονοσθενείς ανόργανες ή οργανικές ομάδες.[4] Ειδικότερα, όμως, η «μητρική» αζιριδίνη[5] (aziridine) ή αιθυλενιμίνη είναι η απλούστερη ετεροκυκλική αμίνη, με μοριακό τύπο C2H5N, αν και συνήθως παριστάνεται με το γραμμικό τύπο της, ![]() . Όπως φαίνεται σε αυτόν τον τύπο, δομικά αποτελείται από μια δευτεροταγή αμινομάδα (-NH-) και δυο (2) μεθυλενικές ομάδες (-CH2-).
. Όπως φαίνεται σε αυτόν τον τύπο, δομικά αποτελείται από μια δευτεροταγή αμινομάδα (-NH-) και δυο (2) μεθυλενικές ομάδες (-CH2-).
Ισομέρεια
[Επεξεργασία | επεξεργασία κώδικα]Με βάση το μοριακό τύπο της (C2H5N) έχει τα ακόλουθα τρία (3) ισομερή θέσης:
- Αιθεναμίνη με σύντομο συντακτικό τύπο: CH2=CHNH2.
- Αιθανιμίνη με σύντομο συντακτικό τύπο: CH3CH=NH.
- Ν-μεθυλομεθανιμίνη με σύντομο συντακτικό τύπο: CH2=NCH3.
Δομή
[Επεξεργασία | επεξεργασία κώδικα]Οι δεσμικές γωνίες στην αζιριδίνη είναι ακριβώς 60°, όπως συμβαίνει επίσης με το κυκλοπροπάνιο και το οξιράνιο, σημαντικά μικρότερη από την κανονική δεσμική γωνία των 109,5° των αλκανίων. Το μοντέλο «δεσμών μπανάνα» είναι μια από τις εξηγήσεις που δίνονται για τη δεσμολογία τέτοιων ενώσεων. Η αζιριδίνη είναι λιγότερο βασική σε σύγκριση με τις άκυκλες αλειφατικές αμίνες, καθώς το συζηγές οξύ της έχει pKa = 7,9. Αυτή (η μικρότερη βασικότητα) εξηγείται από τον ενισχυμένο χαρακτήρα που έχει το μονήρες ζεύγος ηλεκτρονίων του αζώτου της. Επίσης η ύπαρξη παραμόρφωσης δεσμικής γωνίας αυξάνει το «εμπόδιο» για την αναστροφή του αζώτου. Αυτό το αυξημένο εμπόδιο επιτρέπει (σε κάποια παράγωγά της) την απομόνωση ξεχωριστών αναστροφομερών, με παραδείγματα τα cis- και trans αναστροφομερών για την 2-μεθυλο-Ν-χλωραζιριδίνη.
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Υπάρχουν αρκετές μέθοδοι παραγωγής των αζιριδινών. Η διεργασία παραγωγής αζιριδίνης ονομάζεται «αζιριδίνωση».[6]
Με κυκλοποίηση 2-αλαμινών ή 2-αμινολών
[Επεξεργασία | επεξεργασία κώδικα]Σύμφωνα με αυτές τις μεθόδους, ένα άτομο υδρογόνου μιας αμινομάδας αποσπάται από ένα διπλανό άτομο αλογόνου με ενδομοριακή πυρηνόφιλη απόσπαση, δημιουργώντας μια αζιριδίνη. Οι 2-αμινόλες μπορούν επίσης να δώσουν παρόμοια αντίδραση, αλλά θα πρέπει πρώτα η υδροξυλομάδα να μετατραπεί μια καλή αποχωρούσα ομάδα. Αυτό συμβαίνει (συνήθως) με χρήση πυκνού θειικού οξέος (H2SO4), το οποίο λειτουργεί συγχρόνως ως οξύ και ως αφυδατικό μέσο, παράγοντας ενδιάμεσα 2-αμινοσουλφονικό οξύ, που τελικά υφίσταται απόσπαση της θειικής ομάδας (SO4) από (συνήθως) με υδροξείδιο του νατρίου (Na2SO4). Η κυκλοποίηση με 2-αμινόλη ονομάζεται σύνθεση Γουένκερ (Wenker synthesis, που ανακαλύφθηκε το 1935), ενώ η κυκλοποίηση με 2-αλαμίνη ονομάζεται μέθοδος αιθυλενιμίνης Γκάμπριελ (Gabriel ethylenimine method, που ανακαλύφθηκε το 1888).[7][8][9]:
Με προσθήκη νιτρενίου
[Επεξεργασία | επεξεργασία κώδικα]Η προσθήκη νιτρενίου (RN=C:) σε αλκένια είναι μια καλά θεμελιωμένη μέθοδος παραγωγής αζιριδινών. Η φωτόλυση ή θερμόλυση αζιδίων (όπως και του συζυγούς τους υδραζωτικού οξέος, HN3) είναι καλοί τρόποι παραγωγής νιτρενίων.
Για παράδειγμα, από υδραζωτικό οξύ με την επίδραση υπεριώδους ακτινοβολίας σε αιθένιο παράγεται αζιριδίνη:
Τα νιτρένια μπορούν επίσης να παραχθούν in situ από (διακετοξυϊωδο)βενζόλιο [Ph(IOAc)2] και σουλφοναμίδια (RSO2NR2) ή αιθοξυκαρβονυλονιτρένιο (EtCΟ2N=C:).
Με παρεμβολή μεθυλενίου στη μεθανιμίνη
[Επεξεργασία | επεξεργασία κώδικα]Με παρεμβολή μεθυλενίου [:CH2, που με τη σειρά του συνήθως παράγεται επίδραση μεθυλενοδιιωδιδίου (CH2I2) και ψευδαργύρου (Zn)] στη μεθανιμίνη (CH2=NH) παράγεται αζιριδίνη:
Από οξιράνιο
[Επεξεργασία | επεξεργασία κώδικα]1. Με επίδραση αζιδίου του νατρίου (NaN3) και αιθανόλης σε οξιράνιο παρουσία χλωριούχου αμμώνιου (NH4Cl) και στη συνέχεια επίδραση διαλύματος τριφαινυλοφωσφίνης σε αιθανονιτρίλιο[10]:
2. Με επίδραση αμμωνίας σε οξιράνιο παράγεται 2-αμιναιθανόλη, που στη συνέχεια δίνει αζιριδίνη, όπως στην §2.1.:
Από δι(βρωμομεθυλ)αμίνη
[Επεξεργασία | επεξεργασία κώδικα]Με τη χρήση ενδομοριακής αντίδρασης Würtz σε δι(βρωμομεθυλ)αμίνη[11][12]
- Όμως η απόδοση αυτής της αντίδρασης είναι σχετικά μικρή, αφού ταυτόχρονα διεξάγεται αναπόφευκτα και διαμοριακή[13]:
- Σήμερα χρησιμοποιείται περισσότερο η τροποποιημένη αντίδραση Freund με Zn, που δίνει μεγαλύτερη απόδοση στην ενδομοριακή αντίδραση. Σ' αυτήν την περίπτωση η στοιχειομετρική εξίσωση της αντίδρασης γίνεται[14][15]:
Χημικές ιδιότητες και παράγωγα
[Επεξεργασία | επεξεργασία κώδικα]- Η αζιριδίνη συμπεριφέρεται ως δευτεροταγής αμίνη. Ο τριμελής δακτύλιος διανοίγεται (με 1,3-κυκλοπροσθήκη) με αρκετά πυρηνόφιλα αλλά και ηλεκτρονιόφιλα αντιδραστήρια.[16]:
N-ακυλίωση
[Επεξεργασία | επεξεργασία κώδικα]Αντιδρά με ακυλαλογονίδια (RCOX), παράγοντας N-ακυλαζιριδίνη:
Ν-αλογόνωση
[Επεξεργασία | επεξεργασία κώδικα]Αντιδρά με υπαλογονώδη άλατα (π.χ. NaOX), παράγοντας N-αλαζιριδίνη:
N-λιθίωση
[Επεξεργασία | επεξεργασία κώδικα]Αντιδρά με το μεθυλολίθιο (CH3Li), παράγοντας N-λιθιαζιριδίνη και μεθάνιο:
N-αλκυλίωση
[Επεξεργασία | επεξεργασία κώδικα]Στην περίπτωση της αλκυλίωσης, με επίδραση (περίσσειας) αλκυλαλογονιδίων (RX), διανοίγεται ο τριμελής δακτύλιος δίνοντας άκυκλη 2-αλο-Ν,Ν-διαλκυλαιθαναμίνη ή και αλογονούχο 2-αλο-Ν,Ν-τριαλκυλαιθαναμμώνιο:
Με νιτρωδυλοχλωρίδιο
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση νιτρωδυλοχλωρίδιου (NOCl) παράγεται αιθένιο, υδροχλώριο και υποξείδιο του αζώτου (N2O):
Με φαινόλη
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση φαινόλης (PhOH) παράγεται 2-φαινοξυαιθαναμίνη:
Με υδραλογόνο
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση υδραλογόνου (HX) παράγεται αρχικά 2-αλαιθαναμίνη (XCH2CH2NH2) και με περίσσεια υδραλογόνου αλογονούχο 2-αλαιθαναμμώνιο ([XCH2CH2NH3]X)[17]:
Με υδρογόνο
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση υδρογόνου παρουσία λευκοχρύσου παραγεται αιθαναμίνη:
Τοξικολογική επίδραση στον ανθρώπινο οργανισμό
[Επεξεργασία | επεξεργασία κώδικα]Ως ηλεκτρονιόφιλη, η αζιριδίνη αντιδρά με πυρηνόφιλα, όπως οι αζωτούζες βάσεις του DNA, καταλήγοντας εν δυνάμει σε μετάλλαξη[18][19][20].
Πηγές πληροφόρησης
[Επεξεργασία | επεξεργασία κώδικα]- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ ΈκδοσηΘεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Διαδικτυακοί τόποι που αναφέρονται στις «Αναφορές και παρατηρήσεις».
Παραπομπές και παρατηρήσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985, σελ. 23, §2.3Β.
- ↑ Gilchrist, T.L. Heterocyclic chemistry. ISBN 0-582-01421-2.
- ↑ Epoxides and aziridines – A mini review Albert Padwaa and S. Shaun Murphreeb Arkivoc (JC-1522R) pp. 6–33 Online article
- ↑ Σημείωση: Είναι ακόμη δυνατό δύο (2) ομάδες R να παριστάνουν μαζί μια δισθενή ομάδα.
- ↑ Σημείωση: Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ Στις παρακάτω στοιχειομετρικές εξισώσεις περιγράφονται μέθοδοι παραγωγής της «μητρικής» αζιριδίνης, για λόγους απλούστευσης. Η παραγωγή των «θυγατρικών» ενώσεων πραγματοποιείται (συνήθως) με κατάλληλη προσαρμογή των μεθόδων παραγωγής της «μητρικής».
- ↑ Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985, σελ. 22, §2.3Α.
- ↑ Σύνθεση Γουένκερ (Wenker synthesis).
- ↑ Μέθοδος Γκάμπριελ: Παραγωγή αζιριδίνης από 2-βρωμαιθαναμίνη[νεκρός σύνδεσμος]. Γενίκευση και για άλλα αλογόνα.
- ↑ Readily Available Unprotected Amino Aldehydes Ryan Hili and Andrei K. Yudin J. Am. Chem. Soc.; 2006; 128(46) pp 14772 - 14773; (Communication)
- ↑ August Freund (1881). "Über Trimethylen". Journal für Praktische Chemie 26 (1): 625–635. doi:10.1002/prac.18820260125.
- ↑ August Freund (1882). "Über Trimethylen". Monatshefte für Chemie 3 (1): 625–635. doi:10.1007/BF01516828.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 152, §6.2.2.
- ↑ G. Gustavson (1887). "Ueber eine neue Darstellungsmethode des Trimethylens". J. Prakt. Chem. 36: 300–305. doi:10.1002/prac.18870360127. http://gallica.bnf.fr/ark:/12148/bpt6k90799n/f308.table.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 154, §6.5.Β1.
- ↑ Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985, σελ. 23-25, §2.3Γ.
- ↑ Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985, σελ. 23, §2.3.
- ↑ Kanerva L, Keskinen H, Autio P, Estlander T, Tuppurainen M, Jolanki R (May 1995). "Occupational respiratory and skin sensitization caused by polyfunctional aziridine hardener". Clin Exp Allergy 25 (5): 432–9. doi:10.1111/j.1365-2222.1995.tb01074.x. PMID 7553246.
- ↑ Sartorelli P, Pistolesi P, Cioni F, Napoli R, Sisinni AG, Bellussi L, Passali GC, Cherubini Di Simplicio E, Flori L (2003). "Skin and respiratory allergic disease caused by polyfunctional aziridine". Med Lav 94 (3): 285–95. PMID 12918320.
- ↑ Mapp CE (2001). "Agents, old and new, causing occupational asthma". Occup. Environ. Med. 58 (5): 354–60. doi:10.1136/oem.58.5.354. PMC 1740131. PMID 11303086.




![{\displaystyle \mathrm {+NaN_{3}+CH_{3}CH_{2}OH{\xrightarrow[{65^{o}C,\;NH_{4}Cl,\;5h}]{-CH_{3}CH_{2}ONa}}N_{3}CH_{2}CH_{2}OH{\xrightarrow[{83^{o}C,\;CH_{3}CN,\;5h}]{+PPh_{3}}}POPh_{3}+N_{2}+} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/e284ddf35ea8aef50ef0a1efc2ac826c2a2e9b50)








![{\displaystyle \mathrm {+2RX{\xrightarrow {-HX}}XCH_{2}CH_{2}NR_{2}{\xrightarrow {+RX}}[XCH_{2}CH_{2}NR_{3}]X} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/47d588863830087e14f9a7981f299af64eee54f8)


![{\displaystyle \mathrm {+HX{\xrightarrow {-HX}}XCH_{2}CH_{2}NH_{2}{\xrightarrow {+HX}}[XCH_{2}CH_{2}NH_{3}]X} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/f8898bcaa4d0121314b955ee630475a177214b5f)
