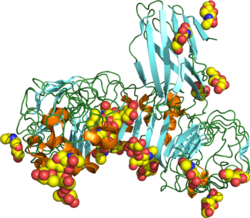
TLR4

Le récepteur Toll Like 4, ou TLR4, parfois également nommé CD284 (Cluster de différenciation 284),est un activateur clé de la réponse immunitaire innée et joue un rôle central dans la lutte contre les infections bactériennes. TLR4 est une protéine transmembranaire d'environ 95 kDa codée par le gène TLR4.
TLR4 appartient à la famille des récepteurs de type toll (TLR), représentative des récepteur de reconnaissance de motifs moléculaires (PRR, pattern recognition receptors). Les PRR sont ainsi nommés pour leur capacité à reconnaître des composants de micro-organismes (bactéries, virus, champignons et parasites) conservés au cours de l'évolution, appelés motifs moléculaires associés aux agents pathogènes (PAMP, pathogen associated molecular pattern). La reconnaissance d'un PAMP par un PRR déclenche une activation rapide de l'immunité innée, essentielle pour lutter contre les maladies infectieuse[5].
TLR4 est exprimé par les cellules immunitaires principalement d’origine myéloïdes, incluant les monocytes, macrophages et cellules dendritiques (DC, dendritic cell). Il est également exprimé à un niveau plus faible dans certaines cellules non immunitaires, telles que les cellules épithéliales, endothéliales, placentaires, et les cellules bêta des ilôts de Langerhans. La plupart des cellules myéloïdes expriment également des niveaux élevés de la protéine CD14 ancrée à la membrane plasmique. Celle-ci facilite l’activation de TLR4 par les LPS et contrôle son internalisation subséquente, importante pour la signalisation du récepteur et sa dégradation[6],[7].
Les principaux ligands du TLR4 sont les lipopolysaccharides (LPS), composants majoritaires de la membrane externe des bactéries Gram-négatives et de certaines bactéries Gram-positives. Le TLR4 peut également être activé par des composés endogènes appelés motifs moléculaires associés aux danger (DAMP, damage associated molecular pattern), notamment la protéine HMGB1 (high mobility group box protein 1), les protéines S100 ou les histones. Ces composés sont libérés lors de lésions tissulaires et par les cellules mourantes ou nécrotiques[8],[9],[10].
Rôles du TLR 4
[modifier | modifier le code]Les TLR sont hautement conservés de la Drosophile à l'homme et partagent des similitudes structurelles et fonctionnelles. Ils reconnaissent les motifs moléculaires associés aux agents pathogènes (PAMP pour Pathogen-Associated Molecular Pattern) qui sont exprimés sur des agents infectieux et interviennent dans la production de cytokines nécessaires au développement d'une immunité efficace.
Son activation conduit à une voie de signalisation intracellulaire NF-κB et à la production de cytokines inflammatoires, responsables de l'activation du système immunitaire inné[11]. Il est bien connu pour la reconnaissance du lipopolysaccharide (LPS), aussi nommé endotoxine, un composant présent dans de nombreuses bactéries à Gram négatif (par exemple Neisseria spp.) et certaines bactéries à Gram positif. Ses ligands comprennent également plusieurs protéines virales, un polysaccharide et diverses protéines endogènes telles que les lipoprotéines de basse densité, les bêta-défensines et la protéine de choc thermique[12].
Plusieurs variantes de transcription de ce gène ont été trouvées, mais le potentiel de codage de protéines de la plupart d'entre elles est incertain[13].
La plupart des effets rapportés de la signalisation de TLR4 dans les tumeurs sont pro-cancérigènes, principalement en raison des contributions de la signalisation de cytokines pro-inflammatoires (dont l'expression est dirigée par des signaux médiés par TLR) au micro-environnement favorisant les tumeurs[14].
Liaison endotoxine (LPS) avec TLR 4
[modifier | modifier le code]La liaison entre le LPS et le récepteur TLR 4 est possible après une fixation du LPS à un corécepteur membranaire MD2 (chaînes C et D), aussi connu sous le nom LY96, au préalable. La liaison du LPS au corécepteur membranaire MD2 permet le rapprochement et l'homodimérisation des deux chaînes de TLR4, activant leurs domaines intracytosoliques respectifs qui recrutent des protéines intracellulaires dans le but d'initier une réponse inflammatoire[15].
Le récepteur CD14 est également un partenaire du TLR 4. En intracellulaire, diverses protéines fixées au domaine intracytosolique du TLR 4 sont recrutées, telle que MyD88 (Myeloid differentiation primary gene 88). En aval, l'activation d'une cascade de protéines impliquées dans diverses voies classiques (celle des MAP kinases ou encore celle de NF-κB) permet ensuite au macrophage activé par la stimulation de ses récepteurs TLR 4 d'être un acteur de l'inflammation (notamment en sécrétant du monoxyde d'azote, par exemple, si activation de NF-κB qui peut stimuler la transcription de la Nitric Oxyde Synthase 2 (iNOS) ou celle de cytokines pro-inflammatoires.
Signalisation
[modifier | modifier le code]Lors de la reconnaissance du LPS, les changements de conformation des récepteurs TLR4 entraînent le recrutement de domaines TIR intracellulaires contenant des molécules adaptatrices. Ces adaptateurs sont associés au cluster TLR4 via des interactions homophiles entre les domaines TIR. Il existe quatre protéines adaptatrices impliquées dans deux voies majeures de signalisation intracellulaire[16].
Il coopère avec LY96 (également appelé MD-2) et CD14 pour jouer un rôle dans les événements de transduction du signal induits par le lipopolysaccharide (LPS)[17] présent dans la plupart des bactéries à Gram négatif. Des mutations dans ce gène ont été associées à des différences de réactivité des LPS.
La signalisation TLR4 répond aux signaux en formant un complexe à l'aide d'un domaine extracellulaire de répétition riche en leucine (LRR pour Leucin-Rich Repeat) et d'un domaine intracellulaire de récepteurs toll/interleukine-1 (TIR). La stimulation par le LPS induit une série d'interactions avec plusieurs protéines accessoires qui forment le complexe TLR4 à la surface de la cellule. La reconnaissance du LPS est initiée par une liaison du LPS à une protéine LBP. Ce complexe LPS-LBP transfère le système LPS sur CD14. CD14 est une protéine membranaire ancrée dans le glycosyl-phosphatidyl-inositol qui lie le complexe LPS-LBP et facilite le transfert du LPS à la protéine MD-2, associée au domaine extracellulaire de TLR4. La liaison au LPS favorise la dimérisation de TLR4/MD-2. Les changements conformationnels du TLR4 induisent le recrutement de protéines adaptatrices intracellulaires contenant le domaine TIR, nécessaires pour activer la voie de signalisation en aval[18].

Voie dépendante de MyD88
[modifier | modifier le code]La voie dépendante de MyD88 est régulée par deux protéines associées à l'adaptateur : le gène de réponse primaire de différenciation myéloïde 88 (MyD88) et la protéine adaptatrice contenant le domaine TIR (TIRAP). TIRAP-MyD88 régule l'activation précoce de NF-κβ et la production de cytokines pro-inflammatoires, telles que l'IL-12[11]. La signalisation MyD88 implique l'activation des kinases associées au récepteur de l'IL-1 (IRAK) et du facteur 6 du facteur associé au récepteur de TNF (TRAF6). TRAF6 induit l'activation de TAK1 (facteur de croissance transformant-kinase activée-β) qui conduit à l'activation de cascades MAPK (protéine kinase activée par un mitogène) et d' IKK (kinase IKB). La voie de signalisation d'IKK conduit à l'induction du facteur de transcription NF-KB, tandis que l'activation des cascades de MAPK entraîne l'activation d'un autre facteur de transcription AP-1. Les deux jouent un rôle dans l'expression des cytokines pro-inflammatoires[18]. L'activation de NF-KB par TAK-1 est complexe et commence par l'assemblage d'un complexe protéique appelé signalosome, constitué d'une protéine d'échafaudage appelée NEMO. Le complexe protéique est constitué de deux kinases κB différentes, appelées IKKα et IKKβ. Cela provoque l'ajout d'une petite protéine régulatrice au signalosome appelée ubiquitine, qui déclenche la libération de la protéine NF-KB, qui coordonne la translocation dans le noyau des cytokines[19].
Voie indépendante de MyD88
[modifier | modifier le code]Cette voie dépendante de TRIF implique le recrutement de protéines adaptatrices TIR-domain-containing adaptator containing interféron-β (TRIF) et la molécule adaptatrice apparentée au TRIF (TRAM). Les signaux TRAM-TRIF activent le facteur de transcription Interferon Regulatory Factor-3 (IRF3) via TRAF3. L'activation d'IRF3 induit la production d' interférons de type 1[16].
SARM: régulateur négatif de la voie médiée par le TRIF
[modifier | modifier le code]Une cinquième protéine adaptatrice contenant un domaine TIR appelée Sterile α and HEAT (motif Armadillo) (SARM) est un inhibiteur de la voie de signalisation TLR4. L'activation de SARM par la liaison au LPS inhibe les voies médiées par le TRIF mais n'inhibe pas les voies médiées par MyD88. Ce mécanisme empêche une activation excessive en réponse au LPS, ce qui peut entraîner des lésions induites par l'inflammation, telles que la septicémie[18].
Histoire évolutive
[modifier | modifier le code]Le TLR4 a été créé lorsque les TLR2 et TLR4 ont divergé il y a environ 500 millions d'années, au début de l'évolution des vertébrés[20]. Les alignements de séquence d'exons de TLR4 humains et de grands singes ont démontré qu'il n'y a pas eu beaucoup d'évolution dans TLR4 humain depuis notre divergence par rapport à notre dernier ancêtre commun avec les chimpanzés. Les exons de TLR4 humain et de chimpanzé ne diffèrent que par trois substitutions, tandis que les humains et les babouins sont similaires à 93,5 % dans le domaine extracellulaire[21]. Notamment, les humains possèdent un plus grand nombre de codons d'arrêt précoce dans TLR4 que les grands singes; dans une étude portant sur 158 humains dans le monde, 0,6 % avaient une mutation non-sens[22],[23]. Cela suggère qu'il existe des pressions évolutives plus faibles sur le TLR4 humain que sur nos parents de primates. La distribution des polymorphismes humains de TLR4 correspond à la migration extra-africaine et il est probable que les polymorphismes aient été générés en Afrique avant la migration vers d'autres continents[23],[24].
Les interactions
[modifier | modifier le code]Il a été démontré que TLR4 interagissait avec :
Le trafic intracellulaire de TLR4 dépend de la GTPase Rab-11a et l’inactivation de Rab-11a freine le recrutement de TLR4 vers les phagosomes contenant E. coli et, par la suite, réduit la transduction du signal par la voie indépendante MyD88[33].
Signification clinique
[modifier | modifier le code]Divers polymorphismes mono-nucléotidiques (SNP) du TLR4 chez l'homme ont été identifiés[34] et pour certains d'entre eux, une association avec une susceptibilité accrue aux infections bactériennes à Gram négatif[35] ou une progression plus rapide et une évolution plus sévère de la septicémie chez les patients gravement malades patients ont été signalées[36].
Résistance à l'insuline
[modifier | modifier le code]Fetuin-A facilite la liaison des lipides aux récepteurs, induisant ainsi une résistance à l'insuline[37].
Dans la progression des cancers
[modifier | modifier le code]L'expression de TLR4 peut être détectée sur de nombreuses cellules tumorales et lignées cellulaires. TLR4 est capable d'activer les voies MAPK et NF-κB, impliquant le rôle direct possible de la signalisation TLR4 autonome de cellules dans la régulation de la cancérogenèse, notamment par la prolifération accrue de cellules tumorales, l'inhibition de l'apoptose et les métastases. La signalisation de TLR4 peut également contribuer à la résistance à la chimiothérapie au paclitaxel dans le cancer de l'ovaire et à la thérapie par siRNA dans le cancer de la prostate. Il a été rapporté que 63 % des patientes atteintes d' un cancer du sein exprimaient TLR4 sur des cellules tumorales et que le niveau d'expression était inversement corrélé à la survie. De plus, une faible expression de MyD88 était corrélée à une diminution des métastases pulmonaires et à une diminution de l'expression des CCL2 et CCL5. Les niveaux d'expression de TLR4 étaient les plus élevés parmi les TLR dans la lignée de cellules de cancer du sein humain MDA-MB-231 et l'inactivation de TLR4 a entraîné une diminution de la prolifération et une diminution des niveaux d'IL-6 et d'IL-8. D'autre part, la signalisation de TLR4 dans les cellules immunitaires et inflammatoires du microenvironnement tumoral peut conduire à la production de cytokines proinflammatoires (TNF, IL-1β, IL-6, IL-18, etc.) de cytokines immunosuppressives (IL-10, TGF- β, etc.) et des médiateurs angiogéniques (VEGF, EGF, TGF-β, etc.). Ces activités peuvent entraîner une polarisation plus poussée des macrophages associés à une tumeur, la conversion de fibroblastes en fibroblastes associés au cancer favorisant la tumeur, la conversion de cellules dendritiques en CD associées à une tumeur et l'activation des fonctions pro-tumorigènes de cellules myéloïdes immatures - Suppresseur d'origine myéloïde Cellules (MDSC). La signalisation TLR a été liée à l'accumulation et à la fonction de MDSC au site de la tumeur et permet également aux cellules stromales mésenchymateuses de contrer l'immunité anti-tumorale médiée par les cellules NK. Dans les cellules de l'hépatoblastome HepG2, le LPS augmentait les niveaux de TLR4, la prolifération cellulaire et la résistance à la chimiothérapie, et ces phénomènes pourraient être inversés par l'inactivation du gène TLR4. De manière similaire, la stimulation par LPS de la lignée cellulaire H7402 de cancer du foie humain a entraîné une régulation à la hausse de TLR4, l'activation de NF-KB, la production de TNF, IL-6 et IL-8 et une prolifération accrue pouvant être inversée par un transducteur de signal et une inhibition de STAT3. Outre l'utilisation réussie bien connue de Bacillus Calmette–Guérin (BCG) dans le traitement du cancer de la vessie, il existe des rapports sur le traitement du carcinome épidermoïde oral, du cancer gastrique et du cancer du col de l'utérus avec la préparation de streptocoque lyophilisée OK-432 et l'utilisation de ligands de TLR4/TLR2 dérivés du muramyl dipeptide[14].
Pendant la grossesse
[modifier | modifier le code]L'activation de TLR4 dans les infections intra-utérines entraîne une dérégulation de la synthèse des prostaglandines, entraînant une contraction du muscle lisse utérin.
Polymorphisme Asp299Gly
[modifier | modifier le code]Classiquement, TLR4 est considéré comme le récepteur du LPS, mais il a également été démontré que TLR4 était également activé par d'autres types de lipides. Plasmodium falciparum, un parasite connu pour causer la forme de paludisme la plus répandue et la plus grave rencontrée principalement en Afrique, produit du glycosylphosphatidylinositol, qui peut activer le TLR4[38]. Deux SNP dans TLR4 sont co-exprimés avec une forte pénétrance dans les populations africaines (c.-à-d. TLR-4-Asp299Gly et TLR-4-Thr399Ile). Ces polymorphismes sont associés à une augmentation de la production d'IL-10 à médiation par TLR4 - un immunomodulateur - et à une diminution des cytokines proinflammatoires[39]. La mutation ponctuelle TLR-4-Asp299Gly est fortement corrélée à un taux d'infection accru avec Plasmodium falciparum. Il semble que la mutation empêche le TLR4 d’agir aussi vigoureusement contre au moins certaines infections plasmodiales. Le taux d'infection paludique et la morbidité associée sont plus élevés dans le groupe TLR-4-Asp299Gly, mais la mortalité semble avoir diminué. Cela peut indiquer qu’au moins une partie de la pathogenèse du paludisme tire parti de la production de cytokines. En réduisant la production de cytokines via la mutation de TLR4, le taux d’infection peut augmenter, mais le nombre de décès dus à l’infection semble diminuer[38].
De plus, TLR4-D299G a été associé au cancer colorectal agressif chez l'homme. Il a été démontré que les adénocarcinomes du côlon humain chez les patients atteints de TLR4-D299G étaient plus fréquemment à un stade avancé avec métastases que ceux portant un TLR4 de type sauvage. La même étude a démontré fonctionnellement que les cellules épithéliales intestinales (Caco-2) exprimant TLR4-D299G subissaient une transition épithélio-mésenchymateuse et des modifications morphologiques associées à la progression tumorale, contrairement aux cellules épithéliales intestinales exprimant le TLR4 sauvage[40].
Études animales
[modifier | modifier le code]Un lien entre le récepteur TLR4 et la consommation excessive d'alcool a été suggéré. Lorsque les gènes responsables de l'expression des récepteurs TLR4 et GABA sont manipulés chez des rongeurs élevés et entraînés à boire de manière excessive, les animaux ont montré une "réduction profonde" des comportements de consommation d'alcool[41]. De plus, il a été démontré que l’éthanol, même en l’absence de LPS, peut activer les voies de signalisation du TLR4[42].
Des niveaux élevés de molécules TLR4 et de macrophages associés aux tumeurs M2 sont associés à une susceptibilité accrue à la croissance du cancer chez les souris privées de sommeil. Les souris génétiquement modifiées afin qu'elles ne puissent pas produire de molécules de TLR4 ont montré une croissance normale du cancer[43].
Particularités et pathologies
[modifier | modifier le code]- Du fait de la consommation d'aliments hyperlipidiques, la composition du microbiote intestinal est susceptible d'être gravement modifiée, pouvant induire une hausse de la concentration plasmatique en LPS. Dans une échéance plus brève, l’ingestion d’un repas riche en lipides induit également une augmentation du LPS plasmatique en postprandial[44],[45]. Ces données pourraient expliquer le rôle physiopathologique du TLR 4 dans le développement d'endotoxémies métaboliques chez l’obèse[46].
- Une déficience en MyD88 semble ne pas être nécessairement pathologique, car le TLR 4 peut dans ce cas activer une voie redondante qui aura des effets similaires. L'activation de ces voies sera en revanche d'une durée plus longue que dans le cas où MyD88 est présent.
Substances ciblant le TLR4
[modifier | modifier le code]Le récepteur Toll-like 4 s'est révélé important pour les effets secondaires à long terme des analgésiques opioïdes. Différents ligands de récepteurs μ-opioïdes ont été testés et ont également démontré leur efficacité en tant qu'agonistes ou antagonistes du TLR4, les agonistes opioïdes tels que la morphine étant des agonistes du TLR4, alors que des antagonistes des opioïdes tels que la naloxone étaient des antagonistes du TLR4. L'activation de TLR4 entraîne la libération en aval de modulateurs inflammatoires, y compris le TNF-α et l'interleukine-1. On pense qu'une libération constante de ces modulateurs réduit l'efficacité du traitement par les opioïdes au fil du temps et contribue à la fois au développement de la tolérance aux analgésiques opioïdes[47],[48] et à l’émergence d’effets secondaires tels que l’hyperalgésie et l’allodynie, qui peuvent devenir un problème après une utilisation prolongée d’opioïdes[49],[50]. Les médicaments qui bloquent l'action du TNF-α ou de l'IL-1β augmentent les effets analgésiques des opioïdes et réduisent le développement de la tolérance et d'autres effets secondaires[51],[52], ce qui a également été démontré avec des médicaments qui bloquent TLR4 lui-même. La réponse de TLR4 aux médicaments opioïdes s’est révélée être dépendante des énantiomères. Par conséquent, les énantiomères "non naturels" des médicaments opioïdes tels que la morphine et la naloxone, qui n'ont pas d’affinité pour les récepteurs opioïdes, produisent toujours la même activité sur TLR4 que les énantiomères"normaux"[53],[54]. Cela signifie que les énantiomères non naturels d'antagonistes des opioïdes, tels que la (+)-naloxone, peuvent être utilisés pour bloquer l'activité TLR4 des médicaments analgésiques opioïdes, sans affecter l'activité analgésique médiée par le récepteur μ-opioïde[55],[54],[56]. Cela pourrait également être le mécanisme à l'origine de l'effet bénéfique de la naltrexone à ultra-faible dose sur l'analgésie opioïde[57].
La morphine provoque une inflammation en se liant à la protéine antigène lymphocytaire 96, qui à son tour provoque la liaison de la protéine au récepteur de type Toll 4 (TLR4)[58]. L'activation de TLR4 induite par la morphine atténue la suppression de la douleur causée par les opioïdes et améliore le développement de la tolérance aux opioïdes et de la dépendance, de la toxicomanie et d'autres effets indésirables tels que la dépression respiratoire et l'hyperalgésie. Les médicaments candidats ciblant le TLR4 pourraient améliorer les traitements de la douleur basés sur les opioïdes[59].
Agonistes
[modifier | modifier le code]- Buprenorphine
- Carbamazepine
- Ethanol[60]
- Fentanyl
- Lévorphanol
- Lipopolysaccharides (LPS)[61]
- Méthadone
- Morphine
- Oxcarbazepine
- Oxycodone
- Péthidine
- Glucuronoxylomannane de Cryptococcus[62],[63]
- Morphine-3-glucuronide (inactif au niveau des récepteurs opioïdes, donc sélectif pour l'activation de TLR4)[50]
- Tapentadol (agoniste / antagoniste mixte)
- Les isomères "non naturels" tels que la (+)- morphine activent TLR4 mais manquent d'activité des récepteurs opioïdes[53], bien que la (+)- morphine montre également une activité en tant qu'agoniste des récepteurs sigma[64].
Antagonistes
[modifier | modifier le code]- Le lipide A, un analgésique, agit en tant qu’antagoniste de TLR4. Il a été développé comme médicament contre la septicémie grave[65]. Cependant, en 2013, un reportage a déclaré que les résultats contre la septicémie étaient quelque peu décevants et qu'il était mieux utilisé pour traiter certains cas de grippe sévère. Bien qu'il ne traite pas le virus lui-même, il pourrait être utilisé contre la réaction immunitaire massive appelée tempête de cytokines, qui survient souvent plus tard au cours de l'infection et constitue une cause majeure de mortalité due à une grippe sévère[66].
- Amitriptyline[67]
- Cyclobenzaprine[67]
- Kétotifène[67]
- Imipramine[67]
- Miansérine[67]
- Ibudilast[68]
- Pinocembrine[69]
- Naloxone[70]
- Naltrexone[70]
- (+)-naltrexone[70]
- LPS-RS[70]
- Propentofylline
- Tapentadol (agoniste et antagoniste)
- (+)- naloxone (isomère « non naturel », sans affinité pour les récepteurs opioïdes, donc sélectif pour l'inhibition de TLR4)[54]
Voir aussi
[modifier | modifier le code]Notes et références
[modifier | modifier le code]- GRCh38: Ensembl release 89: ENSG00000136869 - Ensembl, May 2017
- GRCm38: Ensembl release 89: ENSMUSG00000039005 - Ensembl, May 2017
- « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- (en) Céline Vaure et Yuanqing Liu, « A Comparative Review of Toll-Like Receptor 4 Expression and Functionality in Different Animal Species », Frontiers in Immunology, vol. 5, (ISSN 1664-3224, DOI 10.3389/fimmu.2014.00316, lire en ligne, consulté le )
- (en) Karsten Mahnke, Eva Becher, Paola Ricciardi-Castagnoli et Thomas A. Luger, « CD14 is Expressed by Subsets of Murine Dendritic Cells and Upregulated by Lipopolysaccharide », dans Dendritic Cells in Fundamental and Clinical Immunology: Volume 3, Springer US, , 145–159 p. (ISBN 978-1-4757-9966-8, DOI 10.1007/978-1-4757-9966-8_25, lire en ligne)
- (en) Ian Sabroe, Elizabeth C. Jones, Lynne R. Usher et Moira K. B. Whyte, « Toll-Like Receptor (TLR)2 and TLR4 in Human Peripheral Blood Granulocytes: A Critical Role for Monocytes in Leukocyte Lipopolysaccharide Responses », The Journal of Immunology, vol. 168, no 9, , p. 4701–4710 (ISSN 0022-1767 et 1550-6606, DOI 10.4049/jimmunol.168.9.4701, lire en ligne, consulté le )
- (en) Huan Yang, Haichao Wang, Zhongliang Ju et Ahmed A. Ragab, « MD-2 is required for disulfide HMGB1–dependent TLR4 signaling », Journal of Experimental Medicine, vol. 212, no 1, , p. 5–14 (ISSN 1540-9538 et 0022-1007, PMID 25559892, PMCID PMC4291531, DOI 10.1084/jem.20141318, lire en ligne, consulté le )
- (en) Dianhua Jiang, Jiurong Liang, Juan Fan et Shuang Yu, « Regulation of lung injury and repair by Toll-like receptors and hyaluronan », Nature Medicine, vol. 11, no 11, , p. 1173–1179 (ISSN 1546-170X, DOI 10.1038/nm1315, lire en ligne, consulté le )
- (en) Hongliang Fang, Bing Ang, Xinyun Xu et Xiaohui Huang, « TLR4 is essential for dendritic cell activation and anti-tumor T-cell response enhancement by DAMPs released from chemically stressed cancer cells », Cellular & Molecular Immunology, vol. 11, no 2, , p. 150–159 (ISSN 2042-0226, DOI 10.1038/cmi.2013.59, lire en ligne, consulté le )
- « A comparative review of toll-like receptor 4 expression and functionality in different animal species », Frontiers in Immunology, vol. 5, , p. 316 (PMID 25071777, PMCID 4090903, DOI 10.3389/fimmu.2014.00316)
- « Innate immune pattern recognition: a cell biological perspective », Annual Review of Immunology, vol. 33, , p. 257–90 (PMID 25581309, PMCID 5146691, DOI 10.1146/annurev-immunol-032414-112240)
- « Entrez Gene: TLR4 toll-like receptor 4 »
- « TLR-signaling and proinflammatory cytokines as drivers of tumorigenesis », Cytokine, vol. 89, , p. 127–135 (PMID 26854213, DOI 10.1016/j.cyto.2016.01.021)
- "Crystal structure of the human TLR4-human MD-2-E.coli LPS Ra complex" in Nature 2009 no 458 pages 1191-5
- « The history of Toll-like receptors - redefining innate immunity », Nature Reviews. Immunology, vol. 13, no 6, , p. 453–60 (PMID 23681101, DOI 10.1038/nri3446)
- « O00206 (TLR4_HUMAN) », Uniprot
- « LPS/TLR4 signal transduction pathway », Cytokine, vol. 42, no 2, , p. 145–51 (PMID 18304834, DOI 10.1016/j.cyto.2008.01.006)
- « Signal transduction by the lipopolysaccharide receptor, Toll-like receptor-4 », Immunology, vol. 113, no 2, , p. 153–62 (PMID 15379975, PMCID 1782563, DOI 10.1111/j.1365-2567.2004.01976.x)
- « Evolution of the TIR, tolls and TLRs: functional inferences from computational biology », Current Topics in Microbiology and Immunology, vol. 270, , p. 1–21 (PMID 12467241)
- « Phylogenetic variation and polymorphism at the toll-like receptor 4 locus (TLR4) », Genome Biology, vol. 1, no 1, , RESEARCH002 (PMID 11104518, PMCID 31919, DOI 10.1186/gb-2000-1-1-research002)
- « Different selective pressures shape the evolution of Toll-like receptors in human and African great ape populations », Human Molecular Genetics, vol. 22, no 23, , p. 4829–40 (PMID 23851028, PMCID 3820138, DOI 10.1093/hmg/ddt335)
- « Evolutionary dynamics of human Toll-like receptors and their different contributions to host defense », PLoS Genetics, vol. 5, no 7, , e1000562 (PMID 19609346, PMCID 2702086, DOI 10.1371/journal.pgen.1000562)
- « The evolutionary history of TLR4 polymorphisms in Europe », Journal of Innate Immunity, vol. 4, no 2, , p. 168–75 (PMID 21968286, DOI 10.1159/000329492)
- « Monomeric recombinant MD-2 binds toll-like receptor 4 tightly and confers lipopolysaccharide responsiveness », The Journal of Biological Chemistry, vol. 277, no 26, , p. 23427–32 (PMID 11976338, DOI 10.1074/jbc.M202554200)
- « MD-2, a molecule that confers lipopolysaccharide responsiveness on Toll-like receptor 4 », The Journal of Experimental Medicine, vol. 189, no 11, , p. 1777–82 (PMID 10359581, PMCID 2193086, DOI 10.1084/jem.189.11.1777)
- « Triad3A, an E3 ubiquitin-protein ligase regulating Toll-like receptors », Nature Immunology, vol. 5, no 5, , p. 495–502 (PMID 15107846, DOI 10.1038/ni1066)
- « Toll-like receptor 3 mediates a more potent antiviral response than Toll-like receptor 4 », Journal of Immunology, vol. 170, no 7, , p. 3565–71 (PMID 12646618, DOI 10.4049/jimmunol.170.7.3565)
- « Murine TOLL-like receptor 4 confers lipopolysaccharide responsiveness as determined by activation of NF kappa B and expression of the inducible cyclooxygenase », The Journal of Biological Chemistry, vol. 275, no 44, , p. 34035–40 (PMID 10952994, DOI 10.1074/jbc.M007386200)
- « Mal (MyD88-adapter-like) is required for Toll-like receptor-4 signal transduction », Nature, vol. 413, no 6851, , p. 78–83 (PMID 11544529, DOI 10.1038/35092578)
- « Negative regulation of toll-like receptor-mediated signaling by Tollip », The Journal of Biological Chemistry, vol. 277, no 9, , p. 7059–65 (PMID 11751856, DOI 10.1074/jbc.M109537200)
- « Ni(II) interaction with a peptide model of the human TLR4 ectodomain », J Trace Elem Med Biol., vol. 44, , p. 151-160 (PMID 28965571, DOI 10.1016/j.jtemb.2017.07.006)
- « The Rab11a GTPase controls Toll-like receptor 4-induced activation of interferon regulatory factor-3 on phagosomes », Immunity, vol. 33, no 4, , p. 583–96 (PMID 20933442, DOI 10.1016/j.immuni.2010.09.010)
- « Single nucleotide polymorphisms of Toll-like receptors and susceptibility to infectious disease », The Lancet. Infectious Diseases, vol. 5, no 3, , p. 156–64 (PMID 15766650, DOI 10.1016/S1473-3099(05)01308-3)
- « Relevance of mutations in the TLR4 receptor in patients with gram-negative septic shock », Archives of Internal Medicine, vol. 162, no 9, , p. 1028–32 (PMID 11996613, DOI 10.1001/archinte.162.9.1028)
- « Polymorphisms of the toll-like receptor 2 and 4 genes are associated with faster progression and a more severe course of sepsis in critically ill patients », The Journal of International Medical Research, vol. 42, no 1, , p. 93–110 (PMID 24366499, DOI 10.1177/0300060513504358)
- « Fetuin-A acts as an endogenous ligand of TLR4 to promote lipid-induced insulin resistance », Nature Medicine, vol. 18, no 8, , p. 1279-1285 (PMID 22842477, DOI 10.1038/nm.2851, lire en ligne)
- « Toll-like receptor (TLR) polymorphisms in African children: Common TLR-4 variants predispose to severe malaria », Proceedings of the National Academy of Sciences of the United States of America, vol. 103, no 1, , p. 177–82 (PMID 16371473, PMCID 1324982, DOI 10.1073/pnas.0506803102)
- « Toll-like receptor 4 Asp299Gly/Thr399Ile polymorphisms are a risk factor for Candida bloodstream infection », European Cytokine Network, vol. 17, no 1, , p. 29–34 (PMID 16613760, lire en ligne)
- « Toll-like receptor 4 variant D299G induces features of neoplastic progression in Caco-2 intestinal cells and is associated with advanced human colon cancer », Gastroenterology, vol. 141, no 6, , p. 2154–65 (PMID 21920464, PMCID 3268964, DOI 10.1053/j.gastro.2011.08.043)
- « Binge alcohol drinking is associated with GABAA alpha2-regulated Toll-like receptor 4 (TLR4) expression in the central amygdala », Proceedings of the National Academy of Sciences of the United States of America, vol. 108, no 11, , p. 4465–70 (PMID 21368176, PMCID 3060224, DOI 10.1073/pnas.1019020108)
- « Involvement of TLR4/type I IL-1 receptor signaling in the induction of inflammatory mediators and cell death induced by ethanol in cultured astrocytes », Journal of Immunology, vol. 175, no 10, , p. 6893–9 (PMID 16272348, DOI 10.4049/jimmunol.175.10.6893)
- « Fragmented sleep accelerates tumor growth and progression through recruitment of tumor-associated macrophages and TLR4 signaling », Cancer Research, vol. 74, no 5, , p. 1329–37 (PMID 24448240, PMCID 4247537, DOI 10.1158/0008-5472.CAN-13-3014)
- Erridge, Attina et al. 2007
- Clemente-Postigo, Queipo-Ortuno et al. 2012
- Cani, Bibiloni et al. 2008
- « Interleukin-1 antagonizes morphine analgesia and underlies morphine tolerance », Pain, vol. 115, nos 1–2, , p. 50–9 (PMID 15836969, DOI 10.1016/j.pain.2005.02.003)
- « Dual regulation of mu opioid receptors in SK-N-SH neuroblastoma cells by morphine and interleukin-1β: evidence for opioid-immune crosstalk », Journal of Neuroimmunology, vol. 227, nos 1–2, , p. 26–34 (PMID 20615556, PMCID 2942958, DOI 10.1016/j.jneuroim.2010.06.007)
- « Mechanism of allodynia evoked by intrathecal morphine-3-glucuronide in mice », International Review of Neurobiology, vol. 85, , p. 207–19 (ISBN 9780123748935, PMID 19607972, DOI 10.1016/S0074-7742(09)85016-2)
- « Evidence that intrathecal morphine-3-glucuronide may cause pain enhancement via toll-like receptor 4/MD-2 and interleukin-1beta », Neuroscience, vol. 165, no 2, , p. 569–83 (PMID 19833175, PMCID 2795035, DOI 10.1016/j.neuroscience.2009.10.011)
- « Etanercept restores the antinociceptive effect of morphine and suppresses spinal neuroinflammation in morphine-tolerant rats », Anesthesia and Analgesia, vol. 112, no 2, , p. 454–9 (PMID 21081778, DOI 10.1213/ANE.0b013e3182025b15)
- « An IL-1 receptor antagonist blocks a morphine-induced attenuation of locomotor recovery after spinal cord injury », Brain, Behavior, and Immunity, vol. 25, no 2, , p. 349–59 (PMID 20974246, PMCID 3025088, DOI 10.1016/j.bbi.2010.10.018)
- « The "toll" of opioid-induced glial activation: improving the clinical efficacy of opioids by targeting glia », Trends in Pharmacological Sciences, vol. 30, no 11, , p. 581–91 (PMID 19762094, PMCID 2783351, DOI 10.1016/j.tips.2009.08.002)
- « Non-stereoselective reversal of neuropathic pain by naloxone and naltrexone: involvement of toll-like receptor 4 (TLR4) », The European Journal of Neuroscience, vol. 28, no 1, , p. 20–9 (PMID 18662331, PMCID 2588470, DOI 10.1111/j.1460-9568.2008.06321.x)
- « Proinflammatory cytokines oppose opioid-induced acute and chronic analgesia », Brain, Behavior, and Immunity, vol. 22, no 8, , p. 1178–89 (PMID 18599265, PMCID 2783238, DOI 10.1016/j.bbi.2008.05.004)
- « Possible involvement of toll-like receptor 4/myeloid differentiation factor-2 activity of opioid inactive isomers causes spinal proinflammation and related behavioral consequences », Neuroscience, vol. 167, no 3, , p. 880–93 (PMID 20178837, PMCID 2854318, DOI 10.1016/j.neuroscience.2010.02.011)
- « Ultra-low dose naloxone upregulates interleukin-10 expression and suppresses neuroinflammation in morphine-tolerant rat spinal cords », Behavioural Brain Research, vol. 207, no 1, , p. 30–6 (PMID 19799935, DOI 10.1016/j.bbr.2009.09.034)
- « Neuroscience: Making morphine work better », Nature, vol. 484, no 7395, , p. 419 (DOI 10.1038/484419a)
- Drahl C, « Small Molecules Target Toll-Like Receptors », Chemical & Engineering News,
- Pascual M, Baliño P, Alfonso-Loeches S, Aragón CM, Guerri C, « Impact of TLR4 on behavioral and cognitive dysfunctions associated with alcohol-induced neuroinflammatory damage », Brain, Behavior, and Immunity, vol. 25 Suppl 1, , S80-91 (PMID 21352907, DOI 10.1016/j.bbi.2011.02.012)
- Kelley KW, Dantzer R, « Alcoholism and inflammation: neuroimmunology of behavioral and mood disorders », Brain, Behavior, and Immunity, vol. 25 Suppl 1, , S13-20 (PMID 21193024, PMCID 4068736, DOI 10.1016/j.bbi.2010.12.013)
- « Percutaneous penetration of 2,4-dichlorophenoxyacetic acid and 2,4-D dimethylamine salt in human volunteers », Journal of Toxicology and Environmental Health, vol. 36, no 3, , p. 233–40 (PMID 1629934, DOI 10.1080/15287399209531634)
- « Glucuronoxylomannan, a microbial compound, regulates expression of costimulatory molecules and production of cytokines in macrophages », The Journal of Infectious Diseases, vol. 191, no 1, , p. 127–37 (PMID 15593014, DOI 10.1086/426511)
- « Stereoselective action of (+)-morphine over (-)-morphine in attenuating the (-)-morphine-produced antinociception via the naloxone-sensitive sigma receptor in the mouse », European Journal of Pharmacology, vol. 571, nos 2–3, , p. 145–51 (PMID 17617400, PMCID 2080825, DOI 10.1016/j.ejphar.2007.06.012)
- « Phase 2 trial of eritoran tetrasodium (E5564), a toll-like receptor 4 antagonist, in patients with severe sepsis », Critical Care Medicine, vol. 38, no 1, , p. 72–83 (PMID 19661804, DOI 10.1097/CCM.0b013e3181b07b78)
- « New drug offers novel approach to taming flu virus - Vitals », NBCNews,
- Hutchinson MR, Loram LC, Zhang Y, Shridhar M, Rezvani N, Berkelhammer D, Phipps S, Foster PS, Landgraf K, Falke JJ, Rice KC, Maier SF, Yin H, Watkins LR, « Evidence that tricyclic small molecules may possess toll-like receptor and myeloid differentiation protein 2 activity », Neuroscience, vol. 168, no 2, , p. 551–63 (PMID 20381591, PMCID 2872682, DOI 10.1016/j.neuroscience.2010.03.067)
- Jia ZJ, Wu FX, Huang QH, Liu JM, « [Toll-like receptor 4: the potential therapeutic target for neuropathic pain] », Zhongguo Yi Xue Ke Xue Yuan Xue Bao. Acta Academiae Medicinae Sinicae, vol. 34, no 2, , p. 168–73 (PMID 22776604, DOI 10.3881/j.issn.1000-503X.2012.02.013)
- Lan X, Han X, Li Q, Li Q, Gao Y, Cheng T, Wan J, Zhu W, Wang J, « Pinocembrin protects hemorrhagic brain primarily by inhibiting toll-like receptor 4 and reducing M1 phenotype microglia », Brain, behavior, and immunity, vol. 61, , p. 326–339 (PMID 28007523, PMCID 5453178, DOI 10.1016/j.bbi.2016.12.012)
- Hutchinson MR, Zhang Y, Shridhar M, Evans JH, Buchanan MM, Zhao TX, Slivka PF, Coats BD, Rezvani N, Wieseler J, Hughes TS, Landgraf KE, Chan S, Fong S, Phipps S, Falke JJ, Leinwand LA, Maier SF, Yin H, Rice KC, Watkins LR, « Evidence that opioids may have toll-like receptor 4 and MD-2 effects », Brain, Behavior, and Immunity, vol. 24, no 1, , p. 83–95 (PMID 19679181, PMCID 2788078, DOI 10.1016/j.bbi.2009.08.004)