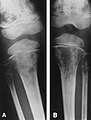
גרורה

 | |
| תחום | אונקולוגיה |
|---|---|
| קישורים ומאגרי מידע | |
| MeSH | D009362 |

גרורה (באנגלית: Metastasis) היא גידול סרטני שנוצר באיבר מרוחק ממקום התפתחות הגידול הראשוני. מקור המונח הלועזי בשפה היוונית, בה משמעות המילה היא הזזה, העברה[1][2].
גרורות באיברים שניוניים מרוחקים הן תוצרים של התהליך הגרורתי הרב שלבי, בו תאים סרטניים ניתקים מן הגידול הראשוני, חודרים לכלי דם או כלי לימפה, נודדים בהם ולבסוף יוצאים מהם ומתיישבים באיברים בגוף המרוחקים מן האיבר בו התפתח הגידול הראשוני[1][2]. האיברים הנוטים יותר לפתח גרורות הם הריאות, הכבד, המוח והעצמות[3].
תהליך יצירת גרורות
[עריכת קוד מקור | עריכה]
גרורות נוצרות בתהליך רב שלבי מורכב. התהליך הגרורתי כולל הינתקות התאים הסרטניים מן הגידול הראשוני, חדירה לכלי דם וכלי לימפה, נדידה ולבסוף יציאה מאותם כלי דם וכלי לימפה והשתרשות באיברים המרוחקים מן האיבר בו התפתח הגידול הראשוני[4]. השתרשות ושגשוג התאים הסרטניים באיבר השניוני יובילו ליצירת גרורות, שהן למעשה גידולים שניוניים.
על מנת שתא סרטני יצליח ליצור גרורות, עליו להשלים את התהליך הגרורתי. התהליך כולל את השלבים הבאים:
- פולשנות מקומית - התאים הסרטניים ניתקים מהגידול הראשוני, חודרים לרקמה בריאה הקרובה אליהם ונזרעים בה.
- חדירה למחזור הדם - התאים הסרטניים חודרים לכלי הדם או כלי לימפה הנמצאים בקרבת מקום ונודדים באמצעותם לאיברים אחרים בגוף.
- יציאה ממחזור הדם - התאים הסרטניים נעצרים או מפסיקים לנוע בכלי דם קטנים, הנקראים נימים, באיבר השניוני המרוחק. אז הם חודרים את הנימים ופולשים לתוך הרקמה של האיבר השניוני.
- התבססות באיברים מרוחקים - התאים הסרטניים מתיישבים ברקמת האיבר השניוני ויוצרים בתחילה מיקרו-גרורות, גידולים קטנים שאינם יכולים להתפתח מעבר לגודל מסוים. מיקרו-גרורות אלה מעודדות יצירה של כלי דם חדשים בסביבתן, מה שמאפשר את התפתחותן למאקרו-גרורות, גידולים גדולים. אספקת הדם נחוצה לתאים הסרטניים על מנת לקבל חמצן וחומרי מזון.
היכולת של תא סרטני להשלים את תהליך יצירת הגרורות תלויה במכלול התכונות שלו. רק תא לו יהיו את כל התכונות הדרושות להשלמת התהליך יצליח להגיע לאיבר מרוחק. גם לאחר ההגעה לאיבר המרוחק, אין כל הבטחה כי התא שצלח את תהליך יצירת הגרורות, יצליח להשתרש באיבר ולשגשג בו. גרורות יכולות להישאר רדומות במשך שנים עד שהן מתחילות לגדול שוב, אם בכלל.
היכולת של תא שהגיע לאיבר שניוני להתרבות וליצור בו גרורות מושפעת, בין היתר, מאינטראקציות של התאים הסרטניים עם סביבת האיבר השניוני[5]. נצפה למשל, שסביבת הריאות מעכבת חיות של תאים סרטניים שיוצרים גרורות בריאות ובכך משפיעה על היכולת ליצור גרורות באיבר זה[6], ייתכן שכחלק ממנגנון ההגנה של הגוף כנגד התקדמות התהליך הסרטני.
מיקום התפתחות גרורות
[עריכת קוד מקור | עריכה]תהליך יצירת הגרורות איננו אקראי - לסרטנים שונים ישנה נטייה לנדוד לאיברים שונים. אבחנה זו נטבעה לראשונה בשנת 1889 על ידי המנתח האנגלי סטיבן פאגט (באנגלית Stephen Paget), אשר טבע את היפותזת ה-Seed and Soil, שאומרת כי גרורות יתפתחו רק כאשר תהיה התאמה בין התא הסרטני (Seed) לבין הסביבה באיבר השניוני אליו הגיע (Soil)[7]. כך למשל, סרטן בלוטת הערמונית יצור לרוב גרורות בעצמות, ואילו סרטן המעי הגס ינדוד לרוב לכבד[8]. אם כן לסביבה באיבר השניוני ישנה השפעה על התפתחות גרורות באיבר זה[9].
| סוג הסרטן | איברים עיקריים להתפתחות גרורות |
|---|---|
| שלפוחית השתן | עצמות, כבד, ריאות |
| סרטן השד | עצמות, כבד, ריאות, מוח |
| סרטן המעי הגס | כבד, ריאות, צפק |
| סרטן הכליות | עצמות, כבד, ריאות, מוח, בלוטת האדרנל |
| סרטן הריאות | עצמות, כבד, ריאות, מוח, בלוטת האדרנל |
| סרטן העור | עצמות, כבד, ריאות, מוח |
| סרטן השחלות | כבד, ריאות, צפק |
| סרטן הלבלב | כבד, ריאות, צפק |
| סרטן בלוטת הערמונית | עצמות, כבד, ריאות, בלוטת האדרנל |
| סרטן הקיבה | כבד, ריאות, צפק |
| סרטן בלוטת התריס | עצמות, כבד, ריאות |
| סרטן הרחם | עצמות, כבד, ריאות, צפק, נרתיק |
תסמינים
[עריכת קוד מקור | עריכה]לרוב, התאים סרטניים נודדים בשלב ראשוני לעבר קשרי לימפה. הריאות, העצמות, גם הכבד והמוח הם איברים נפוצים להתפתחות גרורות[10]. התסמינים השכיחים באיברים הללו הם:
- קשרי לימפה - הרחבת קשרי לימפה
- ריאות - שיעול, יריקת דם וקוצר נשימה
- עצמות - כאב ושברים
- כבד - הגדלה, בחילות וצהבת
- מוח - תסמינים הקשורים למערכת העצבים כגון כאבי ראש, פרכוסים וסחרחורת
לחלק מהחולים, עם זאת, אין תסמינים כלל.
אבחנה
[עריכת קוד מקור | עריכה]גרורות יכולות להימצא בעת האבחנה של הגידול הראשוני או שנים אחריה. כאשר גידולים נוספים מאובחנים בחולה שטופל כנגד סרטן בעבר, לרוב מדובר בגרורות ולא בגידול ראשוני נוסף. אין בדיקה אחת המאבחנת גרורות, בדיקות שונות נחוצות על מנת לאבחן הימצאות או היעדר גרורות. הבדיקות שנעשות נבחרות על פי סוג הגידול הראשוני ועל פי התסמינים אותם מתאר החולה.
בדיקות דם
[עריכת קוד מקור | עריכה]בדיקות דם שגרתיות יכולות להצביע על מדדים חריגים המרמזים על הימצאות גרורות. כך למשל תפקודי כבד חריגים יכולים להצביע על גרורות בכבד. עם זאת, למדדים חריגים אלה יכולים להיות גורמים רבים שאינם סרטן. לרוב, בדיקות הדם תקינות, גם אצל אנשים בעלי מחלה מפושטת ומתקדמת. בסרטנים מסוימים, ישנם סמנים (מרקרים) ספציפיים אשר ניתן למדוד את רמתם בדם, כגון הסמן PSA בסרטן בלוטת הערמונית ו-CA-125 בסרטן השחלות. עלייה ברמת הביטוי של מדדים אלה בדם לעומת רמת הביטוי שלהם בעת האבחנה יכולה להצביע על התקדמות והתפשטות הסרטן ולרמז על פיזור גרורתי.
בדיקות דימות
[עריכת קוד מקור | עריכה]ישנן בדיקות רבות שמטרתן "לצלם תמונות" של איברים שונים בתוך הגוף. בדיקות הדימות (Medical Imaging) שיבוצעו ייבחרו על פי סוג הגידול הראשוני, האיברים המועדפים ליצירת גרורות על ידי הגידול הראשוני ועל פי התסמינים שיתוארו על ידי החולה.
- בצילום רנטגן נבלעות קרני הרנטגן בחומרים צפופים בתוך הגוף, כגון סחוס ועצם, אבל לא על ידי חומרים שאינם צפופים, כמו דם. לכן צילום זה מאפשר לבחון הימצאות גרורות בעצמות הגוף.
- מיפוי עצמות מתבצע באמצעות חומר רדיואקטיבי המאפשר לאבחן נזק בעצמות בכל הגוף. אם אכן נצפה נזק, ניתן לבצע צילום רנטגן על מנת לאפיין את גודל הנזק.
- אולטרה סאונד היא דרך לאבחן הימצאות של גרורות בחלל הבטן. השיטה טובה בזיהוי נוזלים בחלל הבטן ולכן יכולה להבדיל היטב בין ציסטה בכבד שהיא שפירה, לבין גידול מוצק בכבד החשוד כגרורתי.
- בדיקת טומוגרפיה ממוחשבת (CT) היא סוג מתוחכם יותר של צילום רנטגן, הבונה תמונה תלת־ממדית של פנים הגוף. בבדיקה זו ניתן לקבל תמונה של הראש, הצוואר, בית החזה והאגן ולבחון הימצאות גרורות באיברים אלה.
- הדמיית תהודה מגנטית (MRI) מאפשרת להדגים רקמות רכות עם ניגודיות טובה יותר מאשר בטומוגרפיה ממוחשבת (CT), וללא שימוש בקרינה מייננת. השימוש הטוב ביותר לבדיקה זו הוא אבחון הימצאות גידולים סרטניים או גרורות במוח או גרורות בעמוד השדרה.
- טומוגרפיית פליטת פוזיטרונים (PET - positron emission tomography) מאתרת אזורים בגוף בהם יש פעילות חילוף חומרים גבוהה, האופיינית לגידולים ולגרורות. כאשר הבדיקה מסתיימת, אותם אזורים בעלי פעילות חילוף חומרים גבוהה "יידלקו". עם זאת, ישנם תאים סרטניים להם אין פעילות חילוף חומרים גבוהה ולכן לא יזוהו בשיטה זו, וכמו כן, לעיתים "יידלקו" אזורים בהם יש פעילות מוגברת בשל סיבות אחרות שאינן הימצאות תאים סרטניים.
- טומוגרפיית פליטת פוזיטרונים בשילוב טומוגרפיה ממוחשבת (PET-CT): בדיקה זו משלבת את שיטת הטומוגרפיית פליטת פוזיטרונים (PET) ושיטת הטומוגרפיה הממוחשבת (CT). שילוב שתי שיטות אלה יעיל מאוד באיתור מקומות בהם ישנה פעילות חילוף חומרים מוגברת, האופיינית לגידולים ולגרורות. בשילוב שתי השיטות מתקבל כלי הדמיה היכול להבדיל בין ממצא גרורתי לממצא שאינו כזה ולאפיינו היטב מבחינת גודל ומיקום. הבדיקה פחות יעילה בממצאים שגודלם פחות מסנטימטר אחד.
אנדוסקופיה
[עריכת קוד מקור | עריכה]אנדוסקופיה מאפשרת התבוננות באיברים פנימיים באמצעות צינור גמיש אשר בקצהו ישנה מצלמה. לעיתים יוחדר צינור זה בפתחים שקיימים בגוף, כגון פי הטבעת, ולעיתים יצטרך המנתח לעשות חתך קטן דרכו יוחדר הצינור, על מנת לבחון למשל את חלל הבטן. במהלך בדיקה זו ניתן גם לקחת דגימות מרקמות.
ביופסיה
[עריכת קוד מקור | עריכה]לעיתים קרובות, גם לאחר ביצוע בדיקות רבות, הרופאים לא יהיו בטוחים מהו הממצא החשוד, ויהיה צורך לקחת דגימת תאים מהאזור החשוד ולשלוח אותם לבדיקה פתולוגית. תהליך לקיחת דגימה קטנה זו קרוי ביופסיה ומטרתו הוא לאבחן האם הממצא החשוד הוא שפיר או סרטני באמצעות בדיקות של חתכי רקמה (היסטולוגיה).
- צילום רנטגן של גרורות בעצמות
- אולטרה סאונד (US) של גרורות בכבד
- טומוגרפיה ממוחשבת (CT) של גרורה במוח
- הדמיית תהודה מגנטית (MRI) של גרורה במוח
- טומוגרפיית פליטת פוזיטרונים (PET) של גרורות בכבד
- טומוגרפיית פליטת פוזיטרונים בשילוב עם טומוגרפיה ממוחשבת (PET-CT) של גרורות בקשרי לימפה
טיפול
[עריכת קוד מקור | עריכה]הטיפול נקבע ברובו על פי סוג הגידול הראשוני, גודלו, מיקומו, מספר הגרורות ומיקומן, גיל החולה, מצב בריאותו הכללי וסוג טיפולים שקיבל החולה בעבר, אם בכלל. בעת הימצאות גרורות, ישנם מספר טיפולים שיכולים להינתן:
טיפול מערכתי
[עריכת קוד מקור | עריכה]בטיפול מערכתי ניתנים חומרים הנודדים בזרם הדם ובכך משפיעים על כל התאים בגוף. לשיטת טיפול זו שייכים הטיפולים ההורמונליים, כימותרפיה, טיפולים ביולוגיים ורוב הטיפולים הניסיוניים. לרוב כאשר מתגלות גרורות, הטיפול המערכתי הוא הטיפול הנבחר, כיוון שאם התגלו גרורות באיבר מסוים, סביר כי ישנן גרורות באיברים נוספים גם אם לא אובחנו בשיטות הדימות בשל גודלן הקטן.
טיפול מקומי
[עריכת קוד מקור | עריכה]בטיפול מקומי מתמקדים על אזור הגרורה בלבד. לשיטת טיפול זו שייכים הניתוח המקומי להסרת גרורות וטיפול קרינתי, או שילוב של השניים. לרוב, טיפול מקומי זה ייבחר כאשר יהיה צורך בטיפול חזק, ממוקד ומהיר, וכאשר אין זמן להמתין עד שהטיפול המערכתי יגיע לאזורים בהן ישנן גרורות.
טיפול מניעתי
[עריכת קוד מקור | עריכה]לעיתים, כאשר מדובר בסרטנים להם יש נטייה לשלוח גרורות, לאחר הסרת הגידול הראשוני תהיה המלצה לבצע טיפול מניעתי כדי למנוע התפתחות גרורות באיברים מרוחקים. כלומר, הטיפול ימנע מתאים סרטניים בודדים שייתכן והגיעו לאיברים מרוחקים להתפתח לגרורות. הטיפולים המניעתיים יכולים להיות טיפולים מערכתיים או טיפולים מקומיים. לדוגמה טיפול קרינתי למוח בסרטן הריאות[11] או כימותרפיה לחולות בסרטן השד[12].
טיפול להקלה בכאב
[עריכת קוד מקור | עריכה]טיפול להקלה בכאב קרוי גם טיפול פליאטיבי והוא ניתן לעיתים בשילוב עם טיפול מערכתי או טיפול מקומי, ובמקרים אחרים כאשר לא ניתן לטפל כלל הוא ניתן על מנת להקל בתסמינים של החולה אשר לא ניתן לעשות דבר על מנת להצילו.
שיטות הטיפול הקיימות ברובן אינן מצליחות לרפא סרטן גרורתי, על אף שישנם כמה סוגי סרטן, כגון סרטן בלוטת הערמונית וסרטן בלוטת התריס שניתנים לטיפול גם לאחר שליחת גרורות. מדענים רבים בוחנים דרכים חדשות למנוע התפשטות גידולים ראשוניים על מנת לבלום היווצרות גרורות. לפני שטיפול יהפוך לזמין לחולים ברחבי העולם, הוא צריך להיבחן במחקרים קליניים ולהימצא יעיל ובטוח. ישנם מחקרים קליניים רבים המתקיימים בבתי חולים, אוניברסיטאות, מכוני מחקר ועוד. תוצאות של מחקרים קליניים קודמים הובילו להתקדמות בטיפול בסרטן והן לזיהוי, אבחנה ומניעה של המחלה.
סיכויי הישרדות
[עריכת קוד מקור | עריכה]גרורות הן הגורם העיקרי למוות בחולי סרטן. ברוב המקרים, חולים עם מחלה מקומית שאיננה גרורתית ומפושטת הם בעלי סיכויי הישרדות גבוהים יותר משל אלה עם מחלה גרורתית. ראיות שהצטברו במהלך העשורים האחרונים מצביעות על כך ש-60 עד 70 אחוז מהחולים הם בעלי מחלה גרורתית כבר בעת האבחנה. בנוסף, חולים שאינם מציגים מחלה מפושטת בעת האבחנה, עלולים לפתח מחלה גרורתית שתצריך טיפול מתאים. קיומן או העדרן של גרורות, המצביע על התפשטות המחלה, משפיע על דירוג הגידול הסרטני ועל סוג הטיפול שיינתן. על אף שישנם סוגי סרטן גרורתיים שיוכלו להירפא על ידי טיפולים מסוימים, רוב סוגי הסרטן הגרורתיים הם חשוכי מרפא. עם זאת, ישנם טיפולים זמינים לכל החולים עם סרטנים גרורתיים. המטרה העיקרית של הטיפולים הללו היא לשלוט בהתקדמות והתפתחות הגידול ולהקל בתסמינים הנגרמים לחולה בעקבות התהליך הסרטני. במקרים מסוימים, טיפולים נגד סרטנים גרורתיים יאריכו חיים. רוב החולים שמתים מסרטן, מתים מסרטן גרורתי.
ראו גם
[עריכת קוד מקור | עריכה]קישורים חיצוניים
[עריכת קוד מקור | עריכה]- גרורות - האגודה למלחמה בסרטן
- הצלחה ראשונה בניבוי גרורות על סמך בדיקה מכנית של תאים מגידולים סרטניים, אתר "הידען", יולי 2020.
- גרורה, באתר אנציקלופדיה בריטניקה (באנגלית)
 גרורות, דף שער בספרייה הלאומית
גרורות, דף שער בספרייה הלאומית
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ 1 2 Klein, C. A. (2008). "CANCER: The Metastasis Cascade". Science. 321 (5897): 1785–7. doi:10.1126/science.1164853. PMID 18818347.
- ^ 1 2 Chiang, Anne C.; Massagué, Joan (2008). "Molecular Basis of Metastasis". New England Journal of Medicine. 359 (26): 2814–23. doi:10.1056/NEJMra0805239. PMID 19109576.
- ^ Coghlin, Caroline; Murray, Graeme I (2010). "Current and emerging concepts in tumour metastasis". The Journal of Pathology. 222 (1): 1–15. doi:10.1002/path.2727. PMID 20681009.
- ^ Pantel, K; Brakenhoff, RH (2004). "Dissecting the metastatic cascade". Nature reviews. Cancer. 4 (6): 448–56. doi:10.1038/nrc1370. PMID 15170447.
- ^ Maman, Shelly; Witz, Isaac P. (2013). The Tumor Immunoenvironment. p. 15. doi:10.1007/978-94-007-6217-6_2. ISBN 978-94-007-6216-9.
- ^ Maman, Shelly; Edry-Botzer, Liat; Sagi-Assif, Orit; Meshel, Tsipi; Yuan, Weirong; Lu, Wuyuan; Witz, Isaac P. (2013). "The metastatic microenvironment: Lung-derived factors control the viability of neuroblastoma lung metastasis". International Journal of Cancer. 133 (10): 2296. doi:10.1002/ijc.28255.
- ^ Hart, IR (1982). "'Seed and soil' revisited: Mechanisms of site-specific metastasis". Cancer metastasis reviews. 1 (1): 5–16. PMID 6764375.
- ^ Disibio, G; French, SW (2008). "Metastatic patterns of cancers: Results from a large autopsy study". Archives of pathology & laboratory medicine. 132 (6): 931–9. doi:10.1043/1543-2165(2008)132\931:MPOCRF]2.0.CO;2. PMID 18517275.
- ^ Klein-Goldberg, Anat; Maman, Shelly; Witz, Isaac P. (2013). "The role played by the microenvironment in site-specific metastasis". Cancer Letters. doi:10.1016/j.canlet.2013.08.029.
- ^ Leong, SP; Cady, B; Jablons, DM; Garcia-Aguilar, J; Reintgen, D; Jakub, J; Pendas, S; Duhaime, L; Cassell, R; Gardner, M; Giuliano, R; Archie, V; Calvin, D; Mensha, L; Shivers, S; Cox, C; Werner, JA; Kitagawa, Y; Kitajima, M (2006). "Clinical patterns of metastasis". Cancer metastasis reviews. 25 (2): 221–32. doi:10.1007/s10555-006-8502-8. PMID 16770534.
- ^ Yang, GY; Matthews, RH (2000). "Prophylactic cranial irradiation in small-cell lung cancer". The oncologist. 5 (4): 293–8. PMID 10964996.
- ^ Wickerham, DL (2010). "Breast cancer chemoprevention: Progress and controversy". Surgical oncology clinics of North America. 19 (3): 463–73. doi:10.1016/j.soc.2010.03.005. PMC 3034655. PMID 20620921.
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.