תגובת פרידל-קרפטס

תגובות פרידל-קרפטס הן קבוצת תגובות שפותחו על ידי שארל פרידל וג'יימס קרפטס בשנת 1877 המאפשרות לקשור מתמירים לטבעת ארומטית. שני הסוגים העיקריים של תגובות פרידל קרפטס:
התגובות מלוות בהתמרה אלקטרופילית ארומטית. תרשים כללי של תגובת פרידל-קרפטס:

אלקילציית פרידל-קרפטס
[עריכת קוד מקור | עריכה]אליקלצית פרידל-קרפטס היא אלקילציה של טבעת ארומטית באמצעות אלקיל-הליד ושימוש בחומצת לואיס חזקה כזרז. התגובה נעשית בנוכחות FeCl3, והקבוצה האלקילית נקשרת לטבעת הארומטית במקום שבו היה הכלור:

בעיה בתגובה זו היא שהתוצר הוא יותר נוקלאופילי (ריאקטיבי) מהמגיב עקב המתמיר האלקילי הנוסף לטבעת הארומטית, ומימן נוסף עשוי לעבור התמרה עם אלקיל וכך המולקולה עשויה לעבור אלקילציה נוספת. כמו כן אם הכלור לא מצוי על פחמן שלישוני, מתרחשים שחלופים של הקרבוקטיון (בשלב הראשון). שחלופים אלו קורים בשל היציבות היחסית של קרבוקטיון שלישוני על פני קרבוקטיון שניוני או קרבוקטיון ראשוני.
דוגמה לשימוש באלקילציית פרידל-קרפטס היא בייצור אתילבנזן, באמצעות בנזן ואתן בתגובות המבוססות על אלקיציה זו. לאתילבנזן חשיבות בתעשייה הפטרוכימית בהיותו תוצר ביניים בתהליך ייצור סטירן (Styrene), המשמש בהמשך לייצור פוליסטירן.[1]
אצילציית פרידל-קרפטס
[עריכת קוד מקור | עריכה]אצילציית פרידל-קרפטס היא אצילציה של טבעות ארומטיות עם אציל כלוריד ובעזרת חומצת לואיס חזקה כזרז. אצילציית פרידל-קרפטס אפשרית גם עם אנהידרידים. התנאים הדרושים לתגובה דומים לאלו של אלקילציית פרידל-קרפטס. לתגובה זו מספר יתרונות על אלקילציית פרידל-קרפטס: הודות לקבוצת הקרבוניל המושכת אלקטרונים, הקטון הנוצר הוא פחות ריאקטיבי מהמולקולה המקורית, ולכן לא קורות אצילציות נוספות. כמו כן אין שחלופים של קרבוקרטיון, הודות לייצוב רזונטיבי.

קיומה של אצילציית פרידל-קרפטס תלויה ביציבותו של האציל כלוריד המגיב. פורמיל כלוריד למשל לא יציב מספיק, ולפיכך ליצירה של בנזאלדהיד דרך פרידל-קרפטס נדרשת תגובת גטרמן קוך (Gattermann-Koch) שבה הפורמיל כלוריד יסונתז יחד עם פחמן חד-חמצני וחומצה הידרוכלורית (HCl) תחת תנאי לחץ גבוה, המזורזת על ידי אלומיניום כלוריד ו-CuCl.

מנגנון התגובה
[עריכת קוד מקור | עריכה]השלב הראשון מורכב מניתוק יון כלוריד ליצירת קטיון של אציל:

בהמשך יון האציליום מותקף נוקלאופילית על ידי הטבעת הארומטית:

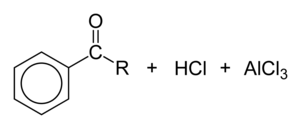
לבסוף אניון כלוריד (או AlCl4-) עושה דה-פרוטונציה לטבעת ליצירת HCl, והזרז AlCl3 נוצר מחדש:
את הקטון בסוף התגובה ניתן לחזר ולהפוך לאלקאן מתאים באמצעות חיזור וולף-קישנר (Wolff–Kishner) או חיזור קלמנסן (Clemmensen). התוצאה הסופית תהיה דומה לאלקילציית פרידל-קרפטס[2].
קישורים חיצוניים
[עריכת קוד מקור | עריכה]הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Jim Clark, FRIEDEL-CRAFTS REACTIONS OF BENZENE AND METHYLBENZENE
- ^ Friedel-Crafts Acylation, organic-chemistry.org
| תגובות כימיות | |||||
|---|---|---|---|---|---|
| מיון תגובות | |||||
| על-פי מנגנון | |||||
| על-פי תרמודינמיקה |
| ||||
| מונחים | |||||
| קינטיקה של תגובות כימיות | תאוריית ההתנגשויות המולקולריות • אנרגיה חופשית • קבוע קצב • משוואת קצב • שלב קובע המהירות • אנרגיית שפעול • מצב מעבר • חומר ביניים • שיווי משקל כימי • טמפרטורה • לחץ • זרז | ||||
| נושאים נוספים | סטריאוכימיה • סטריאוסלקטיביות • סטריאוספציפיות • כיראליות • אפקט סטרי • היברידיזציה • קונפיגורציה מולקולרית • רזוננס כימי • היפרקוניוגציה • מערכת מצומדת • ארומטיות • כלל הופמן • כלל זייצב • כלל מרקובניקוב • כללי וודוורד-הופמן | ||||
| פורטל כימיה | |||||