Метол

| Метол | |
|---|---|
 | |
| Общие | |
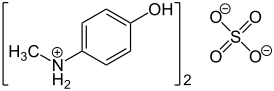
| Систематическое наименование | 4-метиламинофенол сульфат |
| Хим. формула | (C7H10NO)2SO4 |
| Физические свойства | |
| Молярная масса | 344,38 г/моль |
| Термические свойства | |
| Температура | |
| • разложения | 250 °C |
| Классификация | |
| Рег. номер CAS | 55-55-0 |
| PubChem | 5930 и 57508591 |
| Рег. номер EINECS | 200-237-1 |
| SMILES | |
| InChI | |
| ChEBI | 55413 |
| ChemSpider | 5717 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Мето́л (4-метиламинофенол сульфат, параметиламинофенолсульфат, монометилпарааминофенола сернокислая соль) — органическое вещество с формулой (C7H10NO)2SO4. Применяется в чёрно-белой фотографии в качестве проявляющего вещества. В составе проявителей часто сочетается с другими проявляющими веществами, например с гидрохиноном.
Торговые наименования — элон (Kodak, США), монол, метатил, M-143, генол, планетол[1][2].
Физические и химические свойства
[править | править код]Выглядит как порошок из бесцветных или сероватых кристаллов или иголок. Растворим в воде — 5 г на 100 г воды (25 °С), 16,5 г на 100 г воды (100 °C). Плохо растворим в спирте, не растворим в эфире, хлороформе и бензоле. Температура плавления — 250 °C (с разложением)[3][1].
Быстро окисляется в водных растворах, особенно в щелочных. Для замедления скорости окисления в растворы добавляют сульфит натрия[3].
Водный раствор метола даёт ряд цветных реакций[3]. Например:
- фиолетовую окраску с меркуриацетатом[3];
- красную окраску с азотной кислотой[1];
- жёлтую окраску с железосинеродистым калием[1].
Для количественного определения метола применяют иодометрический метод, основанный на окислении метола иодом до 4-хинонмонометилимина, либо применяют метод диазотирования с образованием N-нитрозопроизводного[3].
Обладает проявляющим действием, начиная проявлять в слабокислой среде при pH 6, что позволяет использовать метол в бесщелочных проявителях[3].
Получение
[править | править код]В промышленности получают из 4-оксифенилглицина, растворённого в циклогексаноне путем нагрева до 150 °C, что приводит к отщеплению углекислого газа[3]:
После завершения реакции смесь подкисляют расчётным количеством серной кислоты, получая осадок чистого метола[3].
На заводах Eastman Kodak метол получали из гидрохинона под давлением. Для этого 40 % метиламин смешивали с гидрохиноном и в присутствии бисульфита натрия обрабатывали в автоклаве в течение 4 часов, выдерживая температуру в диапазоне 170—180 °C[4]:
Реакционную массу затем обрабатывали гидроксидом натрия, получая натриевую соль, которую обрабатывали соляной кислотой для получения вещества технической чистоты. Далее, для очистки соединение перекристаллизовывали в щелочном растворе и затем выделяли в виде сернокислой соли[4].
Метол также можно получить метилированием 4-аминофенола. Для этого 4-аминофенол обрабатывают метилсульфатом[англ.], взятом не более чем в одном эквиваленте, так как в противном случае будет в заметном количестве образовываться диметиловое производное. Вместе с метолом в реакции будет образовываться сульфат 4-аминофенола, который требуется удалять путём подкисления раствора уксусной кислотой и последующим осаживанием бензальдегидом, при этом метол остаётся в растворе. Метол выделяют при концентрировании маточного раствора и затем перекристаллизовывают[4].
Применение
[править | править код]Быстрое проявляющее вещество, дает при проявлении мягкое изображение и относительно сильную вуаль. В случае использования метола как единственного проявляющего вещества в растворе изображение будет иметь хорошую проработку теней, но малую плотность в светах. Хорошо проявляет с бурой. Для получения выравнивающих свойств проявители с метолом готовят без щёлочи, используя только сульфит натрия, при этом выравнивающие свойства состава сильно зависят от чистоты сульфита[1].
Быстро теряет проявляющую способность из-за окисления кислородом, особенно в растворах и на свету. Проявители с метолом чувствительны к изменению температуры и концентрации бромида калия. При увеличении в растворе количества бромида калия время обработки сильно увеличивается[1].
Может применяться как единственное проявляющее вещество, либо в смесях с другими, например гидрохиноном[3]. В проявителях с гидрохиноном получается хорошая проработка в тенях и светах[1]. Примером популярного метол-гидрохинонового проявителя может служить Kodak D-76.
Примечания
[править | править код]Литература
[править | править код]- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). — К.: Тэхника, 1988.
- Пучков В. А. Метол : статья // Химическая энциклопедия / Редкол.: Кнунянц И. Л. (отв. ред.) и др.. — М. : Советская энциклопедия, 1964. — Т. 3: Мальтаза—Пиролиз. — С. 203.
- Glafkides P. Photographic chemistry. — London: Fountain Press, 1958. — Т. 1.

![{\displaystyle {\ce {->[-CO_2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9d7ebda9a95c677f7a17d9709b2311c033854e00)



