Тетраэтоксисилан

| Тетраэтоксисилан | |
|---|---|
  | |
| Общие | |
| Систематическое наименование | Тетраэтоксисилан |
| Сокращения | ТЭС, TEOS |
| Традиционные названия | тетраэтилсиликат, тетраэтилортосиликат, этилсиликат, Tetraethyl orthosilicate, Orthosilicic acid tetraethyl ester, Silicon tetraethoxide, Tetraethoxysilane, Tetraethoxysilicon(IV), Tetraethyl silicate |
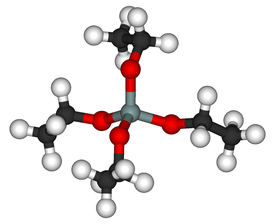
| Хим. формула | (C2H5O)4Si |
| Физические свойства | |
| Состояние | летучая жидкость |
| Молярная масса | 208,33 г/моль |
| Плотность | (20°C) 0,933 г/см³ |
| Энергия ионизации | 9,77 ± 0,01 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | -82 °C |
| • кипения | 169 °C |
| • вспышки | 48 °C |
| Давление пара | 1 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 78-10-4 |
| PubChem | 24848042 |
| Рег. номер EINECS | 201-083-8 |
| SMILES | |
| InChI | |
| RTECS | VV9450000 |
| ChemSpider | 6270 |
| Безопасность | |
| Предельная концентрация | 20мг/м3 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тетраэтоксисила́н (тетраэтилсиликат, этилсиликат, тетраэтилортосиликат) — простой эфир ортокремниевой кислоты и этилового спирта с формулой (C2H5O)4Si. Представляет собой летучую прозрачную бесцветную жидкость с характерным пряно-сладковатым, несколько схожим со спиртовым, запахом.
История и получение
[править | править код]До 60-х годов XX века эфиры-ортосиликаты получали путём прямой этерификации ацетонового раствора ортокремниевой кислоты, полученного разложением жидкого стекла в присутствии ацетона и минеральных кислот с последующим высаливанием 10—12 % ацетонового раствора. Метод характеризовался низкой чистотой получаемого продукта и малым выходом тетраэтоксисилана.
Развитие технологии кремния привело к появлению крупнотоннажного производства тетрахлорида кремния. В конечном итоге к 70-м годам XX века было налажено массовое производство тетраэтокисисилана путём взаимодействия тетрахлорида кремния с этанолом с выходом продукта близким к теоретически возможному.
Свойства
[править | править код]Тетраэтоксисилан хорошо смешивается с органическими растворителями, водой, водными растворами кислот.
В присутствии воды и водных растворов минеральных кислот происходит гидролиз тетраэтоксисилана с отщеплением этанола и последующей конденсацией гидроксипроизводных. В зависимости от условий гидролиза (температура, тип катализатора, наличие органического растворителя) образование геля может происходить с различной скоростью.

В присутствии различных спиртов (и иногда катализатора) тетраэтоксисилан способен переэтерефицироваться, присоединяя молекулы присутствующего спирта с отщеплением этанола. Реакция переэтерификации является обратимой, поэтому для полноты прохождения реакции переэтерификации этанол, как правило, отгоняется самостоятельно или с подходящим азеотропным компонентом.
Применение
[править | править код]Используется в стоматологии, ювелирном деле, технологии керамики как компонент самоотверждающихся составов при снятии слепков.
Является основой для синтеза других эфиров ортокремниевой кислоты путём переэтерификации с параллельной отгонкой выделяющегося этилового спирта.
При синтезе кремнийорганических полимеров применяют в качестве отвердителя.
Примечания
[править | править код]Литература
[править | править код]- Химическая энциклопедия; в 5 т.т.; т.4 Пол-Три; под ред. Зефирова Н. С.; М.:1995 г.-639с.
- ТЭС в каталоге sigma-aldrich
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |
Для улучшения этой статьи желательно:
|