Химический источник тока

Хими́ческий исто́чник то́ка (аббр. ХИТ) — источник тока, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.
История создания
[править | править код]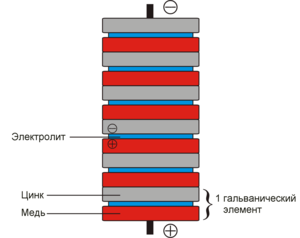
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта в 1800 году. Это был «элемент Вольта» — сосуд с серной кислотой с опущенными в него цинковой и медной пластинками, с проволочными токовыводами. Затем учёный собрал батарею из этих элементов, которая впоследствии была названа «вольтовым столбом». Это изобретение впоследствии использовали другие учёные в своих исследованиях. Так, например, в 1802 году русский академик В. В. Петров сконструировал вольтов столб из 2100 элементов для получения электрической дуги. В 1836 году английский химик Джон Даниель усовершенствовал элемент Вольта, поместив цинковый и медный электроды в раствор серной кислоты. Эта конструкция стала называться «элементом Даниеля».
В 1859 году французский физик Гастон Плантэ изобрёл свинцово-кислотный аккумулятор, поместив скрученную в рулон тонкую свинцовую пластину в серную кислоту. Этот тип элемента и по сей день используется в автомобильных аккумуляторах.
В 1865 году французский химик Ж. Лекланше предложил свой гальванический элемент (элемент Лекланше), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония или другой хлористой соли, в который был помещён агломерат из оксида марганца(IV) MnO2 в качестве деполяризатора с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке Конрад Хьюберт, иммигрант из России, создаёт первый карманный электрический фонарик. А уже в 1896 году компания National Carbon приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia».
Самый старый, поныне работающий гальванический элемент — серебряно-цинковая батарея, изготовленная в Лондоне в 1840 году. Подключенный к двум таким последовательно соединенным батареям звонок работает и по сей день в Кларендонской лаборатории Оксфорда[1].
Принцип действия
[править | править код]Основу химических источников тока составляют два электрода (положительно заряженный катод, содержащий окислитель, и отрицательно заряженный анод, содержащий восстановитель) контактирующие с электролитом. Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода (отрицательного полюса химического источника тока) к положительному. Это соответствует протеканию электрического тока в направлении от положительного полюса к отрицательному, так как направление тока совпадает с направлением движения положительных зарядов в проводнике.
В современных химических источниках тока используются:
- в качестве восстановителя (материал анода) — свинец Pb, кадмий Cd, цинк Zn и другие металлы;
- в качестве окислителя (материал катода) — оксид свинца(IV) PbO2, гидроксооксид никеля NiOOH, оксид марганца(IV) MnO2 и другие;
- в качестве электролита — растворы щелочей, кислот или солей[2].
Классификация
[править | править код]По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций невозможно перезарядить;
- электрические аккумуляторы (вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока (зарядного устройства) можно перезарядить;
- топливные элементы (электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно, пока обеспечивается подача реагентов.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные (например свинцово-кислотный аккумулятор, свинцово-плавиковый элемент), щелочные (например ртутно-цинковый элемент, ртутно-кадмиевый элемент, никель-цинковый аккумулятор, никель-кадмиевый аккумулятор) и солевые (например, марганцево-магниевый элемент, цинк-хлорный аккумулятор).
Некоторые виды химических источников тока
[править | править код]Гальванические элементы
[править | править код]Гальванический элемент — химический источник электрического тока, названный в честь Луиджи Гальвани. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
- См. также Категория: Гальванические элементы.
| Тип | Катод | Электролит | Анод | Напряжение, В |
|---|---|---|---|---|
| Литий-железо-дисульфидный элемент | FeS2 | Li | 1,50—3,50 | |
| Марганцево-цинковый элемент | MnO2 | KOH | Zn | 1,56 |
| Марганцево-оловянный элемент | MnO2 | KOH | Sn | 1,65 |
| Марганцево-магниевый элемент | MnO2 | MgBr2 | Mg | 2,00 |
| Свинцово-цинковый элемент | PbO2 | H2SO4 | Zn | 2,55 |
| Свинцово-кадмиевый элемент | PbO2 | H2SO4 | Cd | 2,42 |
| Свинцово-хлорный элемент | PbO2 | HClO4 | Pb | 1,92 |
| Ртутно-цинковый элемент | HgO | KOH | Zn | 1,36 |
| Ртутно-кадмиевый элемент | HgO2 | KOH | Cd | 1,92 |
| Окисно-ртутно-оловянный элемент | HgO2 | KOH | Sn | 1,30 |
| Хром-цинковый элемент | K2Cr2O7 | H2SO4 | Zn | 1,8—1,9 |
Другие типы:
- Свинцово-плавиковый элемент
- Медно-окисный гальванический элемент
- Висмутисто-магниевый элемент
- Ртутно-висмутисто-индиевый элемент
- Литий-хромсеребряный элемент
- Литий-висмутатный элемент
- Литий-окисномедный элемент
- Литий-йодсвинцовый элемент
- Литий-йодный элемент
- Литий-тионилхлоридный элемент
- Литий-оксидванадиевый элемент
- Литий-фторомедный элемент
- Литий-двуокисносерный элемент
- Диоксисульфатно-ртутный элемент
- Серно-магниевый элемент
- Хлористосвинцово-магниевый элемент
- Хлорсеребряно-магниевый элемент
- Хлористомедно-магниевый элемент
- Иодатно-цинковый элемент
- Магний-перхлоратный элемент
- Магний-м-ДНБ элемент
- Цинк-хлоросеребряный элемент
- Хлор-серебряный элемент
- Бром-серебряный элемент
- Йод-серебряный элемент
- Магний-ванадиевый элемент
- Кальций-хроматный элемент
Электрические аккумуляторы
[править | править код]Электрический аккумулятор — химический источник тока многоразового действия (то есть в отличие от гальванического элемента химические реакции, непосредственно превращаемые в электрическую энергию, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
- См. также Категория: Аккумуляторы.
- Железо-воздушный аккумулятор
- Железо-никелевый аккумулятор
- Лантан-фторидный аккумулятор
- Литий-железо-сульфидный аккумулятор[источник не указан 2073 дня]
- Литий-ионный аккумулятор
- Литий-полимерный аккумулятор
- Литий-фторный аккумулятор
- Литий-хлорный аккумулятор
- Литий-серный аккумулятор
- Марганцево-оловянный элемент
- Натрий-никель-хлоридный аккумулятор
- Натрий-серный аккумулятор
- Никель-кадмиевый аккумулятор
- Никель-металл-гидридный аккумулятор
- Никель-цинковый аккумулятор
- Свинцово-водородный аккумулятор
- Свинцово-кислотный аккумулятор
- Серебряно-кадмиевый аккумулятор
- Серебряно-цинковый аккумулятор
- Цинк-бромный аккумулятор
- Цинк-воздушный аккумулятор
- Цинк-хлорный аккумулятор
Топливные элементы
[править | править код]Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
- См. также Категория: Топливные элементы.
Определение полюсов
[править | править код]Чтобы определить, который полюс источника постоянного напряжения является положительным, а какой — отрицательным, используются специальные «полюсоискатели», действие которых основано на явлении электролиза. Полюсоискатель представляет собой стеклянную ампулу, заполненную раствором поваренной соли с добавкой фенолфталеина. В ампулу снаружи введены электроды. При подключении к электродам источника напряжения начинается электролиз: на отрицательном полюсе идёт выделение водорода и образуется щелочная среда. Из-за наличия щёлочи фенолфталеин меняет свою окраску — краснеет, по красной окраске у электрода и судят о том, что он соединён с отрицательным полюсом источника напряжения[3].
Примечания
[править | править код]- ↑ Exhibit 1 — The Clarendon Dry Pile". Oxford Physics Teaching, History Archive. Retrieved 18 January 2008
- ↑ В демонстрационных экспериментах зачастую используют мякоть плодов апельсина, яблоки и пр.
- ↑ Элементарный учебник физики / Под ред. Г. С. Ландсберга. — 13-е изд.. — М.: ФИЗМАТЛИТ, 2003. — Т. 2. Электричество и магнетизм. — С. 151,152,465.
Литература
[править | править код]- Дасоян М. А. Химические источники тока. — 2-е изд. — Л., 1969.
- Романов В. В., Хашев Ю. М. Химические источники тока. — М., 1968.
- Орлов В. А. Малогабаритные источники тока. — 2-е изд. — М., 1970.
- Вайнел Д. В. Аккумуляторные батареи. — пер. с англ., 4-е изд. — М. — Л., 1960.
- The Primary Battery / ed. G. W. Heise, N. C. Cahoon. — N. Y. — L., 1971. — Т. v. 1.
Ссылки
[править | править код]- Химические источники тока — статья из Большой советской энциклопедии.
- О химических источниках тока
- Аккумуляторные батареи различных электрохимических систем
- ГОСТ Р МЭК 60050-482-2011. Источники тока химические. Термины и определения.