Isocyanate
 Van Wikipedia, de gratis encyclopedie
Van Wikipedia, de gratis encyclopedie

Isocyanate sind die Ester der unbeständigen Isocyansäure. Die Salze der Isocyansäure sind identisch mit den Salzen der Cyansäure und werden deshalb als Cyanate bezeichnet.
Herstellung von Isocyanaten
[Bearbeiten | Quelltext bearbeiten]Isocyanate lassen sich durch die Umsetzung der entsprechenden Amine mit Phosgen als Reaktant herstellen. Die Synthese erfolgt in zwei Schritten über das als Zwischenprodukt auftretende Carbamoylchlorid. In jedem Teilschritt wird ein Chlorwasserstoff-Molekül abgespalten:
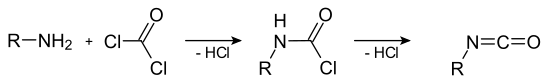
Alternative Synthesewege sind beispielsweise die katalytische Carbonylierung von Nitro-Verbindungen bzw. Aminen oder die Umsetzung primärer Amine mit Di-tert-butyldicarbonat (Diboc) in Anwesenheit von 4-(Dimethylamino)pyridin (DMAP)[1].
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Isocyanate sind chemisch hochreaktive Verbindungen, die das Strukturelement R–N=C=O aufweisen. Die bedeutendsten Reaktionen der Isocyanatgruppe sind Additionsreaktionen. So reagieren sie mit Alkoholen zu Urethanen, mit Aminen zu Harnstoffderivaten und mit Wasser zu Carbamidsäuren; letztere sind jedoch chemisch instabil und zerfallen direkt unter Abgabe von Kohlenstoffdioxid zu den Aminen. Mit Carbonsäuren reagieren sie zu Amiden, die mit weiterem Isocyanat Acylharnstoffe bilden.
Urethanbildung:
Harnstoffderivatbildung:
Reaktion mit Wasser:
Reaktion mit Carbonsäuren (Amid- bzw. Acylharnstoffbildung):
Isocyanate können in einer Gleichgewichtsreaktion zu Uretdionen dimerisieren. Die Dimerisierung kann durch basische Katalysatoren wie Pyridin oder tertiäre Phosphane beschleunigt werden; aromatische Isocyanate dimerisieren jedoch auch ohne Katalysator.[2]

Bei höheren Temperaturen ist die Lage des Gleichgewichts zu den thermisch stabileren Isocyanaten hin verschoben.
Auch eine Trimerisierung zu den sogenannten Isocyanuraten (1,3,5-Triazin-2,4,6-trionen) ist möglich; als Katalysatoren hierfür sind z. B. Natriumformiat, Kaliumacetat, Phosphane oder tertiäre Amine geeignet. Aus Diisocyanaten hergestellte Isocyanurate werden als Reaktionskomponente mit besonders niedrigem Dampfdruck für Polyurethansysteme eingesetzt.[2] Ebenso kann die Trimerisierung aber auch zur Herstellung von Polyisocyanuraten genutzt werden.
Anwendung und Nutzung
[Bearbeiten | Quelltext bearbeiten]Bei der Anwendung der Isocyanate muss unterschieden werden zwischen den sehr flüchtigen Monoisocyanaten und den deutlich weniger flüchtigen Di- und Polyisocyanaten.
Methylisocyanat (CH3–N=C=O) ist der einfachste Ester der Isocyansäure. Es ist eine sehr reaktive Substanz, die z. B. bei der Herstellung von Pestiziden verwendet wird.
Industrielle Nutzung
[Bearbeiten | Quelltext bearbeiten]Diisocyanate und blockierte Isocyanate dienen hauptsächlich der Synthese der Polyurethane.
Die wichtigsten Diisocyanate sind:
- Toluol-2,4-diisocyanat (TDI)
- Diphenylmethandiisocyanat bzw. Methylendiphenyldiisocyanat (MDI)
- Hexamethylendiisocyanat (HDI, HMDI)
- Polymeres Diphenylmethandiisocyanat (PMDI)
- meta-Tetramethylxylylendiisocyanat (TMXDI)
- Isophorondiisocyanat (IPDI)
- 4,4’-Diisocyanatodicyclohexylmethan (H12MDI)
Die beiden letztgenannten aliphatischen Diisocyanate und ihre Derivate sowie das Hexamethylendiisocyanat finden hauptsächlich in hochwertigen Polyurethan-Lacksystemen Verwendung.
Isocyanatharze
[Bearbeiten | Quelltext bearbeiten]Werden Verbindungen mit zwei Isocyanat-Gruppen (Diisocyanate) mit zweiwertigen Alkoholen (Diolen) zur Reaktion gebracht, so laufen Polyadditions-Reaktionen ab und es entstehen als Reaktionsharze die technisch vielfältig genutzten Polyurethane.
Ist gleichzeitig auch noch Wasser (z. B. Luftfeuchtigkeit) vorhanden, läuft auch die Reaktion über die instabilen Carbamidsäuren ab, die unter Kohlenstoffdioxid-Abspaltung zerfallen. Das hierbei entstehende Gas ist für die Schaumbildung bei Polyurethanschäumen verantwortlich. Das gleichzeitig entstehende Amin wiederum kann, wie oben dargestellt, mit einem weiteren Isocyanat zu einer Harnstoffverbindung reagieren. Bei der Härtung von Polyisocyanaten mit Wasser werden also Polyharnstoffe gebildet.
So lassen sich auch einkomponentige Produkte (Lacke, Klebstoffe, Schäume) formulieren, die das zur Härtung erforderliche Wasser als Wasserdampf aus der Umgebungsluft beziehen. Dünne Schichten härten ohne Aufschäumen aus, soweit das Basismaterial eine genügende Durchlässigkeit für Kohlendioxid besitzt. Auf Grund der Reaktivität der Isocyanate haften die Polyurethanbeschichtungen an den meisten Materialien sehr gut. Deshalb werden polymere Isocyanate auch als Haftvermittler oder Primer für andere Beschichtungen verwendet.
Charakterisierung und Einteilung
[Bearbeiten | Quelltext bearbeiten]Es gibt unterschiedliche Möglichkeiten (Poly-)Isocyanate in Klassen einzuteilen oder zu charakterisieren.[3] Zunächst kann eine Charakterisierung über die Stoffliche Zusammensetzung vorgenommen werden. So unterteilt der Anwendung meist in aromatische oder aliphatische Isocyanate. Aus diesem chemischen Aufbau resultieren wichtige Eigenschaften wie etwa Reaktivität und Wetterbeständigkeit der erhaltenen Systeme und Mischungen.
Da die Isocyanatgruppen der (Poly-)Isocyanate meist stöchiometrisch, sprich molar 1:1, mit Reaktionspartnern umgesetzt werden, muss die Menge an Isocyanatgruppen beschrieben werden. In der Regel wird hier der sogenannte Isocyanatgehalt angegeben, welcher sich auf das Isocyanat als Reinstoffe oder auch auf die Anlösung beziehen kann. Der Isocyanatgehalt beschreibt die prozentuale Gewichtsmenge an Isocyanatgruppen im Gemisch:
Da der Isocyanatgehalt nur eine wenig charakterisierende Größe ist, kann alternativ das sogenannte Äquivalentgewicht angegeben werden. Das Isocyanat-Äquivalentgewicht (NCO-Äquivalentgewicht) beschreibt die Menge an Stoff/Mischung, welche exakt ein mol Isocyanatgruppen enthält. Relevant hierfür ist die Kenntnis über die Masse einer Isocyanatgruppe von 42 g pro mol.
Soll nun das Mischungsverhältnis eines (Poly-)Isocyanates mit z. B. einem Polyester-Polyol berechnet werden, so ist auch dessen Äquivalentgewicht nötig. Dieses OH-Äquivalentgewicht beschreibt diejenige Menge Stoff, welche ein mol Hydroxygruppen enthält.
Medizinische Bedeutung
[Bearbeiten | Quelltext bearbeiten]Isocyanate schädigen, durch eine Reaktion mit NH2- und OH-Gruppen, die Zellmembranen menschlicher Zellen. Bei Aufnahme durch Inhalation Isocyanat-haltiger Dämpfe kommt es zu Reizerscheinungen an Haut und Schleimhaut. Im Auge können Hornhautschädigungen verursacht werden. Insbesondere HMDI kann auf der Haut eine Nesselsucht, ein Kontaktekzem oder eine toxische Dermatitis auslösen.
Isocyanate, insbesondere MDI und TDI, können eine allergische Reaktion des Typ I hervorrufen. Das sich dadurch entwickelnde Isocyanat-Asthma präsentiert sich ähnlich wie das klassische allergische Asthma, scheint jedoch etwas anderen molekularen Mechanismen zu unterliegen. Spezifische Antikörper werden nur selten nachgewiesen. Eine Diagnose erfolgt häufig über einen Provokationstest. Weniger häufig kommt es zu einer Schädigung des Alveolarepithels in den Lungen mit dem klinischen Bild einer Alveolitis (Isocyanat-Alveolitis).
Atemwegserkrankungen, die durch Isocyanate ausgelöst werden, können als Berufskrankheit (BK1315) anerkannt werden. Arbeitnehmer, die regelmäßig Isocyanaten ausgesetzt sind, müssen an arbeitsmedizinischen Vorsorgeuntersuchungen teilnehmen.[4][5] Um inhalative Exposition zu vermeiden, werden die niedermolekularen Vertreter in den meisten Anwendungen durch schwerflüchtige Derivate ersetzt.
Die Technische Regel für Gefahrstoffe (TRGS) 430 beschreibt die Gefährdungsbeurteilung und die daraus abgeleiteten Schutzmaßnahmen für Arbeitsplätze, an denen Isocyanate vorkommen, meist handelt es sich um Tätigkeiten zur Herstellung und Anwendung von Polyurethanen.[6]
Die messtechnische Überwachung von Isocyanaten in der Luft am Arbeitsplatz stellt wegen ihrer hohen Reaktivität große Anforderungen an Probenahme und Analytik. Die TRGS 900 nennt nur Arbeitsplatzgrenzwerte (AGW) für monomere Isocyanate. Eine stoffliche Identifizierung der vielfältigen Polyisocyanate (mittels Flüssigchromatographie) ist nicht vollständig möglich. Es ist aber möglich, über die Bestimmung der freien NCO-Gruppen auf den Gehalt an Isocyanaten rückzuschließen. Diese Vorgehensweise ist in der TRGS 430 beschrieben. Dort ist ein Expositionsleitwert (ELW) als Beurteilungsmaßstab für die Summe an reaktionsfähigen NCO-Gruppen von 0,018 mg NCO/m³ festgelegt worden. Ist der ELW eingehalten, sind keine weiteren stoffspezifischen Analysen erforderlich; alle einzelnen Arbeitsgrenzwerte für monomere Diisocyanate werden bei Unterschreitung des ELW auch unterschritten. Bei einer Überschreitung des ELW sind detailliertere Analysen nötig.[7]
Durch wiederholten Hautkontakt können lokale toxische und allergische Reaktionen und überdies eine stoffspezifische bronchiale Überempfindlichkeit hervorgerufen werden. Sensibilisierte Personen können schon bei geringsten Isocyanatkonzentrationen (auch unterhalb der Bestimmungsgrenze) von erheblichen gesundheitlichen Beeinträchtigungen betroffen sein und z. B. asthmatische Beschwerden entwickeln. Dies ist bei der Gefährdungsbeurteilung zu berücksichtigen.[8][6] Aufgrund der sensibilisierenden Wirkung sind bei Tätigkeiten mit Isocyanaten Chemikalienschutzhandschuhe der Kat. III einzusetzen, die gegenüber Isocyanaten eine ausreichende Barriere bilden.[9]
Toxizität
[Bearbeiten | Quelltext bearbeiten]Isocyansäure, Methylisocyanat und andere Isocyanate sind sehr giftig.
Am 3. Dezember 1984 entwichen aus einem defekten Tank einer Pestizidfabrik des amerikanischen Chemiekonzerns Union Carbide Corporation in der Nähe der Stadt Bhopal (Indien) rund 40 Tonnen Methylisocyanat („Bhopalunglück“). Die Gaswolke tötete mehr als 2800 Menschen und verursachte bei mehreren Hunderttausend weiteren Personen schwere Verletzungen wie Augen- und Schleimhautschäden.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Hans-Joachim Knölker, Tobias Braxmeier, Georg Schlechtingen: A Novel Method for the Synthesis of Isocyanates Under Mild Conditions. In: Angewandte Chemie International Edition in English. 34, 1995, S. 2497–2500, doi:10.1002/anie.199524971.
- ↑ a b Hans Kittel: Lehrbuch der Lacke und Beschichtungen. In: Walter Krauß (Hrsg.): Band 2: Bindemittel für lösemittelhaltige und lösemittelfreie System. 2. Auflage. Hirzel, Stuttgart 1998, ISBN 3-7776-0886-6.
- ↑ Ulrich Poth: Synthetische Bindemittel für Beschichtungssysteme. Vincentz Network, Hannover 2016, ISBN 978-3-86630-611-0.
- ↑ Jürgen Fritze: Die ärztliche Begutachtung: Rechtsfragen, Funktionsprüfungen, Beurteilungen. 7. Auflage. Steinkopff, Darmstadt 2008, ISBN 3-7985-1563-8.
- ↑ Claus Kroegel, Neil C. Barns: Asthma bronchiale: Pathogenetische Grundlagen, Diagnostik, Therapie. 2. Auflage, Georg Thieme, Stuttgart/New York 2001, ISBN 3-13-104732-1.
- ↑ a b TRGS 430 Isocyanate – Gefährdungsbeurteilung und Schutzmaßnahmen. In: baua.de. 6. Dezember 2022, abgerufen am 6. Dezember 2022.
- ↑ Messung von Gefahrstoffen – IFA-Arbeitsmappe: Isocyanate – Monomere Diisocyanate, Totalkonzentration reaktiver Isocyanatgruppen TRIG und Polyisocyanatgehalt (Messung von Gefahrstoffen – IFA-Arbeitsmappe)
- ↑ Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA): Empfehlungen Gefährdungsermittlung der Unfallversicherungsträger (EGU). Abgerufen am 28. September 2021.
- ↑ Deutsche Gesetzliche Unfallversicherung e. V. (DGUV): Häufig gestellte Fragen und Antworten zum Sachgebiet Schutzkleidung / Schutzhandschuhe. Abgerufen am 28. September 2021.


![{\displaystyle \mathrm {R{-}NCO+H_{2}O\longrightarrow [R{-}NHCOOH]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/acad08599ab8245d881cb05ff8e9108f258fd5f4)
![{\displaystyle \mathrm {[R{-}NHCOOH]\longrightarrow R{-}NH_{2}+CO_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7bd4910a435e2ccc5efac7cfd8634383a2e44516)


![{\displaystyle {\text{Isocyanatgehalt}}={\frac {({\text{Masse}}[{\text{Isocyanatgruppen}}])}{\text{Gesamtmasse}}}{\text{ in }}[{\text{Prozent}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/afa8ba3b4023c9a694ffcc38aa1cf900eaf580cf)
![{\displaystyle NCO-{\text{Äquivalentgewicht}}={\frac {1}{\left({\frac {{\text{Isocyanatgehalt}}[\%]}{100\cdot 42\mathrm {\frac {g}{mol}} }}\right)}}{\text{ in }}[\mathrm {g/mol(NCO)} ]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e8ea593a4c9b63b0888483c465edf9734e1de190)
