Acide paracoumarique

| Acide paracoumarique | |
 | |
| Identification | |
|---|---|
| Nom UICPA | acide 3-(4-hydroxyphényl)-prop-2-ènoïque |
| Synonymes | acide para-4-hydroxycinnamique |
| No CAS | |
| No ECHA | 100.116.210 |
| No CE | 610-511-6 |
| PubChem | 637542 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C9H8O3 [Isomères] |
| Masse molaire[2] | 164,158 ± 0,008 7 g/mol C 65,85 %, H 4,91 %, O 29,24 %, |
| pKa | 4,64[1] |
| Propriétés physiques | |
| T° fusion | 214 °C[1] |
| Solubilité | peu soluble dans l'eau, soluble dans l'éthanol et l'éther diéthylique |
| Précautions | |
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
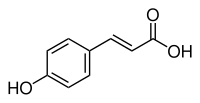
L'acide paracoumarique ou acide parahydroxycinnamique est un composé phytochimique dérivé de l'acide cinnamique de formule brute C9H8O3. C'est l'isomère para de l'acide coumarique et le plus abondant des trois isomères dans la nature. Il est ainsi, par abus de langage, souvent appelé simplement acide coumarique.
Occurrence naturelle
[modifier | modifier le code]L'acide paracoumarique se trouve dans une grande variété de plantes comestibles, comme les cacahuètes, les tomates, les carottes et l'ail.
Synthèse
[modifier | modifier le code]L'acide paracoumarique est biosynthétisé à partir de l'acide cinnamique par l'action de l'enzyme cinnamate 4-hydroxylase (C4H), selon la voie des phénylpropanoïdes.
Il peut aussi être obtenu à partir de la tyrosine par l'action de l'enzyme tyrosine ammonialyase (TAL).
Précurseur
[modifier | modifier le code]Élément-clé de la voie des phénylpropanoïdes, il est le précurseur de nombreux composés des différentes familles de phénylpropanoïdes :
- deux fois réduit, il donne l'alcool paracoumarique qui, avec l'alcool sinapylique et l'alcool coniférylique, est l'un des principaux constituants de la lignocellulose ;
- hydroxylé, il donne l'acide caféique, qui pourra à son tour être transformé en acide férulique (qui pourra être transformé par double réduction en alcool coniférylique), et enfin en acide sinapique (qui pourra être transformé par double réduction en alcool sinapylique) ;
- par réaction avec la coenzyme A (CoA), il forme un thioester, la 4-coumaroyl-CoA. Ce dernier peut par la suite, par action de la chalcone synthase (CHS), être transformé en chalcone, précurseurs des flavonoïdes, ou transformé par cyclisation interne en stilbénoïde ;
- par cyclisation interne, il peut être transformé en coumarine.
Applications
[modifier | modifier le code]L'acide paracoumarique a des propriétés antioxydantes et pourrait avoir un rôle dans la réduction de risque de cancer de l'estomac[3] en réduisant la formation des nitrosamines, cancérogènes[4].
Notes et références
[modifier | modifier le code]- (en) « Acide paracoumarique », sur ChemIDplus, consulté le 5 mars 2009
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Ferguson LR, Shuo-tun Z, Harris PJ, « Antioxidant and antigenotoxic effects of plant cell wall hydroxycinnamic acids in cultured HT-29 », Molecular Nutrition & Food Research, vol. 49, no 6, , p. 585–693 (DOI 10.1002/mnfr.200500014)
- (en) Kikugawa K, Hakamada T, Hasunuma M, Kurechi T, « Reaction of p-hydroxycinnamic acid derivatives with nitrite and its elevance to nitrosamine formation », Journal of Agricultural and Food Chemistry, vol. 1, no 4, , p. 780–785 (DOI 10.1021/jf00118a025, lire en ligne)


