Benzimidazole

| Benzimidazole | |
 | |
| Identification | |
|---|---|
| Nom UICPA | 1H-benzimidazole |
| Synonymes | 1,3-benzodiazole |
| No CAS | |
| No ECHA | 100.000.075 |
| No CE | 200-081-4 |
| No RTECS | DD5425000 |
| PubChem | 5798 |
| SMILES | |
| InChI | |
| Apparence | solide cristallin marron clair[1] |
| Propriétés chimiques | |
| Formule | C7H6N2 |
| Masse molaire[3] | 118,135 9 ± 0,006 4 g/mol C 71,17 %, H 5,12 %, N 23,71 %, |
| pKa | 5,3 à 25 °C[2] |
| Propriétés physiques | |
| T° fusion | 169 à 171 °C[1],[2] |
| T° ébullition | 360 °C[1] |
| Solubilité | 2 010 mg·l-1 (eau, 20 °C)[2] |
| Pression de vapeur saturante | 7,64×10-5 mmHg (25 °C)[2] |
| Précautions | |
| SGH[1] | |
| NFPA 704[1] | |
| Écotoxicologie | |
| DL50 | 445 mg·kg-1 (souris, intrapéritonéal)[4] 280 mg·kg-1 (souris, IV)[5] 2 910 mg·kg-1 (souris, oral)[6] 385 mg·kg-1 (rat, intrapéritonéal)[7] |
| LogP | 1,32[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
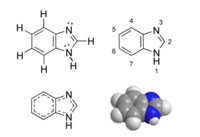
Le benzimidazole est un composé hétérocyclique aromatique résultant de la fusion d'un cycle de benzène et d'un cycle imidazole. Les composés partageant cette structure sont appelés benzimidazoles, l'un des plus importants d'entre eux étant sans doute le N-ribosyldiméthylbenzimidazole, qui sert de ligand pour le cobalt dans la vitamine B12.
Synthèse
[modifier | modifier le code]Le benzimidazole est vendu dans le commerce. Il est généralement préparé par condensation d'orthophénylènediamine avec l'acide formique, HCOOH[8] ou avec l'équivalent orthoformiate de triméthyle HC(OCH3)3 :
- C6H4(NH2)2 + HC(OCH3)3 → C6H4N(NH)CH + 3 CH3OH.
En changeant l'acide carboxylique utilisé, il est généralement possible d'obtenir des benzimidazoles 2-substitués par cette méthode[8].
Utilisation
[modifier | modifier le code]Les benzimidazoles, qui peuvent être vus comme une extension du modèle bien connu de l'imidazole, ont été utilisés comme squelette carboné pour la préparation de carbènes N-hétérocycliques (NHC). Ces composés sont utilisés comme ligands pour les complexes de métaux de transition. Ils sont souvent préparés par déprotonation par une base en position 2 d'un sel de benzimidazolium N,N'-disubstituté[9],[10].
Pesticide : le benzimidazole a également des propriétés fongicides utilisées à partir des années 1970[11]. Il agit en se liant aux microtubules fongiques et en stoppant la croissance des hyphes. Il se lie aussi aux microtubules du fuseau et bloque leur division nucléaire.
Antiparasitaire : le Benzimidazole est aussi utilisé contre l'échinocoque responsable de l'échinococcose alvéolaire (avant cela seule la chirurgie pouvait être utilisée). Il a longtemps et communément été présenté comme « médicament parasitostatique », c'est-à-dire bloquant l'avancée de la maladie plutôt que « parasitocide » (c'est-à-dire permettant à lui seul une guérison complète et définitive) ce pourquoi il était systématiquement prescrit en traitement à vie (chimiothérapie de long terme). Une étude récente (2014) mise en œuvre par le groupe suisse d'étude de l'échinococcose (SESG pour Swiss Echinococcosis Study Group) ayant porté sur 34 patients non opérables et traités par ce médicament a cependant montré que ce médicament semble avoir bien tué le parasite chez 1/3 de ces patients (11 patients sur 34 exactement). L'étude n'a pas précisé pourquoi certains patients ont guéri et d'autres non[12]. Selon cette étude, si le parasite ne réapparait pas dans les 24 mois suivant l'arrêt de la chimiothérapie, il peut alors être considéré comme éradiqué.
Exemples de benzimidazoles : albendazole, flubendazole, astémizole, un antihistaminique qui a une activité anti-prion démontrée[13].
Notes et références
[modifier | modifier le code]- Fiche Sigma-Aldrich du composé Benzimidazole, consultée le 24 juin 2012.
- (en) « Benzimidazole », sur ChemIDplus
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Pharmaceutical Chemistry Journal, vol. 14, p. 130, 1980.
- Principles of Medicinal Chemistry, Foye, W.O., et al., eds., Philadelphia, Lea & Febiger, 1974, vol. -, p. 246, 1974.
- Journal of Pharmacology and Experimental Therapeutics, vol. 105, p. 486, 1952. PMID
- Archives Internationales de Pharmacodynamie et de Thérapie, vol. 95, p. 123, 1953.
- E. C. Wagner et W. H. Millett, Benzimidazole, Org. Synth., coll. « vol. 19 », , p. 12.
- (en) R. Jackstell, A. Frisch, M. Beller, D. Rottger, M. Malaun et B. Bildstein, « Efficient telomerization of 1,3-butadiene with alcohols in the presence of in situ generated palladium(0)carbene complexes », Journal of Molecular Catalysis A: Chemical, vol. 185, nos 1–2, , p. 105–112 (DOI 10.1016/S1381-1169(02)00068-7)
- (en) H. V. Huynh, J. H. H. Ho, T. C. Neo et L. L. Koh, « Solvent-controlled selective synthesis of a trans-configured benzimidazoline-2-ylidene palladium(II) complex and investigations of its Heck-type catalytic activity », Journal of Organometallic Chemistry, vol. 690, no 16, , p. 3 854–3 860 (DOI 10.1016/j.jorganchem.2005.04.053)
- Laville, E. (1970). Perspectives nouvelles offertes par les fongicides dérives du Benzimidazole dans le traitement des agrumes. Fruits, 25(5), 337-339. URL=https://revues.cirad.fr/index.php/fruits/article/download/33705/32970
- Ammann Rudolf W & al. (2014) May combined PET and serological follow-up predict a parasitocidal effect of chemotherapy in a subset of patients with non-resectable alveolar echinococcosis ?, D.A. Vuitton et al. : Parasite 2014, 21,28
- (en) http://www.scripps.edu/news/press/2013/20130403lasmezas.html
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Benzimidazole » (voir la liste des auteurs).
Voir aussi
[modifier | modifier le code]- Benzimidazoline
- Polybenzimidazole
- Indole, un analogue où CH remplace l'azote en position 3.
- Purine, un analogue avec deux atomes additionnels d'azote dans le cycle à six (cycle de pyrimidine au lieu d'un cycle de benzène).
- Noyau aromatique simple
