Trichlorofluorométhane

| Trichlorofluorométhane | ||
 | ||
 | ||
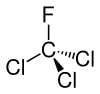
| Représentation du trichlorofluorométhane. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Trichlorofluorométhane | |
| Synonymes | Trichloromonofluorométhane | |
| No CAS | ||
| No ECHA | 100.000.812 | |
| No CE | 200-892-3 | |
| No RTECS | PB6125000 | |
| PubChem | ||
| ChEBI | 48236 | |
| SMILES | ||
| InChI | ||
| Apparence | gaz incolore ou liquide très volatil, d'odeur caractéristique[1]. | |
| Propriétés chimiques | ||
| Formule | CCl3F [Isomères] | |
| Masse molaire[3] | 137,368 ± 0,007 g/mol C 8,74 %, Cl 77,43 %, F 13,83 %, | |
| Moment dipolaire | 0,46 ± 0,02 D[2] | |
| Propriétés physiques | ||
| T° fusion | −111 °C[1] | |
| T° ébullition | 24 °C[1] | |
| Solubilité | dans l'eau à 20 °C : 1 g l−1[1] | |
| Paramètre de solubilité δ | 15,5 MPa1/2 (25 °C)[4] | |
| Masse volumique | 1,49 g cm−3[1] | |
| Pression de vapeur saturante | à 20 °C : 89,0 kPa[1], 39,17 psi (55 °C)[réf. souhaitée] | |
| Point critique | 44,1 bar, 198,05 °C[5] | |
| Thermochimie | ||
| Cp | ||
| Propriétés électroniques | ||
| 1re énergie d'ionisation | 11,77 ± 0,02 eV (gaz)[7] | |
| Précautions | ||
| SIMDUT[8] | ||
Produit non contrôlé | ||
| Directive 67/548/EEC | ||
| Écotoxicologie | ||
| LogP | 2,53[1] | |
| Seuil de l’odorat | bas : 200 000 ppm[9] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier | ||
Le trichlorofluorométhane CCl3F, également appelé fréon 11 (nom de marque), CFC-11, ou R-11 selon la liste de réfrigérants, est un chlorofluorocarbure (CFC). Ce liquide incolore, presque inodore, très volatil, qui bout à température ambiante, a été le premier réfrigérant employé couramment en raison de son bas point d'ébullition. Il s'emploie dans les systèmes à basse pression de fonctionnement contrairement aux systèmes fonctionnant au R-12 ou R-22 qui nécessitent une haute pression de fonctionnement. C'est un gaz à effet de serre, et en tant que destructeur de la couche d'ozone, il est interdit par le Protocole de Montréal mais sa production industrielle semble avoir illégalement repris en Chine[10].
Applications industrielles (avant interdiction)
[modifier | modifier le code]- Réfrigérant, dont pour les systèmes de climatisation d'air industriel.
- Fluide de rinçage de circuits frigorifiques.
- Fluide caloporteur.
- Propulseur pour aérosols en pharmaceutique, cosmétique et thérapeutique (souvent en association avec le dichlorodifluorométhane).
- Agent gonflant pour les mousses de polymères.
- Solvant pour le dégraissage (notamment des circuits imprimés) et pour le nettoyage à sec (textiles).
Propriétés
[modifier | modifier le code]Ce fluide de la famille des chlorofluorocarbures est :
- incolore ;
- ininflammable ;
- d'odeur légèrement éthérée ;
- point critique : 198 °C à 4 410 kPa.
- Potentiel de déplétion ozonique (ODP) : 1,0 (le trichlorofluorométhane sert de référence à l'échelle).
- Potentiel de réchauffement global (GWP) : 4 600.
Interdiction et production illégale
[modifier | modifier le code]Le trichlorofluorométhane est interdit par le Protocole de Montréal en raison de son effet néfaste sur la couche d'ozone[11].
Grâce au Protocole de Montréal[12], sa concentration dans l'atmosphère a décliné régulièrement dès le milieu des années 1990[11], mais moindrement depuis 2012, probablement à la suite d'une reprise illégale de sa production industrielle dans l'est de la Chine[11].

Biodégradabilité ?
[modifier | modifier le code]Quelques tests faits de 2003 à 2005 ont montré une certaine biodégradation du CFC-11, mais uniquement en conditions anaérobies (dont dans les eaux marines anoxiques selon Bullister et Lee, 1995), mais ce produit est très volatil, il tend donc à se répandre dans l'air, tant qu'il n'est pas prisonnier d'un contenant ou des pores d'une mousse isolante qui en sont un réservoir de polluant pour le futur (des preuves existent d'émanations de CFC-11 à partir de certaines décharges)[13].
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Lin, Y. et al. (2019), Observations of High Levels of Ozone- Depleting CFC-11 at a Remote Mountain-Top Site in Southern China, Environ. Sci. Technol. Lett., 6, 3, 114 -118, DOI 10.1021/acs.estlett.9b00022.
- Lunt, M.F. et al. (2018), Continued emissions of the ozone-depleting substance carbon tetrachloride from eastern Asia, Geophys. Res. Lett., 45, 11,423–11,430, DOI 10.1029/2018GL079500.
- Manning, A.J. et al. (2003), Estimating European emis- sions of ozone-depleting and greenhouse gases using observations and a modeling back-attribution technique, J. Geophys. Res., 108 (D14), 4405, DOI 10.1029/2002JD002312.
- Montzka, S.A. et al. (2018), An unexpected and persistent increase in global emissions of ozone- depleting CFC-11, Nature, 557, 413–417, DOI 10.1038/s41586-018-0106-2.
- Park, S. et al. (2018), Toward resolving the budget discrep- ancy of ozone-depleting carbon tetrachloride (CCl4): an analysis of top-down emissions from China, Atmos. Chem. Phys., 18, 11729-11738, DOI 10.5194/acp-18-11729-2018.
- Rigby, M. et al. (2019), Increase in CFC-11 emissions from eastern China based on atmospheric observations, Nature, 569, 546–550, DOI 10.1038/s41586-019-1193-4.
- Say, D. et al. (2019), Emissions of CFCs, HCFCs and HFCs from India, Atmos. Chem. Phys. Discuss., DOI 10.5194/acp- 2018-1146, in review.
Notes et références
[modifier | modifier le code]- TRICHLOROFLUOROMETHANE, Fiches internationales de sécurité chimique
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 9-50.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294.
- « Properties of Various Gases », sur flexwareinc.com (consulté le ).
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, 2 et 3, Huston, Texas, Gulf Pub., , 396 p. (ISBN 0-88415-857-8, 0-88415-858-6 et 0-88415-859-4).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- « Fluorotrichlorométhane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- « Fluorotrichloromethane », sur hazmap.nlm.nih.gov (consulté le ).
- (en) N.R.P. Harris, S.A. Montzka, P.A. Newman et al., « Report on the International Symposium on the Unexpected Increase in Emissions of Ozone-Depleting CFC-11 », SPARC newsletter, vol. 53, (lire en ligne).
- (en) M. Rigby, S. Park et al., « Increase in CFC-11 emissions from eastern China based on atmospheric observations », Nature, vol. 569, (lire en ligne).
- (en) Lei Hu et al., « Considerable contribution of the Montreal Protocol to declining greenhouse gas emissions from the United States », Geophysical Research Letters, vol. 44, , p. 8075-8083 (DOI 10.1002/2017GL074388, lire en ligne).
- (en) Paul Ashford, Koichi Mizuno et Miguel Quintero, Report of the Task Force on Foam End-of-Life Issues, (ISBN 92-807-2637-4, lire en ligne).




