Chloroéthane

| Chloroéthane | |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Chloroéthane | ||
| Synonymes | Chlorure d'éthyle | ||
| No CAS | |||
| No ECHA | 100.000.755 | ||
| No CE | 200-830-5 | ||
| Apparence | gaz comprimé liquefié incolore, d'odeur caractéristique[1]. | ||
| Propriétés chimiques | |||
| Formule | C2H5Cl [Isomères] | ||
| Masse molaire[2] | 64,514 ± 0,004 g/mol C 37,23 %, H 7,81 %, Cl 54,95 %, | ||
| Moment dipolaire | 2,06 D | ||
| Propriétés physiques | |||
| T° fusion | −138 °C[1] | ||
| T° ébullition | 12,5 °C[1] | ||
| Solubilité | dans l'eau à 20 °C : 5,74 g·l-1[1] | ||
| Paramètre de solubilité δ | 18,8 MPa1/2 (25 °C)[3]; 8,3 cal1/2·cm-3/2 (25 °C)[4] | ||
| Masse volumique | 0,918 g·cm-3[1] | ||
| T° d'auto-inflammation | 519 °C[1] | ||
| Point d’éclair | −50 °C (coupelle fermée)[1] | ||
| Limites d’explosivité dans l’air | 3,6–14,8 %vol[1] | ||
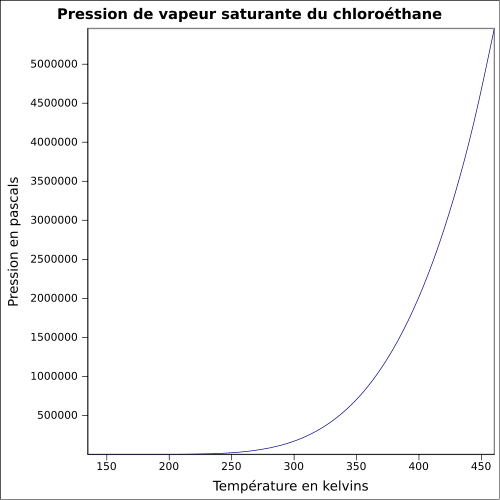
| Pression de vapeur saturante | à 20 °C : 133,3 kPa[1] | ||
| Point critique | 187,2 °C; 52,4 bar[6] | ||
| Point triple | −138,33 °C | ||
| Thermochimie | |||
| ΔfH0gaz | -112,3 kJ/mol[7] | ||
| Cp | 103.3 J/mol.K (liquide)[8] | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 10,98 ± 0,02 eV (gaz)[10] | ||
| Précautions | |||
| SGH[12] | |||
| H220, H351 et H412 | |||
| SIMDUT[13] | |||
  A, B1, | |||
| NFPA 704 | |||
| Transport | |||
| |||
| Classification du CIRC | |||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[11] | |||
| Écotoxicologie | |||
| LogP | 1,54[1] | ||
| Seuil de l’odorat | bas : 4,2 ppm[14] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier | |||
Le chloroéthane ou monochloroéthane, généralement connu par son ancienne appellation chlorure éthylique (ou chlorure d'éthyle, plus anciennement nommé éther muriatique), est un composé chimique autrefois employé couramment comme anesthésique, comme support de parfum ou pour produire le plomb tétraéthyle, un additif pour le carburant. C'est un gaz incolore et inflammable, très volatil, avec une odeur légère et douce.
C’est aussi un fluide frigorigène.
Historique
[modifier | modifier le code]Il aurait été découvert par Guillaume-François Rouelle, et utilisé comme anesthésique par Pierre Flourens[15].

Produit dans son usine de La Plaine en Suisse à partir de 1876 et commercialisé sous le nom de Kélène par la société chimique des usines du Rhône, il est utilisé comme anesthésique local puis comme support de parfum et, enfin, comme une sorte de fluide glacial parfumé qui sera vendu en très grande quantité au Brésil[16].
Utilisation
[modifier | modifier le code]
- réactif dans la synthèse du plomb tétraethyle : à partir des années 1920 et pendant la majeure partie du XXe siècle, le chlorure d'éthyle a été massivement utilisé pour la synthèse du principal additif de l'essence plombée. Après le retrait progressif des carburants au plomb entre 1976 et 2000, la production de chlorure d'éthyle a fortement chuté.
- liquide réfrigérant
- liquide propulseur dans les flacons d'aérosol et comme agent d'entraînement des mousses polymérisables.
- anesthésiant local : appliqué directement sur la peau sous forme de spray, il produit en s'évaporant une baisse rapide de température qui insensibilise momentanément la zone traitée. On l'utilise par exemple pour calmer la douleur à la suite de piqûre d'insecte ou pour une petite chirurgie locale. Il n'est en revanche pas utilisé en anesthésie générale en raison de sa toxicité.
- solvant des corps gras, des résines, du soufre, du phosphore.
- agent éthylant dans la synthèse de certains colorants, de médicaments et à plus grande échelle pour la préparation de l'éthylcellulose qui est un épaississant et un liant utilisé dans les peintures et les cosmétiques.
Production et synthèse
[modifier | modifier le code]Le chloroéthane est le produit de la réaction entre l'éthylène et le chlorure d'hydrogène avec un catalyseur de chlorure d'aluminium à des températures comprises entre 130 °C et 250 °C. Dans ces conditions, le chloroéthane est produit selon l'équation chimique :
Autrefois, le chlorure d'éthyle était également produit à partir de l'éthanol et de l'acide chlorhydrique, ou à partir de l'éthane et du chlore, mais ces procédés ne sont pas rentables. Une certaine quantité de chlorure d'éthyle est issue de la production du polychlorure de vinyle.
Sécurité
[modifier | modifier le code]Sécurité incendie
[modifier | modifier le code]C'est un produit extrêmement inflammable avec émission de gaz et fumées toxiques et irritants (chlorure d'hydrogène, phosgène notamment).
Toxicité
[modifier | modifier le code]Le chlorure d'éthyle est le moins toxique des chloroéthanes. Comme les autres hydrocarbures chlorés, il agit sur le système nerveux central mais dans une moindre mesure que d'autres composés similaires. L'inhalation de vapeurs à une concentration inférieure à 1 % ne donne généralement lieu à aucun symptôme. A une concentration plus élevée on observe des symptômes voisins de ceux que procure une intoxication éthylique. Au-delà d'une concentration supérieure à 15 %, l'exposition entraîne une perte de conscience, des désordres du fonctionnement cardiaque et peut s'avérer fatale.
Références
[modifier | modifier le code]- CHLOROETHANE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- (en) Nicholas P. Chopey, Handbook of Chemical Engineering Calculations, McGraw-Hill, , 3e éd., 800 p. (ISBN 978-0-07-136262-7), p. 1.43
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- Berthoud, A., Determination of Critical Temperatures and Pressures of Amines and Alkyl Chlorides, J. Chim. Phys. Phys.-Chim. Biol., 1917, 15, 3.
- Fletcher, R.A.; Pilcher, G., Measurements of heats of combustion by flame calorimetry. Part 7.-Chloromethane, chloroethane, 1-chloropropane, 2-chloropropane, Trans. Faraday Soc., 1971, 67, 3191-3201.
- Gordon, J.; Giauque, W.F., The entropy of ethyl chloride. Heat capacity from 18 to 287K. Vapor pressure. Heats of fusion and vaporization, J. Am. Chem. Soc., 1948, 70, 1506-1510.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-857-8)
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur monographs.iarc.fr, CIRC, (consulté le ).
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Chloroéthane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- « Ethyl chloride »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur hazmap.nlm.nih.gov (consulté le )
- Chlorure d’éthyle, auteur : Cazalaà Jean-Bernard https://char-fr.net/Chlorure-d-ethyle-2471.html
- Lefebvre Thierry, Raynal Cécile. Le Lance-parfum. Un matériel médical devenu accessoire de carnaval. In: Revue d'histoire de la pharmacie, 95ᵉ année, n°357, 2008. pp. 63-79. DOI : https://doi.org/10.3406/pharm.2008.6441 www.persee.fr/doc/pharm_0035-2349_2008_num_95_357_6441
Voir aussi
[modifier | modifier le code]- Bromoéthane
- Fluoroéthane
- Iodoéthane
- Dichloroéthane