Montelukast

| Montelukast | |
|---|---|
 | |
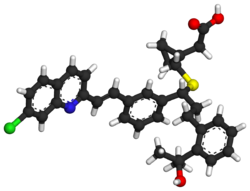 | |
| Nome IUPAC | |
| 2-[1-[[(1R)-1-[3-[2-(7-clorochinolin-2-il)etenil] fenill]-3-[2-(2-idrossi-2-metiletil)fenil]propil] sulfanilmetil]ciclopropil]Acetato | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C35H36ClNO3S |
| Massa molecolare (u) | 586.184 g/mol |
| Numero CAS | |
| Numero EINECS | 605-168-4 |
| Codice ATC | R03 |
| PubChem | 60951 |
| DrugBank | DBDB00471 |
| SMILES | CC(C)(C1=CC=CC=C1CCC(C2=CC=CC(=C2)C=CC3=NC4=C(C=CC(=C4)Cl)C=C3)SCC5(CC5)CC(=O)O)O |
| Dati farmacologici | |
| Modalità di somministrazione | orale |
| Dati farmacocinetici | |
| Biodisponibilità | dal 63% al 73% |
| Legame proteico | 99% |
| Metabolismo | Epatico, mediato da CYP3A4 e CYP2C9 |
| Emivita | 3-6 ore |
| Escrezione | biliare |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
Il montelukast è un farmaco antiasmatico con attività antagonista sui recettori per i leucotrieni.[2] In Italia il farmaco è venduto dalla società farmaceutica Merck Sharp and Dohme con il nome di Singulair nella forma farmacologica di compresse masticabili, ad uso pediatrico, di colore rosa contenenti 5 mg di principio attivo e di compresse rivestite da film di colore beige, da 10 mg. Essendo scaduto il brevetto sulla molecola il farmaco è prodotto da numerose altre società farmaceutiche come medicinale equivalente.
Farmacodinamica
[modifica | modifica wikitesto]Montelukast è un inibitore dei recettori dei leucotrieni, in particolare del recettore dei cisteinil-leucotrieni di tipo 1 (CysLT1). I cisteinil-leucotrieni (LTC4, LTD4, LTE4) sono degli eicosanoidi (fattori infiammatori) rilasciati da diverse cellule, tra cui mastcellule ed eosinofili. Il legame di questi leucotrieni con lo specifico recettore, causa la contrazione della muscolatura liscia bronchiale, aumentata la secrezione di muco, la permeabilità vascolare ed il reclutamento degli eosinofili (aumento degli eosinofili nel circolo periferico e nelle vie aeree). I leucotrieni sono quindi uno dei fattori responsabili dell'attacco asmatico.[2] Montelukast, e molecole simili come lo zafirlukast, sono antagoniste di tali recettori, funzionando cioè attraverso un meccanismo di saturazione recettoriale. Ciò significa che, legandosi ai recettori, non evocano alcuna risposta, ma impediscono meccanicamente ai ligandi fisiologici di interagirvi. I leucotrieni perciò, trovando i recettori occupati, non possono attivare la trasduzione del segnale che induce la broncocostrizione. A dimostrazione di ciò in studi clinici sperimentali montelukast a bassi dosaggi si è dimostrato in grado di inibire la broncocostrizione causata dall'inalazione di LTD4. Inoltre, montelukast risulta essere un inibitore più potente ed efficace rispetto a zafirlukast.[3]
Farmacocinetica
[modifica | modifica wikitesto]Dopo somministrazione per via orale montelukast viene rapidamente assorbito dal tratto gastroenterico. La concentrazione plasmatica massima (Cmax) viene raggiunta dopo circa 3 ore (Tmax) dalla somministrazione a digiuno. La biodisponibilità varia dal 63% al 73% (media del 64% circa). Biodisponibilità orale e picco plasmatico non sembrano essere influenzati dalla contemporanea assunzione di cibo. Il legame della molecola con le proteine plasmatiche è estremamente tenace: più del 99% di montelukast si lega ad esse, in particolare all'albumina.[4] Studi sperimentali sui ratti[5][6] e sull'uomo[5] hanno evidenziato che montelukast oltrepassa in modo significativo la barriera ematoencefalica, probabilmente per effetto di trasporto dell'albumina.
Rispetto allo zafirlukast, il montelukast presenta una più estesa metabolizzazione epatica. Gli studi effettuati mostrano un ampio coinvolgimento del citocromo P450 ed in particolare degli isoenzimi CYP3A4 e CYP2C9 e CYP2A6. L'ampio metabolismo spiega la più breve emivita di quest'ultima molecola, compresa tra le 3 e le 6 ore.[7] L'escrezione del farmaco avviene quasi esclusivamente tramite la bile. Gli studi sperimentali con montelukast radiomarcato hanno mostrato che l'86% del farmaco viene eliminato nelle feci, entro cinque giorni, e meno dello 0,2% attraverso le urine.
Nei soggetti anziani e nei pazienti con insufficienza epatica da lieve a moderata, non è necessario alcun aggiustamento del dosaggio. Data la scarsa eliminazione per via renale, non è dato attendersi la necessità di aggiustamenti della dose nei soggetti con insufficienza renale.
Usi clinici
[modifica | modifica wikitesto]Montelukast trova indicazione per il trattamento dell'asma come terapia aggiuntiva, qualora altri agenti (agonisti β-adrenergici ad azione rapida e steroidi per via inalatoria)da usare "al bisogno" non si dimostrino efficaci nel fornire un adeguato controllo clinico. Al contrario dei farmaci Beta 2 agonisti selettivi, montelukast non serve per la terapia dell'attacco acuto di asma, né deve essere considerato una terapia sostitutiva dei corticosteroidi somministrati per via inalatoria. Il farmaco trova invece la propria applicazione nella prevenzione e nell'inibizione dell'insorgenza dell'asma, benché si sia dimostrato meno efficiente dei corticosteroidi assunti per via inalatoria.[8] Un ulteriore utilizzo si ha nei soggetti particolarmente sensibili all'azione broncocostrittrice dell'aspirina e di altri FANS,[3] così come nel trattamento sintomatico della rinite allergica stagionale,sempre nei soggetti in cui è indicato per la terapia dell'asma. Può essere inoltre utilizzato per la profilassi dell'asma in quei soggetti in cui predomina la broncocostrizione indotta dall'esercizio fisico.
Effetti collaterali
[modifica | modifica wikitesto]| Tipi di reazioni | Comuni (>1/100, <1/10) | Non comuni (>1/1.000, <1/100) | Rare (>1/10.000, <1/1.000) | Molto rare (<1/10.000) | Frequenza non nota |
|---|---|---|---|---|---|
| Malattie del sistema nervoso | |||||
| Disturbi psichiatrici(2) |
| ||||
| Malattie gastrointestinali | |||||
| Malattie cardiache |
| ||||
| Malattie respiratorie, toraciche e mediastiniche |
| ||||
| Malattie epatiche e biliari |
| ||||
| Disturbi della cute e del tessuto sottocutaneo |
|
|
|
| |
| Disturbi sistemici | |||||
| Malattie muscolo-scheletriche | |||||
| Esami di laboratorio |
|
(1) In soggetti che fanno uso degli antagonisti recettoriali dei leucotrieni è stata segnalato un minimo aumento dell'incidenza della sindrome di Churg-Strauss[8], evento che può derivare dallo smascheramento di tale fenomeno autoimmune dopo la sospensione dei farmaci corticosteroidei.
(2) A partire dal 2008 in letteratura medica apparvero degli studi inerenti ad una presunta relazione tra assunzione di montelukast e suicidio. Nel gennaio 2009, la Food and Drug Administration pubblicava uno studio dove veniva dimostrato che, benché non vi fossero ancora dati concernenti ulteriori problemi psichiatrici, poteva escludersi una correlazione tra assunzione di montelukast e tendenza al suicidio.[21] A distanza di alcuni mesi, nel giugno del 2009, sempre la Food and Drug Administration (FDA) emetteva un box warning, per tutti gli antileucotrienici, sulla scorta delle analisi di Farmacovigilanza.[22] In questo avviso l'agenzia del farmaco statunitense segnalava che: Tra gli eventi neuropsichiatrici segnalati, nei casi di sorveglianza post-marketing, vi sono agitazione, aggressività, ansia, alterazioni dei sogni e allucinazioni, depressione, insonnia, irritabilità, irrequietezza, pensieri e comportamenti suicidari (compreso il suicidio) e tremore.
Controindicazioni
[modifica | modifica wikitesto]La sospensione del corticosteroide a favore dell'inibitore recettoriale per i leucotrieni dovrebbe essere evitata in soggetti con notevole eosinofilia[3], poiché tali farmaci non sono in grado di deprimere le reazioni sistemiche sostenute dagli eosinofili.
Dosi terapeutiche
[modifica | modifica wikitesto]Nei soggetti adulti e negli adolescenti con più di 15 anni di età la dose consigliata è pari a 10 mg al giorno, da assumersi preferibilmente la sera. Il farmaco può essere assunto con o senza cibo e deve continuare ad essere assunto anche quando l'asma è sotto controllo, così come durante le fasi di peggioramento dell'asma. In alcuni soggetti può essere necessario ricorrere all'assunzione di dosi maggiori. Il montelukast viene sovente assunto con una posologia di 20 mg per due volte al giorno.[23] L'elevata compliance dell'assunzione orale di compresse rende questi farmaci particolarmente adatti ai bambini e a soggetti che non tollerano l'insufflazione del preparato farmacologico.[2] Montelukast, rispetto a zafirlukast, è maggiormente indicato nei bambini tra i 2 e i 5 anni (compresse masticabili da 4 mg) e nei bambini dai 4 ai 6 mesi (come granulato da 4 mg).[2]
Gravidanza e allattamento
[modifica | modifica wikitesto]La Food and Drug Administration (FDA) ha inserito il montelukast in classe B per l'uso in gravidanza. In questa classe sono inseriti i farmaci i cui studi riproduttivi sugli animali non hanno mostrato un rischio per il feto e per i quali non esistono studi controllati sull'uomo e i farmaci i cui studi sugli animali hanno mostrato un effetto dannoso (oltre a un decremento della fertilità) che non è stato confermato con studi controllati in donne nel I trimestre (e non c'è evidenza di danno nelle fasi avanzate della gravidanza).[24][25]
Studi effettuati sui ratti hanno mostrato che montelukast viene escreto nel latte materno. Non è noto se la molecola venga escreta nel latte delle donne che allattano al seno. Si rende pertanto necessario valutare con attenzione il rapporto rischio/beneficio di un'eventuale terapia.
Avvertenze
[modifica | modifica wikitesto]Pazienti pediatrici: la somministrazione di montelukast per periodi prolungati non altera il profilo di crescita lineare del bambino.[26]
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 27.09.2012, riferita al sale sodico idrato
- ^ a b c d Bertram G. Katzung, Farmacologia generale e clinica, Padova, Piccin, 2006, ISBN 88-299-1804-0.
- ^ a b c ST. Holgate, P. Bradding; AP. Sampson, Leukotriene antagonists and synthesis inhibitors: new directions in asthma therapy., in J Allergy Clin Immunol, vol. 98, n. 1, Lug 1996, pp. 1-13, PMID 8765812.
- ^ ME. Krawiec, SE. Wenzel, Leukotriene inhibitors and non-steroidal therapies in the treatment of asthma., in Expert Opin Pharmacother, vol. 2, n. 1, Gen 2001, pp. 47-65, DOI:10.1517/14656566.2.1.47, PMID 11336568.
- ^ a b (EN) Julia Marschallinger, Iris Schäffner e Barbara Klein, Structural and functional rejuvenation of the aged brain by an approved anti-asthmatic drug, in Nature Communications, vol. 6, 27 ottobre 2015, DOI:10.1038/ncomms9466. URL consultato il 3 dicembre 2015.
- ^ FDA, Montelukast. (Singulair, application number 20-829), in Pharmacology Review.
- ^ a b K. Malmstrom, G. Rodriguez-Gomez; J. Guerra; C. Villaran; A. Piñeiro; LX. Wei; BC. Seidenberg; TF. Reiss, Oral montelukast, inhaled beclomethasone, and placebo for chronic asthma. A randomized, controlled trial. Montelukast/Beclomethasone Study Group., in Ann Intern Med, vol. 130, n. 6, Mar 1999, pp. 487-95, PMID 10075616.
- ^ a b Brunton, Lazo, Parker, Goodman & Gilman - Le basi farmacologiche della terapia 11/ed, McGraw Hill, 2006, ISBN 978-88-386-3911-1.
- ^ TT. Postolache, Komarow H, Tonelli LH., Allergy: a risk factor for suicide?, in Curr Treat Options Neurol, vol. 10, n. 5, Dic 2008, pp. 363-76, PMID 18782509.
- ^ H. Jick, KW. Hagberg; P. Egger, Rate of suicide in patients taking montelukast., in Pharmacotherapy, vol. 29, n. 2, Feb 2009, pp. 165-6, DOI:10.1592/phco.29.2.165, PMID 19170586.
- ^ P. Manalai, JM. Woo; TT. Postolache, Suicidality and montelukast., in Expert Opin Drug Saf, vol. 8, n. 3, Mag 2009, pp. 273-82, DOI:10.1517/14740330902932688, PMID 19505261.
- ^ G. Philip, C. Hustad; G. Noonan; MP. Malice; A. Ezekowitz; TF. Reiss; B. Knorr, Reports of suicidality in clinical trials of montelukast., in J Allergy Clin Immunol, vol. 124, n. 4, Ott 2009, pp. 691-6.e6, DOI:10.1016/j.jaci.2009.08.010, PMID 19815114.
- ^ GT. Schumock, TA. Lee; MJ. Joo; RJ. Valuck; LT. Stayner; RD. Gibbons, Association between leukotriene-modifying agents and suicide: what is the evidence?, in Drug Saf, vol. 34, n. 7, Lug 2011, pp. 533-44, DOI:10.2165/11587260-000000000-00000, PMID 21663330.
- ^ GT. Schumock, RD. Gibbons; TA. Lee; MJ. Joo; RJ. Valuck; LT. Stayner, Relationship between leukotriene-modifying agent prescriptions dispensed and rate of suicide deaths by county in the US., in Drug Healthc Patient Saf, vol. 3, 2011, pp. 47-52, DOI:10.2147/DHPS.S23665, PMID 22046105.
- ^ G. Jamaleddine, K. Diab; Z. Tabbarah; A. Tawil; T. Arayssi, Leukotriene antagonists and the Churg-Strauss syndrome., in Semin Arthritis Rheum, vol. 31, n. 4, Feb 2002, pp. 218-27, PMID 11836655.
- ^ P. Guilpain, C. Pagnoux; F. Lhote; L. Mouthon; L. Guillevin, [Antileukotrienes and Churg-Strauss syndrome]., in Presse Med, vol. 36, 5 Pt 2, Mag 2007, pp. 890-4, DOI:10.1016/j.lpm.2007.01.034, PMID 17383148.
- ^ N. Nathani, MA. Little; H. Kunst; D. Wilson; DR. Thickett, Churg-Strauss syndrome and leukotriene antagonist use: a respiratory perspective., in Thorax, vol. 63, n. 10, Ott 2008, pp. 883-8, DOI:10.1136/thx.2007.093955, PMID 18492740.
- ^ J. Weeks, How alternative providers get their credentials., in Med Econ, vol. 76, n. 23, Dic 1999, pp. 130, 133-4, PMID 10788235.
- ^ DA. Sass, KB. Chopra; T. Wu, A case of montelukast-induced hepatotoxicity., in Am J Gastroenterol, vol. 98, n. 3, Mar 2003, pp. 704-5, PMID 12650820.
- ^ MF. Goldstein, J. Anoia; M. Black, Montelukast-induced hepatitis., in Ann Intern Med, vol. 140, n. 7, Apr 2004, pp. 586-7, PMID 15069001.
- ^ Food and Drug Administration, Follow-up to the March 27, 2008 Communication about the Ongoing Safety Review of Montelukast (Singulair), su fda.gov, FDA, 13 gennaio 2009. URL consultato il 4 luglio 2013.
- ^ Food and Drug Administration, Updated Information on Leukotriene Inhibitors: Montelukast (marketed as Singulair), Zafirlukast (marketed as Accolate), and Zileuton (marketed as Zyflo and Zyflo CR), su fda.gov, 2009. URL consultato il 3 luglio 2013 (archiviato dall'url originale il 22 giugno 2013).
- ^ Harrison, Principi di Medicina Interna (16ª edizione), New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
- ^ Onyeka Otugo, Olabode Ogundare, Christopher Vaughan, Emmanuel Fadiran, Leyla Sahin, Consistency of Pregnancy Labeling Across Different Therapeutic Classes (PDF), su fda.gov, Food and Drug Administration - Office of Women’s Health, 1979. URL consultato il 27 giugno 2013.
- ^ R. Sannerstedt, P. Lundborg; BR. Danielsson; I. Kihlström; G. Alván; B. Prame; E. Ridley, Drugs during pregnancy: an issue of risk classification and information to prescribers., in Drug Saf, vol. 14, n. 2, Feb 1996, pp. 69-77, PMID 8852521.
- ^ AB. Becker, O. Kuznetsova; J. Vermeulen; ME. Soto-Quiros; B. Young; TF. Reiss; SB. Dass; BA. Knorr, Linear growth in prepubertal asthmatic children treated with montelukast, beclomethasone, or placebo: a 56-week randomized double-blind study., in Ann Allergy Asthma Immunol, vol. 96, n. 6, Giu 2006, pp. 800-7, PMID 16802767.
Bibliografia
[modifica | modifica wikitesto]- Brunton, Lazo, Parker, Goodman & Gilman - Le basi farmacologiche della terapia 11/ed, McGraw Hill, 2006, ISBN 978-88-386-3911-1.
- Bertram G. Katzung, Farmacologia generale e clinica, Padova, Piccin, 2006, ISBN 88-299-1804-0.
- British National Formulary, Guida all’uso dei farmaci 4ª edizione, Lavis, Agenzia Italiana del Farmaco, 2007.
- Farma Annuario 2010.
- Philip G. Hustad CM, Analysis of behavior-related adverse experience in clinical trials of montelukas.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Montelukast
Wikimedia Commons contiene immagini o altri file su Montelukast
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) RCP USA (PDF), su accessdata.fda.gov.