Амид калия
 Из Википедии, бесплатной энциклопедии
Из Википедии, бесплатной энциклопедии
| Амид калия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование | Амид калия |
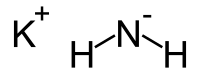
| Хим. формула | KNH2 |
| Физические свойства | |
| Состояние | белые или желтоватые кристаллы |
| Молярная масса | 55,12 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 338 °C |
| Классификация | |
| Рег. номер CAS | 17242-52-3 |
| PubChem | 87015 |
| Рег. номер EINECS | 241-275-9 |
| SMILES | |
| InChI | |
| ChemSpider | 78490 и 23354231 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ами́д калия — неорганическое вещество с формулой KNH2, производное аммиака. Белые или желтоватые кристаллы.
Получение
[править | править код]- Реакция гидрида калия с аммиаком:
- Реакция оксида калия с жидким аммиаком:
Физические свойства
[править | править код]Представляет собой белое кристаллическое вещество, на воздухе желтеет вследствие окисления. Плавится без разложения. В воде гидролизуется, в жидком аммиаке растворяется слабо[1].
Химические свойства
[править | править код]- При нагревании разлагается:
- Реагирует с водой:
- С неокисляющими кислотами:
- С окисляющими кислотами:
- Углеродом восстанавливается до цианида калия[1]:
Применение
[править | править код]- В органическом синтезе.
Примечания
[править | править код]- ↑ 1 2 Лидин, 2000, с. 40.
Литература
[править | править код]- Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |







