Цитотоксичні T-клітини

Цитотоксичні Т-клітини (також відомі як TC, цитотоксичні Т-лімфоцити, CTL, Т-кілери, цитолітичні Т-клітини, CD8+ Т-клітини) є Т-лімфоцитами (тип білих кров'яних тілець), які вбивають ракові клітини, інфіковані (особливо вірусами) клітини, або клітини, пошкоджені іншими способами.[1]
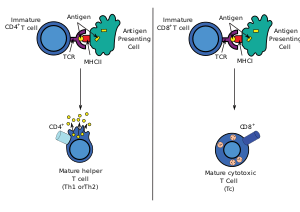
Більшість TC експресують Т-клітинні рецептори (TCR), які можуть розпізнавати специфічний антиген. Антиген — це молекула, здатна стимулювати імунну відповідь, яка часто виробляється раковими клітинами або вірусами. Антигени всередині клітини зв'язуються з молекулами ГКГС класу I і виносяться ними на поверхню клітини, де їх може розпізнати Т-клітина. Якщо TCR є специфічним до цього антигену, він зв'язується з комплексом молекули ГКГС класу I та антигеном, а TC руйнує клітину, що несе цей антиген.
Для того, щоб TCR зв'язувався з молекулою ГКГС класу I, він повинен супроводжуватися глікопротеїном під назвою CD8, який зв'язується з постійною частиною молекули ГКГС класу I. Тому ці Т-клітини називають CD8+ Т-клітинами .
Спорідненість між CD8 і молекулою ГКГС утримує клітини ТС і клітини-мішені, близько один до одного під час антиген-специфічної активації. CD8+ T-клітини вважаються цитотоксичними після відповідної активації. CD8+ Т-клітини також мають здатність виробляти деякі цитокіни.
Імунна система повинна розпізнавати мільйони потенційних антигенів. В організмі людини менше 30 000 генів, тому неможливо мати один ген для кожного антигена. Натомість ДНК в мільйонах білих кров'яних тільцях у кістковому мозку перекомбінується, що створює клітини з унікальними рецепторами, кожен з яких може зв'язуватися з різним антигеном. Деякі рецептори зв'язуються з тканинами самого організму людини. Тому, щоб запобігти самоушкодженню організму, ці аутореактивні білі кров'яні клітини руйнуються під час подальшого розвитку в тимусі (важливим елементом для цього є йод).[2]
TCR має дві частини, як правило, альфа- та бета-ланцюги (деякі TCR мають гамма- і дельта-ланцюги). Стовбурові гемопоетичні клітини в кістковому мозку мігрують в тимус, де відбувається V(D)J рекомбінація їхньої ДНК, яка кодує бета-ланцюг TCR з утворенням проміжної форми білка TCR, відомого як pre-TCR. Якщо ця перебудова успішна, клітини перебудовує свою ДНК TCR альфа-ланцюга, щоб створити функціональний комплекс альфа-бета TCR. Цей високомінливий продукт генетичної перебудови (рекомбінації) в генах TCR допомагає створити мільйони різних Т-клітин з різними TCR, допомагаючи імунній системі організму реагувати практично на будь-який білок інфекційного агента. Переважна більшість Т-клітин експресують альфа-бета-TCR (αβ-Т-клітини), але деякі Т-клітини в епітеліальних тканинах (наприклад, кишечника) експресують гамма-дельта-TCR (гамма-дельта-Т-клітини), які розпізнають небілкові антигени.
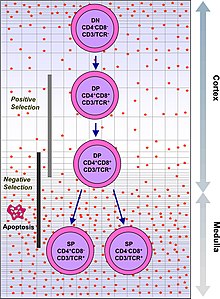
Т-клітини з функціонально стабільними TCR експресують як корецептори CD4, так і CD8, і тому їх називають «подвійно позитивними» (DP)Т-клітинами (CD4+CD8+). Подвійно позитивні Т-клітини піддаються впливу широкого спектру власних антигенів у тимусі та проходять дві форми відбору:
- позитивний відбір, при якому залишаються двічі позитивні Т-клітини, які зв'язуються з чужорідним антигеном у присутності власного ГКГС. Вони диференціюються на CD4+ або CD8+ залежно від того, який ГКГС асоціюється з представленим антигеном (ГКГС1 для CD8, ГКГС2 для CD4). Для диференціації у CD8+ Т-клітину антиген презентується в присутності ГКГС1. Позитивний відбір означає відбір тих TCR, які здатні розпізнавати власні молекули ГКГС.
- негативний відбір, при якому ті подвійно-позитивні Т-клітини, які занадто сильно зв'язуються з власними антигенами, які презентуються ГКГС, піддаються апоптозу, оскільки в іншому випадку вони можуть стати аутореактивними, що призведе до аутоімунітету.
Позитивно відбираються лише ті Т-клітини, які слабко зв'язуються з комплексами ГКГС-самоантиген. Ті клітини, які виживають при позитивному та негативному відборі, диференціюються в однопозитивні Т-клітини (або CD4+, або CD8+), залежно від того, чи розпізнає їх TCR антиген, представлений ГКГС класу I (CD8) або антиген ГКГС класу II (CD4). CD8+ Т-клітини дозрівають і перетворюються на цитотоксичні Т-клітини після їх активації антигеном, пов'язаним з ГКГС класу I.
За винятком деяких типів клітин (без'ядерні, включаючи еритроцити), ГКГС класу I експресується всіма власними клітинами організму. Коли ці клітини інфіковані вірусом (або іншим внутрішньоклітинним патогеном), відбувається розщеплення чужорідних білків шляхом процесингу антигену. В результаті утворюються пептидні фрагменти, деякі з яких презентуються рецептору CD8+ Т-клітин за допомогою ГКГС класу I.
Активація TC залежить від кількох одночасних взаємодій між молекулами, які експресуються на поверхні Т-клітини, і молекулами на поверхні антигенпрезентувальної клітини (АПК). Існує двосигнальна модель активації Тс-клітин:
| Сигнал | Т-клітина | АПК | Опис |
| Перший сигнал | TCR | зв'язана з пептидами молекула ГКГС класу I | Для стабілізації цього сигналу існує друга взаємодія між корецептором CD8 і молекулою ГКГС класу I. |
| Другий сигнал | Молекула CD28 на Т-клітині | CD80 або CD86 (також називаються B7-1 і B7-2) | CD80 і CD86 відомі як костимулятори для активації Т-клітин. Цей другий сигнал може бути посилений (або замінений), стимулюванням Тс-клітини цитокінами, вивільненими Т-хелперами. |
Проста активація наївних (неактивованих) CD8+Т-клітин вимагає взаємодії зі спеціалізованими АПК, в основному з дозрілими дендритними клітинами. Для створення довгоживучих Т-клітин пам'яті та для повторної стимуляції TC, дендритні клітини повинні взаємодіяти як з активованими CD4+ Т-клітинами-хелперами, так і з CD8+ Т-клітинами.[3][4] Під час цього процесу Т-хелпери «надають ліцензію» дендритним клітинам, на потужний активуючий сигнал наївним CD8+ Т-клітинам.[5]
Крім того, дозрівання CD8+ Т-клітин опосередковується через передачу сигналу CD40.[6] Після того, як наївна CD8+ Т-клітина зв'язується з інфікованою клітиною, інфікована клітина запускає вивільнення CD40.[6] Це вивільнення CD40 за допомогою Т-хелперів ініціює диференціацію наївних CD8+ Т-клітин у зрілі CD8+ Т-клітини.[6]
Хоча в більшості випадків активація TC залежить від розпізнавання антигену через TCR, були описані й альтернативні шляхи активації. Наприклад, було показано, що TC активуються під час дії інших CD8+ Т-клітин, що призводить до толерантності останніх.[7]
Після активації ТС клонуються за допомогою цитокіну інтерлейкіну 2 (IL-2), який є фактором росту і диференціювання для Т-клітин. Це збільшує кількість клітин, специфічних до антигену-мішені, які потім можуть подорожувати по всьому тілу в пошуках соматичних клітин на яких є ці антигени.
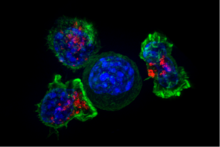
При дії на заражені/дисфункційні соматичні клітини, TC виділяють цитотоксини перфорин, гранзими і гранулізин. Завдяки дії перфорину гранзими потрапляють в цитоплазму клітини-мішені, де дія серинової протеази запускає каспазний каскад, який є серією цистеїнових протеаз, які, кінець-кінцем, призводять до апоптозу (запрограмованої смерті клітини). Через високу щільність ліпідів і негативно заряджений фосфатидилсерин, присутній в їх плазматичній мембрані, TC стійки до впливу власного перфорину і гранзимів.[8]
Другий спосіб викликати апоптоз — взаємодія між TC й інфікованою клітиною через клітинні поверхні. Коли TC активована, вона починає експресувати поверхневий білок FAS ліганд (FasL)(Apo1L)(CD95L), який може зв'язуватися з молекулою Fas (APO1) (CD95), що експресується на клітині-мішені. Однак, така взаємодія Fas-FasL, вважається більш важливою для видалення небажаних Т-лімфоцитів у процесі їх «тренування» або для літичної активності деяких клітин T-хелперів, ніж для цитолітичної активності ефекторних цитотоксичних T-клітин. Взаємодія Fas-FasL дозволяє залучити індукований некрозом сигнальний комплекс (DISC).[9] Fas-асоційований домен некрозу (FADD) транслокується з DISC, що дозволяє активувати прокаспази 8 і 10.[9] Ці каспази потім активують ефекторні каспази 3, 6 і 7, що призводить до розщеплення субстратів некрозу, таких як ламін A, ламін B1, ламін B2, PARP (полі-АДФ рибозополімераза) і DNA-PKcs (ДНК-активована протеїнкіназа). Кінцевим результатом є апоптоз клітини, яка експресує Fas.
Вважається, що транскрипційний фактор еомезодермін відіграє ключову роль у функції TC, діючи як регуляторний ген в адаптивній імунній відповіді.[10] Дослідження, що вивчали вплив втрати функції еомезодерміну, виявили, що зниження експресії цього транскрипційного фактора призвело до зменшення кількості перфорину, що виробляється TC.[10]
На відміну від антитіл, які ефективні як проти вірусних, так і проти бактеріальних інфекцій, TC в основному ефективні проти вірусів.[11]
Під час інфікування вірусом гепатиту B (HBV) TC вбивають інфіковані клітини та виробляють противірусні цитокіни, здатні очищати життєздатні гепатоцити від HBV. Вони також відіграють важливу патогенну роль, сприяючи майже всім ушкодженням печінки, пов'язаним з інфекцією HBV.[12] Було показано, що тромбоцити сприяють накопиченню вірус-специфічних TC в інфікованій печінці.[13]
TC причетні до прогресування артриту: деградація макромолекул хряща колінного суглоба, таких як глікозаміноглікани, TC та макрофагами спостерігалася на моделі захворювання у щурів.[14]
Встановлено, що CD8+ Т-клітини відіграють роль у ВІЛ-інфекції. З часом ВІЛ розробив багато стратегій, щоб уникнути імунної системи клітини-хазяїна. Наприклад, ВІЛ дуже сильно мутує, що дозволяє йому уникнути розпізнавання CD8+ Т-клітинами.[15] Він також здатен знижувати експресію поверхневих білків ГКГС класу I клітин, які він інфікує, для подальшого уникнення руйнування CD8+ Т-клітинами.[15] Якщо CD8+ Т-клітини не можуть знайти, розпізнати та зв'язатися з інфікованими клітинами, вірус не буде знищений і продовжить розмноження.
Крім того, TC можуть бути залучені до розвитку діабету 1 типу.[16] На додаток до ролі CD4+ клітин у цьому аутоімунному захворюванні, дослідження на мишачій моделі діабету показали, що TC також можуть відігравати певну роль, руйнуючи клітини острівців підшлункової залози, що виробляють інсулін.[16]
TC можуть бути необхідні для усунення периферичної нейропатії, спричиненої хіміотерапією (CIPN).[17][18] У мишей без TC спостерігається подовжений CIPN порівняно зі звичайними мишами, а ін'єкція «тренованих» TC усуває або запобігає CIPN.
Аномальна гіперактивація ТС може бути пов'язана з розвитком тяжкої ковідної пневмонії[19].
- ↑ Lymphocytes. Advanced Hematology in Integrated Cardiovascular Chinese Medicine. Elsevier. 2020. с. 41—46. doi:10.1016/b978-0-12-817572-9.00007-0. ISBN 978-0-12-817572-9.
Helper T cells/CD4+ •express CD4 glycoproteins on their cell surface, which activate in the presence of peptide antigens on the surface of invading pathogens; •respond immediately to protect the immune system; •secrete different cytokine proteins according to the immune response.
- ↑ Venturi S, Venturi M (September 2009). Iodine, thymus, and immunity. Nutrition. 25 (9): 977—9. doi:10.1016/j.nut.2009.06.002. PMID 19647627.
- ↑ Hivroz C, Chemin K, Tourret M, Bohineust A (2012). Crosstalk between T lymphocytes and dendritic cells. Critical Reviews in Immunology. 32 (2): 139—55. doi:10.1615/CritRevImmunol.v32.i2.30. PMID 23216612.
- ↑ Hoyer S, Prommersberger S, Pfeiffer IA, Schuler-Thurner B, Schuler G, Dörrie J, Schaft N (December 2014). Concurrent interaction of DCs with CD4(+) and CD8(+) T cells improves secondary CTL expansion: It takes three to tango. European Journal of Immunology. 44 (12): 3543—59. doi:10.1002/eji.201444477. PMID 25211552.
- ↑ Lanzavecchia A (1998). Immunology. Licence to kill. Nature. 393 (6684): 413—414. doi:10.1038/30845. PMID 9623994.
- ↑ а б в Bennett SR, Carbone FR, Karamalis F, Flavell RA, Miller JF, Heath WR (June 1998). Help for cytotoxic-T-cell responses is mediated by CD40 signalling. Nature (англ.). 393 (6684): 478—80. Bibcode:1998Natur.393..478B. doi:10.1038/30996. PMID 9624004.
- ↑ Milstein O, Hagin D, Lask A, Reich-Zeliger S, Shezen E, Ophir E, Eidelstein Y, Afik R, Antebi YE, Dustin ML, Reisner Y (January 2011). CTLs respond with activation and granule secretion when serving as targets for T-cell recognition. Blood. 117 (3): 1042—52. doi:10.1182/blood-2010-05-283770. PMC 3035066. PMID 21045195.
- ↑ Rudd-Schmidt JA, Hodel AW, Noori T, Lopez JA, Cho HJ, Verschoor S, Ciccone A, Trapani JA, Hoogenboom BW, Voskoboinik I (November 2019). Lipid order and charge protect killer T cells from accidental death. Nature Communications. 10 (1): 5396. doi:10.1038/s41467-019-13385-x. PMC 6881447. PMID 31776337.
{{cite journal}}: Недійсний|displayauthors=6(довідка) - ↑ а б Bakshi, Rakesh K.; Cox, Maureen A.; Zajac, Allan J. (2014). Cytotoxic T Lymphocytes. Encyclopedia of Medical Immunology. с. 332—342. doi:10.1007/978-0-387-84828-0_36. ISBN 978-0-387-84827-3.
- ↑ а б Pearce EL, Mullen AC, Martins GA, Krawczyk CM, Hutchins AS, Zediak VP, Banica M, DiCioccio CB, Gross DA, Mao CA, Shen H, Cereb N, Yang SY, Lindsten T, Rossant J, Hunter CA, Reiner SL (November 2003). Control of effector CD8+ T cell function by the transcription factor Eomesodermin. Science. 302 (5647): 1041—3. doi:10.1126/science.1090148. PMID 14605368.
- ↑ Kemball CC, Alirezaei M, Whitton JL (2010). Type B coxsackieviruses and their interactions with the innate and adaptive immune systems. Future Microbiology. 5 (9): 1329—1347. doi:10.2217/fmb.10.101. PMC 3045535. PMID 20860480.
- ↑ Iannacone M, Sitia G, Guidotti LG (2006). Pathogenetic and antiviral immune responses against hepatitis B virus. Future Virology. 1 (2): 189—96. doi:10.2217/17460794.1.2.189.
- ↑ Iannacone M, Sitia G, Isogawa M, Marchese P, Castro MG, Lowenstein PR, Chisari FV, Ruggeri ZM, Guidotti LG (November 2005). Platelets mediate cytotoxic T lymphocyte-induced liver damage. Nature Medicine. 11 (11): 1167—9. doi:10.1038/nm1317. PMC 2908083. PMID 16258538.
- ↑ Subramanian S, Ramalingam K (2005). Electron microscopic evidence on the participation Cytotoxic T Lymphocytes and Macrophages in Mtb adjuvant induced connective tissue inflammation and arthritogenesis in Rattus norvegicus. Asian Journal of Microbiology, Biotechnology and Environmental Sciences. 7 (2): 227—233. ISSN 0972-3005.
- ↑ а б Gulzar N, Copeland KF (January 2004). CD8+ T-cells: function and response to HIV infection. Current HIV Research. 2 (1): 23—37. doi:10.2174/1570162043485077. PMID 15053338.
- ↑ а б Tsai S, Shameli A, Santamaria P (2008). CD8+ T cells in type 1 diabetes. Advances in Immunology. 100: 79—124. doi:10.1016/S0065-2776(08)00804-3. PMID 19111164.
- ↑ Laumet G, Edralin JD, Dantzer R, Heijnen CJ, Kavelaars A (June 2019). Cisplatin educates CD8+ T cells to prevent and resolve chemotherapy-induced peripheral neuropathy in mice. Pain. 160 (6): 1459—1468. doi:10.1097/j.pain.0000000000001512. PMC 6527475. PMID 30720585.
- ↑ Krukowski K, Eijkelkamp N, Laumet G, Hack CE, Li Y, Dougherty PM, Heijnen CJ, Kavelaars A (October 2016). CD8+ T Cells and Endogenous IL-10 Are Required for Resolution of Chemotherapy-Induced Neuropathic Pain. The Journal of Neuroscience. 36 (43): 11074—11083. doi:10.1523/JNEUROSCI.3708-15.2016. PMC 5098842. PMID 27798187.
{{cite journal}}: Недійсний|displayauthors=6(довідка) - ↑ Kang, Chang Kyung; Han, Gi-Chan; Kim, Minji; Kim, Gwanghun; Shin, Hyun Mu; Song, Kyoung-Ho; Choe, Pyoeng Gyun; Park, Wan Beom; Kim, Eu Suk (2020-08). Aberrant hyperactivation of cytotoxic T-cell as a potential determinant of COVID-19 severity. International Journal of Infectious Diseases (англ.). Т. 97. с. 313—321. doi:10.1016/j.ijid.2020.05.106. PMC 7261468. PMID 32492530. Процитовано 30 листопада 2021.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання)