亚硝酰氯

| 亚硝酰氯 | |
|---|---|
 | |
 | |
| IUPAC名 Nitrosyl chloride | |
| 别名 | 氯化亚硝酰、 氯氧化氮、氧氯化氮 |
| 识别 | |
| CAS号 | 2696-92-6 |
| PubChem | 17601 |
| ChemSpider | 16641 |
| SMILES |
|
| UN编号 | 1069 |
| EINECS | 220-273-1 |
| RTECS | QZ7883000 |
| MeSH | nitrosyl+chloride |
| 性质 | |
| 化学式 | ClNO |
| 摩尔质量 | 65.46 g·mol⁻¹ |
| 外观 | 黄色气体或红色液体 固体为亮橙色[1] |
| 密度 | 1.417 g/cm3 (-12°C,液) 2.99 g/L(气) |
| 熔点 | -59.6 °C |
| 沸点 | -6.4 °C |
| 溶解性(水) | 反应 |
| 溶解性(其他溶剂) | 可溶于氯代烃 |
| 结构 | |
| 分子构型 | N原子为sp2杂化 |
| 偶极矩 | 1.90 D |
| 危险性 | |
| MSDS | ICSC 1580 |
| 主要危害 | 劇毒 |
| NFPA 704 | |
| 相关物质 | |
| 相关化学品 | 一氧化氮、硝酰氯、 亚硝基硫酸、 氟硼酸亚硝酰 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
亚硝酰氯(化学式:NOCl)是一个常见的亚硝酰化合物。室温下为不稳定的黄色气体,具刺鼻恶臭味,遇水分解,可溶于发烟硫酸中。存在于王水中。用作催化剂、有机化学试剂,也用于合成洗涤剂。具强腐蚀性,有毒,对眼部、皮肤和肺部有刺激性。
结构
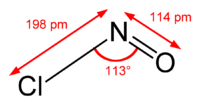
[编辑]NOCl分子为弯曲型,中心的N原子为sp2杂化。N=O双键键长为1.16 Å,N-Cl键长为1.69 Å,Cl-N-O键角为113°。[2]
制取
[编辑]- Cl2 + 2 NO → 2 NOCl
或用亚硝基硫酸与氯化氢反应:
- HCl + NOHSO4 → NOCl + H2SO4
- HNO3 + 3 HCl → Cl2 + 2 H2O + NOCl
反应
[编辑]- 与水反应,先生成亚硝酸和盐酸,进一步反应得到硝酸、亚硝酸、一氧化氮和盐酸等;
- 与碘反应,部分生成一氧化氮和一氯化碘;
- 与其他化合物发生复分解,得到其他亚硝酰盐,如氟硼酸亚硝酰。此反应常在液态NOCl中进行,它可以电离出NO+和Cl−,同时也用作溶剂;
- 加热至100°C时分解为氯气和一氧化氮;
- 与氧气反应,生成二氧化氮和氯气;
- 与烯烃加成,生成1-氯-2-亚硝基化合物,经互变异构得到α-氯代肟,水解生成α-卤代酮:[4]
参见
[编辑]参考资料
[编辑]- ^ Kristopher A. Rosadiuk, D. Scott Bohle. Anhydrous Dinitrogen Trioxide Solutions for Brønsted Acid Free Nitrous Acid Chemistry. European Journal of Inorganic Chemistry. 2017-12-15, 2017 (46): 5461–5465 [2022-08-31]. ISSN 1434-1948. doi:10.1002/ejic.201701091 (英语).
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ L. J. Beckham, W. A. Fessler, M. A. Kise. Nitrosyl Chloride. Chemical Reviews. 1951, 48: 319–396. doi:10.1021/cr60151a001.
- ^ Ohno, M,; Naruse, N.; Terasawa, I. (1973). "7-cyanoheptanal". Org. Synth.; Coll. Vol. 5: 266.

