磷化钠

| 磷化钠 | |
|---|---|
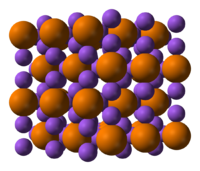 | |
| 别名 | sodium phosphide, common trisodiophosphine |
| 识别 | |
| CAS号 | 12058-85-4 |
| PubChem | 61547 |
| ChemSpider | 55463 |
| SMILES |
|
| InChI |
|
| InChIKey | FHHBFSHDCCEUKM-UHFFFAOYAE |
| 性质 | |
| 化学式 | Na3P |
| 摩尔质量 | 99.943 g·mol⁻¹ |
| 外观 | 红色固体 |
| 密度 | 1.74 g/cm3 |
| 熔点 | > 650 °C |
| 溶解性(水) | 不溶 |
| 溶解性 | 不溶于液态CO2 |
| 结构 | |
| 晶体结构 | 六方晶系 a = 4.9512 Å c = 8.7874 Å |
| 配位几何 | 三角双锥[1] |
| 相关物质 | |
| 其他阴离子 | 氯化钠 氮化钠 |
| 其他阳离子 | 磷化铝 磷化锂 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
磷化钠(Na3P)是一种红色固体,是由钠离子和磷离子构成的无机化合物。[2]Na3P能够提供非常活泼的磷离子。它用作磷化剂,制备磷化氢和农药。
除了Na3P,钠还已知多种磷化物,如NaP、Na3P7、Na3P11、NaP7和NaP15等。[3]
制备及性质
[编辑]磷化钠遇水立刻反应,生成剧毒且可燃的气体。
- Na3P + 3H2O → 3NaOH + PH3↑
参考资料
[编辑]- ^ Dong, Y; Disalvo, F.J. Reinvestigation of Na3P based on single-crystal data. Acta Crystallogr. E. 2005, 61 (11): i223–i224. doi:10.1107/S1600536805031168.
- ^ Yunle, G; Fan, G; Yiate, Q; Huagui, Z; Ziping, Y. A solvothermal synthesis of ultra-fine iron phosphide. Mater. Res. Bull. 2002, 37 (6): 1101–1106. doi:10.1016/S0025-5408(02)00749-3.
- ^ Inorganic Chemistry, Egon Wiberg, Arnold Frederick Holleman Elsevier 2001 ISBN 0-12-352651-5
| 这是一篇关于无机化合物的小作品。您可以通过编辑或修订扩充其内容。 |