Malattia infiammatoria pelvica

| Malattia infiammatoria pelvica | |
|---|---|
 | |
| Specialità | ginecologia |
| Classificazione e risorse esterne (EN) | |
| MeSH | D000292 |
| MedlinePlus | 000888 |
| eMedicine | 256448 |
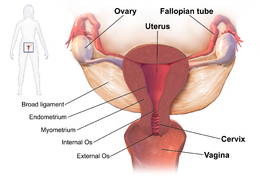
La malattia infiammatoria pelvica (in inglese Pelvic Inflammatory Disease, PID) è una infezione della parte superiore del sistema riproduttivo femminile, vale a dire dell'utero, delle tube di Falloppio e delle ovaie, all'interno del bacino.[1][2] Spesso si presenta senza alcun sintomo evidente.[3] I segni e i sintomi, quando si presentano possono includere dolore addominale inferiore, perdite vaginali, febbre, minzione con sensazione di bruciore, rapporti sessuali dolorosi e mestruazioni irregolari.[3] La condizione, se non trattata, può portare a complicazioni a lungo termine tra cui infertilità, gravidanza ectopica, dolore pelvico cronico e il cancro.[2][4][5]
La malattia è causata dalla diffusione dei batteri nella vagina e nella cervice.[6] Infezioni da Chlamydia trachomatis o Neisseria gonorrhoeae sono presenti dal 75% al 90% dei casi. Spesso sono coinvolti più batteri diversi.[2] In assenza di un trattamento, circa il 10% di quelli con una infezione da clamidia e il 40% di quelli con una infezione da gonorrea svilupperà una malattia infiammatoria pelvica.[2][7] I fattori di rischio sono simili, in generale, a quelli delle infezioni sessualmente trasmesse e includono un numero elevato di partner sessuali e l'uso di droghe. Le lavande vaginali possono aumentare anch'esse il rischio. Tipicamente la diagnosi si basa sulla presentazione dei segni e dei sintomi. Si raccomanda che la malattia possa essere considerata in tutte le donne in età fertile che hanno dolori al basso addome. Una diagnosi definitiva può essere formulata trovando del pus nelle tube di Falloppio, durante un intervento chirurgico. L'ecografia può anche essere utile nella diagnosi.[2]
La prevenzione per la malattia include non avere rapporti sessuali o avere un ristretto numero di partner e fare uso dei preservativi.[8] Lo screening delle donne a rischio di infezione da Chlamydia, seguito da un trattamento adeguato, diminuisce il rischio della malattia.[9] Se la diagnosi viene sospettata, si consiglia di procedere con un trattamento.[2] Il trattamento dovrebbe essere esteso anche i partner sessuali passati della donna.[10] In coloro con sintomi lievi o moderati, una singola iniezione dell'antibiotico ceftriaxone, seguito da due settimane di somministrazione di doxiciclina e, eventualmente, metronidazolo per via orale è comunemente raccomandato. Per coloro in cui non si nota un miglioramento dopo tre giorni o chi ha sperimentato una grave forma di infezione, la somministrazione per via endovenosa di antibiotici deve essere utilizzata.[11]
Nel 2008, a livello mondiale circa 106 milioni di casi di clamidia e 106 milioni di casi di gonorrea si sono verificati. Il numero di casi di malattia infiammatoria pelvica, tuttavia, non è chiaro.[10] Si stima che colpisca circa l'1,5% delle giovani donne ogni anno.[10] Secondo alcune stime, la condizione negli Stati Uniti interessa circa un milione di persone ogni anno.[12] A partire dal 1970, l'utilizzo di un tipo di dispositivo intrauterino (IUD), noto come lo scudo Dalkon ha portato ad un aumento dei tassi dell'infezione pelvica. Gli attuali IUD non sono associati a questo problema, dopo il primo mese di utilizzo.[2]
I processi infiammatori delle tube (salpingiti) e dell'ovaio (ovarite) vengono definiti annessiti: poiché in queste affezioni la flogosi si estende spesso anche al peritoneo, si parla di malattia infiammatoria pelvica.
Epidemiologia
[modifica | modifica wikitesto]Nel 2008, a livello mondiale si sono verificati circa 106 milioni di casi di clamidia e 106 milioni di casi di gonorrea.[7] Il numero di casi infiammazione pelvica, tuttavia, non sono chiari.[10] Si stima che colpisca circa il 1,5 per cento delle giovani donne ogni anno.[10] Si stima che negli Stati Uniti la condizione interessi circa un milione di persone ogni anno.[12] L'incidenza è più elevata negli adolescenti e nelle puerpere. La condizione provoca più di 100.000 casi di infertilità, negli soli Stati Uniti, ogni anno.[13][14]
Eziologia
[modifica | modifica wikitesto]Il Chlamydia trachomatis e il Neisseria gonorrhoeae sono di solito la principale causa della malattia infiammatoria pelvica. I dati suggeriscono che spesso la condizione è polimicrobica.[15] Microorganismi anaerobi facoltativi sono stati ottenuti dal tratto genitale superiore, mentre il N. gonorrhoeae è stato isolato nelle tube di Falloppio, altri organismi anaerobici facoltativi sono stati individuati nel tessuto endometriale.[16][17]
La struttura anatomica degli organi interni e dei tessuti del tratto riproduttivo femminile forniscono un percorso per gli agenti patogeni che ascendono dalla vagina dirigendosi verso la cavità pelvica. Il disturbo della naturale flora batterica vaginale associato a vaginosi batterica aumenta il rischio della malattia infiammatoria pelvica.[16]
N. gonorrhoeae e C. trachomatis sono gli organismi più comuni. Le infezioni meno comuni sono state causate esclusivamente da organismi anaerobi facoltativi. Gli anaerobi facoltativi e i batteri sono stati isolati nel 50% dei pazienti; mentre nel tratto genitale superiore sono stati trovati in quasi i due terzi dei pazienti con la condizione.[16] I microrganismi associati con la malattia infiammatoria pelvica sono elencati di seguito.[16]
Batteri coinvolti
[modifica | modifica wikitesto]I seguenti batteri sono rienuti per essere causa della malattia ifiammatoria pelvica:[16]
- Chlamydia trachomatis
- Neisseria gonorrhoeae
- Prevotella spp.
- Streptococcus pyogenes
- Prevotella bivia
- Prevotella disiens
- Bacteroides spp.
- Peptostreptococcus asaccharolyticus
- Peptostreptococcus anaerobius
- Gardnerella vaginalis
- Escherichia coli
- Streptococco del gruppo B
- Streptococco alfa-emolitico
- Stafilococco coagulasi negativi
- Atopobium vaginae
- Acinetobacter spp.
- Dialister spp.
- Fusobacterium gonidiaformans
- Gemella spp.
- Leptotrichia spp.
- Mogibacterium spp.
- Porphyromonas spp.
- Propionibacterium acnes
- Sphingomonas spp.
- Veillonella spp.
- Mycoplasma genitalium[17]
- Mycoplasma hominis
- Ureaplasma spp.[15]
Segni e sintomi
[modifica | modifica wikitesto]
I sintomi della malattia infiammatoria pelvica variano da nessuno (forma asintomatica) a gravi. Tra i possibili sintomi: febbre, dolore pelvico recente e bilaterale, dolore pelvico durante i rapporti sessuali (dispareunia) e sanguinamento post-coitale, dolore che inizia al termine delle mestruazioni, dolore durante l'esplorazione vaginale ai movimenti di lateralizzazione impressi all'utero, addome non perfettamente trattabile, tumefazione in sede annessiale, mestruazioni irregolari.[2][3][18][19]
Altre complicazioni includono endometrite, salpingite, ascesso tubo-ovarico, peritonite pelvica, periappendicite e periepatite.[15]
Diagnosi
[modifica | modifica wikitesto]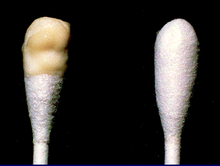

Un esame obiettivo ginecologico è fondamentale per formulare una diagnosi[6] con cui possono essere osservate una cervicite mucopurulenta e l'uretrite. Nei casi più gravi, ulteriori esami diagnostici possono essere richiesti, come la laparoscopia, la coltura dei batteri ottenuti tramite campionamento intra-addominale o la biopsia dei tessuti.[15][20]
La laparoscopia è in grado di visualizzare aderenze a "corda di violino", caratteristiche della sindrome di Fitz-Hugh-Curtis, e altri ascessi che possono essere presenti.[20]
Altre tecniche di imaging biomedico, come l'ecografia, la tomografia computerizzata (TC) e la risonanza magnetica possono aiutare nella diagnosi.[20] Gli esami del sangue possono aiutare ad identificare la presenza di infezione, attraverso test quali la velocità di eritrosedimentazione (VES), i valori della proteina C-reattiva e la ricerca di DNA di batteri.[15][20]
Il Nucleic Acid Test (AAT), il direct fluorescent antibody (DFA) e l'Enzyme-linked Immunosorbent Assay (ELISA) sono molto sensibili e in grado di identificare gli agenti patogeni specifici presenti. I test sierologici per gli anticorpi non appaiono così utili in quanto la presenza dei microrganismi in persone sane può confondere l'interpretazione dei livelli di titolo anticorpale.[15]
Criteri diagnostici definitivi comprendono l'evidenza istopatologica di endometrite, l'ispessimento delle tube di Falloppio o i risultati di una laparoscopia. Due terzi dei pazienti con evidenza laparoscopica di una precedente infiammazione pelvica non erano a conoscenza di esserne affetti, ma anche la condizione asintomatica può causare gravi danni. L'identificazione laparoscopica è utile nella diagnosi di malattia delle tube.[21]
Diagnosi differenziale
[modifica | modifica wikitesto]Un certo numero di altre patologie possono provacare sintomi simili, tra cui: appendicite, gravidanza ectopica, emorragia o rottura di cisti ovariche, endometriosi, gastroenterite, peritonite e vaginosi.[2]
La malattia infiammatoria pelvica può presentarsi con maggior probabilità quando vi è una precedente storia di infezione, un recente rapporto sessuale, recente inizio delle mestruazioni, inserimento di un dispositivo intrauterino o se il proprio partner ha una infezione a trasmissione sessuale.[22]
La malattia infiammatoria pelvica acuta è altamente improbabile, quando non vi sono stati rapporti recenti o un dispositivo intrauterino non è presente. Un test di gravidanza sierologico può essere eseguito per escludere una gravidanza ectopica. La culdocentesi è in grado di differenziare tra emoperitoneo (rottura di gravidanza ectopica o cisti emorragica) dalla sepsi pelvica (salpingite, rottura di ascesso pelvico o di appendice).[23]
L'ecografia pelvica e vaginale è utile per la diagnosi della malattia infiammatoria pelvica. Nelle prime fasi dell'infezione, l'ecografia può apparire normale. Col progredire della malattia, risultati non specifici possono includere liquido libero pelvico, ispessimento endometriale, distensione della cavità uterina da liquido o gas. In alcuni casi i confini dell'utero e delle ovaie possono essere indistinti. L'ingrossamento delle ovaie, accompagnato dall'aumento del numero di piccole cisti è correlabile con la malattia infiammatoria pelvica.[23]
Raramente si ricorre alla laparoscopia per diagnosticare la condizione, dato che non è prontamente disponibile. Inoltre, potrebbe non rilevare sottili infiammazione delle tube di Falloppio e non riesce a rilevare l'endometrite.[24]
Trattamento
[modifica | modifica wikitesto]
Spesso il trattamento viene iniziato senza che vi sia la conferma dell'infezione, per via delle gravi complicanze che possono derivare se la cura viene ritardata troppo. Il trattamento dipende l'agente infettivo e generalmente implica l'uso di una terapia antibiotica. Se non vi è alcun miglioramento entro due o tre giorni, alla paziente viene consigliato di provare ulteriori trattamenti farmacologici. Il ricovero in ospedale diventa a volte necessario se vi sono altre complicazioni. Trattare i partner sessuali per eventuali malattie sessualmente trasmissibili può aiutare nel trattamento e nella prevenzione.[9]
Per le donne con una infiammazione pelvica di lieve o moderata gravità, terapie orali o parenteralo sembrano essere efficaci.[25][26] I regimi tipici includono il cefotetan o la cefoxitina più la doxiciclina, la clindamicina con la gentamicina. Un regime alternativo è la somministrazione parenterale di ampicillina/sulbactam in aggiunta alla doxiciclina. Un'altra alternativa è quella di utilizzare un regime parenterale con ceftriaxone o cefoxitina più doxiciclina.[22] L'esperienza clinica guida la decisione per quanto riguarda la transizione da parenterale alla terapia orale, che può essere iniziato di solito entro 24-48 ore dopo che si riscontra un miglioramento clinico.[24]
Prognosi
[modifica | modifica wikitesto]Anche quando l'infezione è guarita, i suoi effetti possono essere permanenti; ciò rende la sua precoce identificazione essenziale per una buona prognosi. Il trattamento, con conseguente cura, è molto importante nella prevenzione di danni al sistema riproduttivo. L'eventuale formazione di tessuto cicatriziale a causa di uno o più episodi di malattia infiammatoria pelvica può portare al blocco delle tube, aumentando il rischio di incapacità di rimanere incinta e ad un dolore pelvico/addominale per lungo tempo.[27] Talune occorrenze, come un intervento chirurgico in zona pelvica, il periodo di tempo subito dopo il parto, il verificarsi di un aborto spontaneo o un aborto, aumentano il rischio di contrarre un'infezione che può portare a recidive della malattia.[22]
Complicazioni
[modifica | modifica wikitesto]La malattia infiammatoria pelvica può causare cicatrici all'interno del sistema riproduttivo, che possono poi causare gravi complicazioni, tra cui dolore cronico pelvico, infertilità, gravidanza ectopica (la principale causa di decessi legati alla gravidanza nelle donne adulte) e altre complicazioni della gravidanza. Occasionalmente, l'infezione può diffondersi al peritoneo e causare infiammazione e formazione di tessuto cicatriziale sulla superficie esterna del fegato (sindrome Fitz-Hugh-Curtis).[28]
Sindrome di Fitz-Hugh-Curtis
[modifica | modifica wikitesto]Si tratta dell'associazione tra Malattia Infiammatoria Pelvica ed aderenze tra diaframma e fegato. L'agente eziopatologico è più frequentemente il Gonococco. Caratteristica della malattia è l'associazione di sintomi ginecologici ed epatici. La prognosi non è peggiore rispetto alla forma solo ginecologica.
Prevenzione
[modifica | modifica wikitesto]Eseguire regolari test per le infezioni sessualmente trasmesse è utile per la prevenzione.[29] Il rischio di contrarre la malattia infiammatoria pelvica può essere ridotto dai seguenti comportamenti:
- Utilizzando metodi di barriera come i profilattici.[30]
- Consultare precocemente un medico se si accusano i sintomi della condizione.[30]
- L'utilizzo combinato di pillole anticoncezionali ormonali aiuta a ridurre le probabilità di contrarre infiammazioni per via dell'ispessimento del muco cervicale, impedendo così l'ascesa di organismi dal tratto genitale inferiore.[30]
- Consultare un medico dopo aver appreso che il partner attuale o un ex partner possa aver avuto un'infezione a trasmissione sessuale.[30]
- Diligenza nell'evitare attività vaginale, in particolare i rapporti dopo la fine di una gravidanza (parto, aborto spontaneo o aborto) o dopo alcune procedure ginecologiche, per garantire che la cervice si chiuda.[30]
- La monogamia sessuale che limita l'attività sessuale ad un partner esclusivo e che non abbia partner sessuali al di fuori della coppia.[31]
Note
[modifica | modifica wikitesto]- ^ Edward W. Campion, Robert C. Brunham, Sami L. Gottlieb e Jorma Paavonen, Pelvic Inflammatory Disease, in New England Journal of Medicine, vol. 372, n. 21, 21 maggio 2015, pp. 2039–2048, DOI:10.1056/NEJMra1411426, PMID 25992748.
- ^ a b c d e f g h i C Mitchell e M Prabhu, Pelvic inflammatory disease: current concepts in pathogenesis, diagnosis and treatment., in Infectious disease clinics of North America, vol. 27, n. 4, dicembre 2013, pp. 793–809, DOI:10.1016/j.idc.2013.08.004, PMID 24275271.
- ^ a b c Pelvic Inflammatory Disease (PID) Clinical Manifestations and Sequelae, su cdc.gov, ottobre 2014. URL consultato il 21 febbraio 2015 (archiviato dall'url originale il 22 febbraio 2015).
- ^ A. H. Chang e J. Parsonnet, Role of Bacteria in Oncogenesis, in Clinical Microbiology Reviews, vol. 23, n. 4, 2010, pp. 837–857, DOI:10.1128/CMR.00012-10, ISSN 0893-8512, PMC 2952975, PMID 20930075.
- ^ Philip J. Chan, Ibrahim M. Seraj, Theresa H. Kalugdan e Alan King, Prevalence of Mycoplasma Conserved DNA in Malignant Ovarian Cancer Detected Using Sensitive PCR–ELISA, in Gynecologic Oncology, vol. 63, n. 2, 1996, pp. 258–260, DOI:10.1006/gyno.1996.0316, ISSN 0090-8258, PMID 8910637.
- ^ a b Brunham RC, Gottlieb SL, Paavonen J, Pelvic inflammatory disease, in The New England Journal of Medicine, vol. 372, n. 21, 2015, pp. 2039–48, DOI:10.1056/NEJMra1411426, PMID 25992748.
- ^ a b World Health Organization, Global incidence and prevalence of selected curable sexually transmitted infections - 2008 (PDF), su who.int, 2012, pp. 2, 19. URL consultato il 22 febbraio 2015.
- ^ Pelvic Inflammatory Disease (PID) Patient Counseling and Education, su www2a.cdc.gov, Centers for Disease Control, ottobre 2014. URL consultato il 21 febbraio 2015 (archiviato dall'url originale il 22 febbraio 2015).
- ^ a b Pelvic Inflammatory Disease (PID) Partner Management and Public Health Measures, su www2a.cdc.gov, Centers for Disease Control, ottobre 2014. URL consultato il 21 febbraio 2015 (archiviato dall'url originale il 22 febbraio 2015).
- ^ a b c d e D Eschenbach, Acute Pelvic Inflammatory Disease, in Glob. libr. women's med., 2008, DOI:10.3843/GLOWM.10029, ISSN 1756-2228.
- ^ 2010 STD Treatment Guidelines Pelvic Inflammatory Disease, su cdc.gov, Centers for Disease Control, 15 agosto 2014. URL consultato il 22 febbraio 2015 (archiviato dall'url originale il 22 febbraio 2015).
- ^ a b Self-Study STD Modules for Clinicians - Pelvic Inflammatory Disease (PID) Next Centers for Disease Control and Prevention Your Online Source for Credible Health Information CDC Home Footer Separator Rectangle Epidemiology, su www2a.cdc.gov, Centers for Disease Control, ottobre 2014. URL consultato il 21 febbraio 2015 (archiviato dall'url originale il 22 febbraio 2015).
- ^ Pelvic Inflammatory Disease, su cdc.gov, Center For Disease Control, 4 maggio 2015. URL consultato il 14 luglio 2015.
- ^ MY Sutton, M Sternberg, A Zaidi, ME t Louis e LE Markowitz, Trends in pelvic inflammatory disease hospital discharges and ambulatory visits, United States, 1985–2001, in Sex Transm Dis, vol. 32, n. 12, dicembre 2005, pp. 778–84, DOI:10.1097/01.olq.0000175375.60973.cb, PMID 16314776.
- ^ a b c d e f Suncanica Ljubin-Sternak e Tomislav Mestrovic, Review: Clamydia trachonmatis and Genital Mycoplasmias: Pathogens with an Impact on Human Reproductive Health, in Journal of Pathogens, vol. 2014, n. 183167, 2014, DOI:10.1155/204/183167, PMC 4295611, PMID 25614838.
- ^ a b c d e Sharma H, Tal R, Clark NA, Segars JH, Microbiota and pelvic inflammatory disease, in Seminars in Reproductive Medicine, vol. 32, n. 1, 2014, pp. 43–9, DOI:10.1055/s-0033-1361822, PMC 4148456, PMID 24390920.
- ^ a b R. Lis, A. Rowhani-Rahbar e L. E. Manhart, Mycoplasma genitalium Infection and Female Reproductive Tract Disease: A Meta-Analysis, in Clinical Infectious Diseases, vol. 61, 2015, pp. 418–26, DOI:10.1093/cid/civ312, ISSN 1058-4838, PMID 25900174.
- ^ Ritu Kumar e Michael Stuart Bronze, Pelvic Inflammatory Disease Empiric Therapy, su emedicine.medscape.com, Medscape, 2015. URL consultato il 30 marzo 2015.
- ^ Bernadette Zakher, Amy G. Cantor MD, Monica Daeges e Heidi Nelson MD, Review: Screening for Gonorrhea and Chlamydia: A Systematic Review for the U.S. Prevententive Services Task Force, in Annals of Internal Medicine, vol. 161, n. 12, 16 dicembre 2014, pp. 884–894, DOI:10.7326/M14-1022.
- ^ a b c d Suzanne Moore MD, Pelvic Inflammatory Disease, su Michel Rivlin MD (a cura di), Medscape, Drugs and Diseases, Background, Medscape, 27 marzo 2014. URL consultato il 31 marzo 2015.
- ^ Thomas E. Andreoli e Russell L. Cecil, Cecil Essentials Of Medicine, 5th, Philadelphia, W. B. Saunders, 2001, ISBN 978-0-7216-8179-5.
- ^ a b c Pelvic Inflammatory Disease, su cdc.gov, CDC Fact Sheet, 4 maggio 2015. URL consultato il 15 luglio 2015.
- ^ a b Barbara Hoffman, Williams gynecology, 2nd, New York, McGraw-Hill Medical, 2012, p. 42, ISBN 978-0-07-171672-7.
- ^ a b Pelvic Inflammatory Disease, 2010 STD Treatment Guidelines, su cdc.gov, CDC, 28 gennaio 2011. URL consultato il 14 luglio 2015 (archiviato dall'url originale il 15 luglio 2015).
- ^ RB Ness, SL Hillier e KE Kip, Bacterial vaginosis and risk of pelvic inflammatory disease, in Obstet Gynecol, vol. 4, =Supp 3, 2004, pp. S111–22.
- ^ KJ Smith, RB Ness e HC Wiesenfeld, Cost-effectiveness of alternative outpatient pelvic inflammatory disease treatment strategies, in Sex Transm Dis, vol. 34, 2007, pp. 960–6.
- ^ Pelvic Inflammatory Disease, su cdc.gov, Center For Disease Control, 4 maggio 2015. URL consultato il 14 luglio 2015.
- ^ Pelvic Inflammatory Disease, su emedicine.medscape.com, MedScape, 27 marzo 2014. URL consultato il 10 marzo 2015.
- ^ KJ Smith, RL Cook e MS Roberts, Time from sexually transmitted infection acquisition to pelvic inflammatory disease development: influence on the cost-effectiveness of different screening intervals, in Value Health, vol. 10, n. 5, 2007, pp. 358–66, DOI:10.1111/j.1524-4733.2007.00189.x, PMID 17888100.
- ^ a b c d e Prevention - STD Information from CDC, su cdc.gov, Center For Disease Control, 5 giugno 2015. URL consultato il 21 febbraio 2015.
- ^ Ulrich H. Reichard, Monogamy: past and present, in Ulrich H. Reichard e Christophe Boesch (a cura di), Monogamy: Mating Strategies and Partnerships in Birds, Humans and Other Mammals, Cambridge University Press, 2003, pp. 3–25, ISBN 978-0-521-52577-0.
Bibliografia
[modifica | modifica wikitesto]- (EN) Thomas E. Andreoli e Russell L. Cecil, Cecil Essentials Of Medicine, 5th, Philadelphia, W. B. Saunders, 2001, ISBN 978-0-7216-8179-5.
- (EN) Barbara Hoffman, Williams gynecology, 2nd, New York, McGraw-Hill Medical, 2012, ISBN 978-0-07-171672-7.
- (EN) Ulrich H. Reichard, Monogamy: past and present, in Ulrich H. Reichard e Christophe Boesch (a cura di), Monogamy: Mating Strategies and Partnerships in Birds, Humans and Other Mammals, Cambridge University Press, 2003, ISBN 978-0-521-52577-0.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su malattia infiammatoria pelvica
Wikimedia Commons contiene immagini o altri file su malattia infiammatoria pelvica
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) pelvic inflammatory disease, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | J9U (EN, HE) 987007292813305171 |
|---|