ヒドロキシプロリン
 ウィキペディアから無料の百科事典
ウィキペディアから無料の百科事典
| ヒドロキシプロリン | |
|---|---|
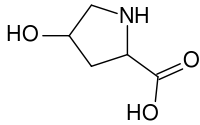 | |
| IUPAC名 | 4-ヒドロキシピロリジン-2-カルボン酸 |
| 別名 | γ-ヒドロキシ-L-プロリン、HYP |
| 分子式 | C5H9NO3 |
| 分子量 | 131.13 |
| CAS登録番号 | 51-35-4 |
| SMILES | OC1CNC(C1)C(O)=O |
ヒドロキシプロリン(Hydroxyproline)は天然に存在する二級環状アミノ酸(かつてはイミノ酸とも呼ばれた)の一種である。略称HYP。
構造[編集]
ヒドロキシプロリンは、プロリンのγ炭素原子にヒドロキシ基が結合した構造をしている。
また珪藻の細胞壁にあり、ケイ素の堆積に必要な2,3-シス-3, 4-トランス-ジヒドロキシプロリンのように、別の形のヒドロキシプロリンも天然に存在する。原生生物である卵菌にもヒドロキシプロリンが見られる[1]。
生産と機能[編集]
ヒドロキシプロリンはタンパク質合成後の翻訳後修飾として、プロリルヒドロキシラーゼによってプロリンにヒドロキシル基が導入されることにより生成される。
ヒドロキシプロリンはコラーゲンの主要な成分であり、プロリンとともにコラーゲンの安定性を担っている[2]。これらは、コラーゲンのらせんをきつく巻くことを可能にし[3]、また水素結合を作ることで、コラーゲンの三本鎖らせんを安定化している。コラーゲン以外には滅多に見られないが、哺乳類の持つタンパク質で他に唯一含まれているのはエラスチンである[4]。このため、ヒドロキシプロリンはコラーゲンやゼラチンの量を測定する指標となりうる。
医学的な意義[編集]
プロリンのヒドロキシル化にはアスコルビン酸(ビタミンC)が必要である。そのためビタミンCが不足するとコラーゲン中のヒドロキシプロリンの割合が少なくなって安定性が低下し、壊血病を引き起こす。
脚注[編集]
- ^ Alexopoulos, C. J., C. W. Mims, & M. Blackwell. 1996. Introductory Mycology, 4th ed., p. 687-688. (New York: John Wiley & Sons). ISBN 0-471-52229-5.
- ^ Nelson, D. L. and Cox, M. M. (2005) Lehninger's Principles of Biochemistry, 4th Edition, W. H. Freeman and Company, New York.
- ^ Brinckmann, J., Notbohm, H. and Müller, P. K. (2005) Collagen, Topics in Current Chemistry 247, Springer, Berlin.
- ^ Ward, A. G. and Courts, A. (1977) The Science and Technology of Gelatin, Academic Press, New York.
関連項目[編集]
外部リンク[編集]
- ヒドロキシリシン (別名:ヒドロキシリジン) - 素材情報データベース<有効性情報>(国立健康・栄養研究所)
- 4-ヒドロキシプロリン - 同
- ヒドロキシプロリン研究データ