原核生物
 ウィキペディアから無料の百科事典
ウィキペディアから無料の百科事典

原核生物(げんかくせいぶつ、英: prokaryote, or procaryote[1])は、核や他の膜結合細胞小器官を持たない単細胞生物である[2]。原核生物という用語は、古代ギリシア語の πρό (pró)「前」と κάρυον (káruon)「仁、核」に由来する[3][4]。エドゥアール・シャットンの研究に基づく2帝系では、原核生物は原核生物帝(Prokaryota)に分類されていた[5]。しかし、分子的分析に基づく3ドメイン系では、原核生物は 細菌(Bacteria、旧: Eubacteria)と古細菌(Archaea、旧: Archaebacteria)の2つのドメインに分けられる。細胞核(核)を持つ生物は、第3のドメインである真核生物(Eukaryota or Eucarya)に位置づけられる[6]。
原核生物は真核生物よりも先に進化し、真核細胞を特徴づける核、ミトコンドリア、その他の明確な細胞小器官のほとんどを持たない。かつては、原核生物の細胞質内に細胞構成要素は存在しないと考えられていたが(細胞外膜を除いて)、タンパク質の殻(例:エンカプスリン・タンパク質ケージ)に囲まれた準細胞小器官と考えられる細菌微小区画が[7][8]、他の原核生物の細胞小器官とともに発見された[9]。シアノバクテリアのような一部の原核生物は、単細胞である一方で、バイオフィルムによってまとまったコロニーを形成することがあり、大きなコロニーでは多層の微生物マットを形成することがある。粘液細菌のように、生活環に多細胞の段階を含むものもある[10]。原核生物は無性生殖を行い、配偶子の融合を伴わない二分裂によって生殖するが、遺伝子の水平伝播は起こりうる。
分子的研究は、生命の3ドメインの進化と相互関係について洞察を与えてきた[11]。原核生物と真核生物の区別は、2つの大きく異なるレベルの細胞組織の存在を反映している。染色体DNAを含む皮膜を持つ核と、ミトコンドリアなど他の特徴的な膜結合細胞小器官を持つのは真核細胞だけである。原核生物の特徴的な種には、好極限性細菌やメタン菌があり、これらはいくつかの極限環境でよく見られる[2]。
歴史[編集]
原核生物と真核生物の区別は、微生物学者のロジャー・スタニエとC・B・ヴァン・ニールが1962年に発表した論文『The concept of a bacterium(細菌の概念)』[12]で確立された(ただし、原核生物はprocaryote、真核生物はeucaryoteと表記された)。この論文では、1937年のエドゥアール・シャットンの著書『Titres et Travaux Scientifiques』[13]を引用してこれらの用語を使用し、区別を認めている。このような分類をした理由の一つは、当時はよく藍藻類(らんそうるい、英: blue-green algae)と呼んでいたもの(現在のシアノバクテリア)を植物として分類せず、細菌と合わせたグループにするためであった。
構造[編集]
細胞構造[編集]
原核生物の細胞骨格は、真核生物のそれよりも原始的である。アクチンとチューブリンの相同体(MreBとFtsZ)の他に、鞭毛(べんもう)を構成するらせん状に配列したフラジェリンは、細菌の基本的な細胞生理反応である走化性の構造的基礎を提供することから、細菌で最も重要な細胞骨格タンパク質の一つである。少なくとも一部の原核生物はまた、原始的な細胞小器官と見なせる細胞内構造体を含んでいる。
膜系細胞小器官(細胞内膜)は、光合成や化学無機栄養などの特殊な代謝特性に特化した液胞や膜系など、いくつかの原核生物のグループで知られている。さらに、いくつかの種には、特定の生理的役割を担う炭水化物に包まれた微小区画が存在する(たとえば、カルボキシソームやガス空胞)。
| 原核細胞の構成要素 | 構造 |
|---|---|
| 鞭毛(常に存在するとは限らない) | グラム陽性菌とグラム陰性菌の両方で使われる、細胞の運動を助ける長い鞭状の突起。 |
| 細胞膜 | 細胞の細胞質を取り囲み、細胞内外との物質の流れを調節する。 |
| 細胞壁(マイコプラズマ属とテルモプラズマ属を除く) | ほとんどの細胞で外側を覆い、菌体を保護し、形状を与える。 |
| 細胞質 | 主に水で構成されるゲル状の物質で、酵素、塩、細胞構成要素、さまざまな有機分子を含む。 |
| リボソーム | タンパク質生成を担う細胞構造体。 |
| 核様体 | 原核生物の単一のDNA分子を含む細胞質の領域。 |
| 細胞外被(糖衣とも。一部の原核生物の種のみ) | 細胞膜を取り囲む糖タンパク質-多糖類の皮膜。 |
| 細胞質封入体 | リボソームや細胞質マトリックス中に散在する大きな塊などの封入体。 |
大きさ[編集]

ほとんどの原核生物の大きさは1 µm-10 µmであるが、0.2 µm(マイコプラズマ・ジェニタリウム)から750 µm(チオマルガリータ・ナミビエンシス)までさまざまである。
形状[編集]
原核細胞はさまざまな形状をしている。細菌の基本的な形は、次の4つである[14]。
- 球菌 - 球形または卵形の細菌は球菌(複: cocci、単: coccus)と呼ばれる。たとえば、連鎖球菌、ブドウ球菌。
- 桿菌 - 円筒状の細菌は桿菌(かんきん、複: bacilli、単: rod, or bacillus)と呼ばれる。
- らせん状細菌 - 桿菌の中にはらせん状にねじれたものがあり、スピリラ(複: spirilla、単: spirillum)とも呼ばれる。
- ビブリオ - 巴(ともえ)形、コンマ型のもの。
古細菌のハロクアドラトゥム属は、平らな四角形の細胞である[15]。
生殖[編集]
無性生殖[編集]
細菌と古細菌は無性生殖を行い、通常は二分裂によって生殖する。それでも遺伝子交換や組み換えは起こるが、これは遺伝子の水平伝播の一形態であって複製過程ではなく、単に細菌接合のように2つの細胞間でDNA転移を伴うだけである。
DNA転移[編集]
原核細胞間のDNA転移は細菌と古細菌で起こるが、主に細菌で研究されてきた。細菌では、遺伝子転移は3つの過程で起こる。すなわち(1)細菌ウイルス(バクテリオファージ)を介した形質導入、(2)プラスミドを介した接合、(3)自然形質転換である。バクテリオファージによる細菌遺伝子の形質導入は、宿主細菌の適応というよりも、ウイルス粒子の細胞内集合の際の偶発的な誤りを反映しているようである。細菌DNAの転移は、(細菌遺伝子ではなく)バクテリオファージの遺伝子の制御下にある。よく研究されている大腸菌(Escherichia coli)系における接合はプラスミド遺伝子によって制御されており、ある細菌宿主から別の宿主にプラスミドの複製を分配するための適応である。この過程でまれに、プラスミドが宿主細菌の染色体に組み込まれ、その後、宿主細菌のDNAの一部が別の細菌に転移することがある。プラスミドを介した宿主細菌のDNA転移(接合)もまた、細菌適応というよりは、偶発的な過程のようである。
自然な細菌性形質転換は、培地を介したある細菌から別の細菌へのDNA転移を伴う。形質転換は、複雑な過程を実行するために特異的に相互作用する多くの細菌遺伝子産物に依存するため、導入や接合とは異なり、DNA転移を伴う細菌適応であることは明らかである[16]。細菌がドナーDNAを自身の染色体に結合し、取り入れ、組み換えるには、まずコンピテンスと呼ばれる特別な生理学的状態になる必要がある。枯草菌(Bacillus subtilis)ではコンピテンスの発現に約40個の遺伝子が必要とされる[17]。枯草菌の形質転換の際に転移するDNAの長さは、染色体全体の3分の1に及ぶことがある[18][19]。形質転換はDNA転移の一般的な様式であり、今のところ67種の原核生物が天然に形質転換能を備えていることが知られている[20]。
古細菌の中では、ハロバクテリウム・ボルカニ(Halobacterium volcanii)が細胞間に細胞質間橋を形成し、ある細胞から別の細胞へのDNA転移に使われているようである[21]。別の古細菌、スルフォロブス・ソルファタリカス(Sulfolobus solfataricus)は、直接接触することで細胞間でDNAを転移させる。Frolsら(2008)は、スルフォロブス・ソルファタリカスをDNA損傷因子に暴露すると細胞凝集が起こることを発見し、細胞凝集が細胞間のDNA転移を促進し、相同組み換えによる損傷DNAの修復を促進する可能性を示唆した[22]。
社会性[編集]
原核生物は厳密には単細胞生物であると考えられているが、そのほとんどは安定した凝集群集を形成することができる[23]。このような群集が安定化ポリマーマトリックス(粘液)に包まれている場合、バイオフィルムと呼ぶことがある[24]。バイオフィルム中の細胞は、しばしば時間的/空間的に異なる遺伝子発現パターン(表現型の分化)を示す。また、多細胞真核生物と同様に、こうした発現の変化はしばしば、細胞間でのシグナル伝達、すなわちクオラムセンシングとして知られる現象に起因しているように見える。
バイオフィルムは高度に不均一で構造的にも複雑であり、固体表面に付着したり、液体-空気界面、あるいは液体-液体界面に存在する可能性さえある。細菌バイオフィルムは多くの場合、マイクロコロニー(細菌とマトリックスのほぼドーム状の塊)で構成され、培地(たとえば水)が流れやすい空隙によって隔てられている。マイクロコロニーは基質上で結合して連続層を形成し、マイクロコロニーを隔てる流路網を閉鎖することもある。このような構造の複雑さと、バイオフィルム全体にわたる培地の移動によって酸素の制限(拡散の規模を超えて拡大するあらゆるものの遍在的な課題)が少なくとも部分的に緩和されるという観察とが相まって、これが循環系を構成しているのではないかと推測する者もおり[25]、多くの研究者が原核生物群集を多細胞性(multicellular)と呼ぶようになった(たとえば[26])。細胞発現の変動、集団行動、シグナル伝達、プログラム細胞死、そして(場合によっては)個別の生物学的拡散現象はどれも、この方向を指し示しているようである[27]。しかし、このようなコロニーは、(動物や植物が単一細胞から成長するに)単一の始祖によって形成されることはほとんどなく、多くの理論的問題を提起する。協力関係や多細胞性の進化に関するほとんど説明は、個体群(またはコロニー、あるいは生物全体)のメンバー間の高度な関連性に焦点を当ててきた。ある遺伝子の複製が集団のすべてのメンバーに存在する場合、メンバー間の協同を促進する行動により、それらのメンバーは利己的な個体からなる同様の集団よりも(平均して)高い適応度を持つことができるのかもしれない[28]。
もしこのような原核生物の社会性が例外的でなく、規則性に基づくことが証明されれば、原核生物全般に対する我々の見方や、医学における原核生物の扱い方に重大な影響を与えることになるだろう[29]。細菌バイオフィルムは、自由生活性の単細胞よりも抗生物質に対して100倍もの耐性を持つ可能性があり、一度表面にコロニーを形成すると除去することはほぼ不可能になる[30]。細菌接合やクオラムセンシングを介した病原性 (en:英語版) など、細菌性協同作用の別の側面は、関連疾患の治療を目指す研究者や医療関係者にさらなる課題をもたらす。
進化[編集]
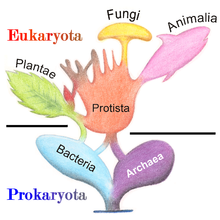

生物の進化に関する現在の一般的なモデルは、最初の生物は原始細胞から進化した何らかの原核生物で、真核生物は生命の歴史の後半に進化したというものである[32]。一部の著者はこの結論に疑問を呈しており、現在の原核生物種は、より複雑な真核生物の祖先から単純化の過程を経て進化した可能性があると主張している[33][34][35]。
また、生命の3つのドメインは、単一の遺伝子給源を形成する多様な細胞の集合から同時に発生したと主張する者もいる[36]。この論争は2005年に次のように要約された[37]。
細胞進化の全体像における真核生物の位置づけについて、生物学者の間で一致を得ていない。真核生物の起源と位置づけに関する現在の意見は、幅広い範囲に及んでいる。たとえば、真核生物が進化の中で最初に出現し、原核生物はその子孫であるという見解、真核生物は真正細菌や古細菌と同時期に出現したため、原核生物と同程度の年代と順位を持つ一次的な子孫であるという見解、真核生物は核の内部共生起源を伴う共生的な事象を通じて生じた、真核生物は内部共生を伴わずに生じた、真核生物は鞭毛と核の内部共生的起源を同時に伴う共生的な事象を通じて出現したなどの見解に加え、他にも多くのモデルがあり、それらは別の場所で検討され、要約されている。
知られている最古の原核生物の化石は約35億年前のもので、これは地球の地殻が形成されてからわずか約10億年後のことである。真核生物が化石記録に現れるのはその後で、複数の原核生物の祖先の内部共生(内共生)から進化して形成された可能性がある。最古の真核生物の化石は約17億年前のものである。しかし、真核生物が30億年前に出現したという遺伝学的な証拠もある[38]。
宇宙で生命が存在することが知られているのは地球だけだが、火星には化石あるいは生きている原核生物の証拠があるとする説もある[39][40]。しかし、この可能性についてはかなりの議論と懐疑が残されている[41][42]。
環境適応[編集]

原核生物は、その長い存在期間を通じて大きく多様化してきた。原核生物の代謝は、真核生物の代謝よりもはるかに多様であり、非常に多くの特徴的な原核生物が出現した。たとえば、真核生物のように光合成や有機化合物をエネルギー源とするだけでなく、硫化水素のような無機化合物からもエネルギーを得る原核生物もある。これによって原核生物は、低温生物学で研究される南極の雪面のように寒冷な環境でも、海底の熱水噴出孔や、陸上の熱水泉のような高温の環境でも、繁栄することができる。
原核生物は地球上のほぼすべての環境に生息している。一部の古細菌や細菌は好極限性細菌であり、高温(好熱菌)や高塩分(好塩菌)のような過酷な条件下で繁殖する[43]。古細菌の多くは海洋でプランクトンとして成長する。共生原核生物は、ヒトを含む他の生物の体内や体表に生息している。原核生物は、土壌(根圏や根鞘を含む)に多く生息している。土壌の原核生物は、人間の近くに存在し、農業にとって経済的に非常に重要であるにもかかわらず、まだ十分に解明されていない[44]。
分類[編集]
1977年、カール・ウーズは、2つの生物群における構造と遺伝学の大きな違いから、原核生物を細菌と古細菌(当初は真正細菌(Eubacteria)と古細菌(Archaebacteria))に分割することを提案した。古細菌は当初、極端な温度、pH、放射線のような劣悪な条件下でのみ生息する好極限性細菌であると考えられていたが、その後、あらゆる種類の生息地で発見されるようになった。その結果、真核生物、細菌、古細菌は、従来の2帝系に代わって3ドメイン系と呼ばれるようになった[45][46]。
Hugら(2016)によるゲノム解析による配列決定に基づく系統解析によれば、それらの関係は次の系統樹のようになる[47]。

真核生物との比較[編集]

原核生物と真核生物との境界は、通常、生物間の最も重要な区別または違いであると考えられている。その違いは、真核生物の細胞がDNAを含む「真の核」を持つのに対し、原核生物の細胞には核がないことである。
真核生物も原核生物も、タンパク質を作るリボソームと呼ばれる大きなRNA/タンパク質構造体を持つが、原核生物のリボソームは真核生物のそれよりも小さい。多くの真核細胞に見られるミトコンドリアと葉緑体という2つの細胞小器官は、原核生物に見られるものと同様の大きさと構造を持つリボソームを含んでいる[48]。これは、ミトコンドリアと葉緑体が自由生活性の細菌の子孫であることを示す多くの証拠のひとつである。細胞内共生説は、初期の真核細胞が食作用によって原始的な原核細胞を取り込み、その構造を組み入れるように自らを適応させた結果、ミトコンドリアや葉緑体が形成されたというものである。
原核生物のゲノムは、核様体と呼ばれる細胞質内のDNAとタンパク質の複合体の中にあり、核膜を持たない[49]。この複合体には、安定した染色体DNAの環状2本鎖分子が1つ含まれていて、真核細胞で見られる複数の密で高度に組織化された線状染色体とは対照的である。さらに、原核生物の重要な遺伝子の多くは、プラスミドと呼ばれる別の環状DNA構造体に保持されている[3]。真核生物と同様に、原核生物も遺伝物質を部分的に複製することがあり、部分的に複製された単数体の染色体構成を持つことができ、これはメロ二倍体として知られる状態である[50]。
原核生物にはミトコンドリアと葉緑体がない。その代わりに、酸化的リン酸化や光合成などの過程が、原核生物の細胞膜を隔てて行われる[51]。また原核生物は、原核細胞骨格のようないくつかの内部構造を持っている[52][53]。細菌門であるプランクトミケス門(Planctomycetota)は、核様体の周囲に膜を持ち、他の膜結合細胞構造を含むことが示唆されている[54]。しかし、さらなる調査により、プランクトミケス門の菌体は区画化も核形成もされておらず、他の細菌膜系と同様に相互に関連していることがわかった[55]。

原核細胞は通常、真核細胞よりもはるかに小さい[3]。そのため、原核生物は体積に対する表面積の比が大きく、真核生物よりも代謝率や成長速度が高く、その結果、世代時間は短くなる[3]。
真核生物のルーツは古細菌のアスガルド群、おそらくヘイムダル古細菌(Heimdallarchaeota)にある(あるいは少なくともその隣にある)という証拠が増えつつある[56]。この考えは1984年のエオサイト仮説[57]の現代版ともいえ、エオサイトはテルモプロテオータ(Thermoproteota)の古い同義語で、当時はまだ知られていなかったアスガルド群の近くに存在する分類群である。たとえば、通常は真核生物の核にDNAを収納するヒストンはいくつかの古細菌群でも見つかっており、相同性を示す証拠となっている。この考えは、細胞内共生説によれば、最初の真核細胞(LECA)を形成したアルファプロテオバクテリアを飲み込んだ真核細胞の謎に包まれた祖先を解明するかもしれない。さらに、細胞核ウイルス起源説と呼ばれるウイルスによる貢献があった可能性もある。古細菌と真核生物からなる非細菌群は、2002年にトーマス・キャバリエ=スミスによってネオムラと呼ばれた[58]。しかし分岐学的な見地では、鳥類は恐竜であるのと同じ意味で、真核生物は古細菌である(鳥類は恐竜の分類群であるマニラプトル類から進化した)。対照的に真核生物を除く古細菌は、鳥類を除く恐竜と同じように、側系統群であるように見える。
原核生物が2つの系統に分かれる可能性[編集]
原核生物と真核生物という基本的な区別という前述の仮定と異なり、生物相の最も重要な違いは、細菌とそれ以外(古細菌と真核生物)の区別かもしれない[56]。たとえば、DNA複製は細菌と古細菌(真核生物の核も含む)では根本的に異なっており、これら2つのグループ間では相同ではないのかもしれない[59]。また、ATP合成酵素はすべての生物で共通(相同)であるが、細菌(ミトコンドリアや葉緑体などの真核生物の細胞小器官を含む)と古細菌/真核生物の核グループでは大きく異なる。すべての生命の最後の共通祖先(LUCA、最終普遍共通祖先と呼ばれる)は、このタンパク質複合体の初期バージョンを持っていたはずである。ATP合成酵素は偏性であり膜結合型であるので、LUCAが細胞生物であったという仮説を支持している。LUCAがDNAを欠いたリボサイト(リボセルとも呼ばれる)であったかもしれないが、原始的な自己複製体としてのリボソームによってRNAゲノムを構築していたかもしれないことから、RNAワールド仮説はこのシナリオを明確にするかもしれない[60]。オリゴペプチドが原始核酸と同時に構築された可能性があるという考えに基づくペプチドRNAワールド仮説(RNPワールド)も、LUCAとしてのリボサイトの概念を支持している。ゲノムの物質的基盤としてのDNAの特徴は、その後、細菌と古細菌(そして、後には真核生物の核に)で別々に組み入れられた可能性があり、おそらく何らかのウイルス(レトロウイルスはRNAをDNAに逆転写することができる)の助けを借りたのだろう[61]。その結果、細菌と古細菌からなる原核生物も多系統化したのかもしれない。
脚注[編集]
- ^ “Definition of PROCARYOTE” (英語). www.merriam-webster.com. 2023年12月30日閲覧。
- ^ a b NC State University. “Prokaryotes: Single-celled Organisms”. 2014年8月6日閲覧。
- ^ a b c d Campbell, N. "Biology:Concepts & Connections". Pearson Education. San Francisco: 2003.
- ^ “prokaryote”. Online Etymology Dictionary. 2013年5月23日閲覧。
- ^ Sapp, J. (2005). “The Prokaryote-Eukaryote Dichotomy: Meanings and Mythology”. Microbiology and Molecular Biology Reviews 69 (2): 292–305. doi:10.1128/MMBR.69.2.292-305.2005. PMC 1197417. PMID 15944457.
- ^ Coté, Gary; De Tullio, Mario (2010). “Beyond Prokaryotes and Eukaryotes: Planctomycetes and Cell Organization”. Nature.
- ^ Kerfeld CA, Sawaya MR, Tanaka S, Nguyen CV, Phillips M, Beeby M, Yeates TO (August 2005). “Protein structures forming the shell of primitive bacterial organelles”. Science 309 (5736): 936–8. Bibcode: 2005Sci...309..936K. doi:10.1126/science.1113397. PMID 16081736.
- ^ Murat D, Byrne M, Komeili A (October 2010). “Cell biology of prokaryotic organelles”. Cold Spring Harbor Perspectives in Biology 2 (10): a000422. doi:10.1101/cshperspect.a000422. PMC 2944366. PMID 20739411.
- ^ Murat, Dorothee; Byrne, Meghan; Komeili, Arash (2010-10-01). “Cell Biology of Prokaryotic Organelles”. Cold Spring Harbor Perspectives in Biology 2 (10): a000422. doi:10.1101/cshperspect.a000422. PMC 2944366. PMID 20739411.
- ^ Kaiser D (October 2003). “Coupling cell movement to multicellular development in myxobacteria”. Nature Reviews. Microbiology 1 (1): 45–54. doi:10.1038/nrmicro733. PMID 15040179.
- ^ Sung KH, Song HK (July 22, 2014). “Insights into the molecular evolution of HslU ATPase through biochemical and mutational analyses”. PLOS ONE 9 (7): e103027. Bibcode: 2014PLoSO...9j3027S. doi:10.1371/journal.pone.0103027. PMC 4106860. PMID 25050622.
- ^ Stanier RY, Van Niel CB (1962). “The concept of a bacterium”. Archiv für Mikrobiologie 42 (1): 17–35. doi:10.1007/BF00425185. PMID 13916221.
- ^ Chatton, Édouard (1937). Titres Et Travaux Scientifiques (1906-1937) De Edouard Chatton. Sète: Impr. E. Sottano.
- ^ Bauman RW, Tizard IR, Machunis-Masouka E (2006). Microbiology. San Francisco: Pearson Benjamin Cummings. ISBN 978-0-8053-7693-7
- ^ Stoeckenius W (October 1981). “Walsby's square bacterium: fine structure of an orthogonal procaryote”. Journal of Bacteriology 148 (1): 352–60. doi:10.1128/JB.148.1.352-360.1981. PMC 216199. PMID 7287626.
- ^ Chen I, Dubnau D (March 2004). “DNA uptake during bacterial transformation”. Nature Reviews. Microbiology 2 (3): 241–9. doi:10.1038/nrmicro844. PMID 15083159.
- ^ Solomon JM, Grossman AD (April 1996). “Who's competent and when: regulation of natural genetic competence in bacteria”. Trends in Genetics 12 (4): 150–5. doi:10.1016/0168-9525(96)10014-7. PMID 8901420.
- ^ Akamatsu T, Taguchi H (April 2001). “Incorporation of the whole chromosomal DNA in protoplast lysates into competent cells of Bacillus subtilis”. Bioscience, Biotechnology, and Biochemistry 65 (4): 823–9. doi:10.1271/bbb.65.823. PMID 11388459.
- ^ Saito Y, Taguchi H, Akamatsu T (March 2006). “Fate of transforming bacterial genome following incorporation into competent cells of Bacillus subtilis: a continuous length of incorporated DNA”. Journal of Bioscience and Bioengineering 101 (3): 257–62. doi:10.1263/jbb.101.257. PMID 16716928.
- ^ Johnsborg O, Eldholm V, Håvarstein LS (December 2007). “Natural genetic transformation: prevalence, mechanisms and function”. Research in Microbiology 158 (10): 767–78. doi:10.1016/j.resmic.2007.09.004. PMID 17997281.
- ^ Rosenshine I, Tchelet R, Mevarech M (September 1989). “The mechanism of DNA transfer in the mating system of an archaebacterium”. Science 245 (4924): 1387–9. Bibcode: 1989Sci...245.1387R. doi:10.1126/science.2818746. PMID 2818746.
- ^ Fröls S, Ajon M, Wagner M, Teichmann D, Zolghadr B, Folea M, Boekema EJ, Driessen AJ, Schleper C, Albers SV (November 2008). “UV-inducible cellular aggregation of the hyperthermophilic archaeon Sulfolobus solfataricus is mediated by pili formation”. Molecular Microbiology 70 (4): 938–52. doi:10.1111/j.1365-2958.2008.06459.x. PMID 18990182.
- ^ Madigan T (2012). Brock biology of microorganisms (13th ed.). San Francisco: Benjamin Cummings. ISBN 9780321649638
- ^ Costerton, J. William (2007). “Direct Observations”. The Biofilm Primer. Springer Series on Biofilms. 1. Berlin, Heidelberg: Springer. pp. 3–4. doi:10.1007/978-3-540-68022-2_2. ISBN 978-3-540-68021-5
- ^ Costerton JW, Lewandowski Z, Caldwell DE, Korber DR, Lappin-Scott HM (October 1995). “Microbial biofilms”. Annual Review of Microbiology 49 (1): 711–45. doi:10.1146/annurev.mi.49.100195.003431. PMID 8561477.
- ^ Shapiro JA (1998). “Thinking about bacterial populations as multicellular organisms”. Annual Review of Microbiology 52 (1): 81–104. doi:10.1146/annurev.micro.52.1.81. PMID 9891794. オリジナルの2011-07-17時点におけるアーカイブ。.
- ^ Chua SL, Liu Y, Yam JK, Chen Y, Vejborg RM, Tan BG, Kjelleberg S, Tolker-Nielsen T, Givskov M, Yang L (July 2014). “Dispersed cells represent a distinct stage in the transition from bacterial biofilm to planktonic lifestyles”. Nature Communications 5 (1): 4462. Bibcode: 2014NatCo...5.4462C. doi:10.1038/ncomms5462. PMID 25042103.
- ^ Hamilton WD (July 1964). “The genetical evolution of social behaviour. II”. Journal of Theoretical Biology 7 (1): 17–52. Bibcode: 1964JThBi...7...17H. doi:10.1016/0022-5193(64)90039-6. PMID 5875340.
- ^ Balaban N, Ren D, Givskov M, Rasmussen TB (2008). “Introduction”. Control of Biofilm Infections by Signal Manipulation. Springer Series on Biofilms. 2. Berlin, Heidelberg: Springer. pp. 1–11. doi:10.1007/7142_2007_006. ISBN 978-3-540-73852-7
- ^ Costerton JW, Stewart PS, Greenberg EP (May 1999). “Bacterial biofilms: a common cause of persistent infections”. Science 284 (5418): 1318–22. Bibcode: 1999Sci...284.1318C. doi:10.1126/science.284.5418.1318. PMID 10334980.
- ^ Egel R (January 2012). “Primal eukaryogenesis: on the communal nature of precellular States, ancestral to modern life”. Life 2 (1): 170–212. Bibcode: 2012Life....2..170E. doi:10.3390/life2010170. PMC 4187143. PMID 25382122.
- ^ Zimmer C (August 2009). “Origins. On the origin of eukaryotes”. Science 325 (5941): 666–8. doi:10.1126/science.325_666. PMID 19661396.
- ^ Brown JR (February 2003). “Ancient horizontal gene transfer”. Nature Reviews. Genetics 4 (2): 121–32. doi:10.1038/nrg1000. PMID 12560809.
- ^ Forterre P, Philippe H (October 1999). “Where is the root of the universal tree of life?”. BioEssays 21 (10): 871–9. doi:10.1002/(SICI)1521-1878(199910)21:10<871::AID-BIES10>3.0.CO;2-Q. PMID 10497338.
- ^ Poole A, Jeffares D, Penny D (October 1999). “Early evolution: prokaryotes, the new kids on the block”. BioEssays 21 (10): 880–9. doi:10.1002/(SICI)1521-1878(199910)21:10<880::AID-BIES11>3.0.CO;2-P. PMID 10497339.
- ^ Woese C (June 1998). “The universal ancestor”. Proceedings of the National Academy of Sciences of the United States of America 95 (12): 6854–9. Bibcode: 1998PNAS...95.6854W. doi:10.1073/pnas.95.12.6854. PMC 22660. PMID 9618502.
- ^ Martin, William (2005). “Woe is the Tree of Life”. In Sapp, Jan. Microbial Phylogeny and Evolution: Concepts and Controversies. Oxford: Oxford University Press. pp. 139
- ^ Carl Woese, J Peter Gogarten, "When did eukaryotic cells (cells with nuclei and other internal organelles) first evolve? What do we know about how they evolved from earlier life-forms?" Scientific American, October 21, 1999.
- ^ McSween HY (July 1997). “Evidence for life in a martian meteorite?”. GSA Today 7 (7): 1–7. PMID 11541665.
- ^ McKay DS, Gibson EK, Thomas-Keprta KL, Vali H, Romanek CS, Clemett SJ, Chillier XD, Maechling CR, Zare RN (August 1996). “Search for past life on Mars: possible relic biogenic activity in martian meteorite ALH84001”. Science 273 (5277): 924–30. Bibcode: 1996Sci...273..924M. doi:10.1126/science.273.5277.924. PMID 8688069.
- ^ Crenson, Matt (2006年8月6日). “After 10 years, few believe life on Mars”. Associated Press (on space.com]). 2006年8月9日時点のオリジナルよりアーカイブ。2006年8月6日閲覧。
- ^ Scott ER (February 1999). “Origin of carbonate-magnetite-sulfide assemblages in Martian meteorite ALH84001”. Journal of Geophysical Research 104 (E2): 3803–13. Bibcode: 1999JGR...104.3803S. doi:10.1029/1998JE900034. PMID 11542931.
- ^ Hogan CM (2010). “Extremophile”. Encyclopedia of Earth. National Council of Science & the Environment
- ^ Cobián Güemes, Ana Georgina; Youle, Merry; Cantú, Vito Adrian; Felts, Ben; Nulton, James; Rohwer, Forest (2016-09-29). “Viruses as Winners in the Game of Life”. Annual Review of Virology (Annual Reviews) 3 (1): 197–214. doi:10.1146/annurev-virology-100114-054952. ISSN 2327-056X. PMID 27741409.
- ^ Woese CR (March 1994). “There must be a prokaryote somewhere: microbiology's search for itself”. Microbiological Reviews 58 (1): 1–9. doi:10.1128/MMBR.58.1.1-9.1994. PMC 372949. PMID 8177167.
- ^ Sapp J (June 2005). “The prokaryote-eukaryote dichotomy: meanings and mythology”. Microbiology and Molecular Biology Reviews 69 (2): 292–305. doi:10.1128/MMBR.69.2.292-305.2005. PMC 1197417. PMID 15944457.
- ^ a b Hug, Laura A.; Baker, Brett J.; Anantharaman, Karthik; Brown, Christopher T.; Probst, Alexander J.; Castelle, Cindy J.; Butterfield, Cristina N.; Hernsdorf, Alex W. et al. (2016-04-11). “A new view of the tree of life” (英語). Nature Microbiology 1 (5): 1–6. doi:10.1038/nmicrobiol.2016.48. ISSN 2058-5276.
- ^ Bruce Alberts (2002). The Molecular Biology of the Cell (fourth ed.). Garland Science. pp. 808. ISBN 0-8153-3218-1
- ^ Thanbichler M, Wang SC, Shapiro L (October 2005). “The bacterial nucleoid: a highly organized and dynamic structure”. Journal of Cellular Biochemistry 96 (3): 506–21. doi:10.1002/jcb.20519. PMID 15988757.
- ^ Johnston C, Caymaris S, Zomer A, Bootsma HJ, Prudhomme M, Granadel C, Hermans PW, Polard P, Martin B, Claverys JP (2013). “Natural genetic transformation generates a population of merodiploids in Streptococcus pneumoniae”. PLOS Genetics 9 (9): e1003819. doi:10.1371/journal.pgen.1003819. PMC 3784515. PMID 24086154.
- ^ Harold FM (June 1972). “Conservation and transformation of energy by bacterial membranes”. Bacteriological Reviews 36 (2): 172–230. doi:10.1128/MMBR.36.2.172-230.1972. PMC 408323. PMID 4261111.
- ^ Shih YL, Rothfield L (September 2006). “The bacterial cytoskeleton”. Microbiology and Molecular Biology Reviews 70 (3): 729–54. doi:10.1128/MMBR.00017-06. PMC 1594594. PMID 16959967.
- ^ Michie KA, Löwe J (2006). “Dynamic filaments of the bacterial cytoskeleton”. Annual Review of Biochemistry 75 (1): 467–92. doi:10.1146/annurev.biochem.75.103004.142452. PMID 16756499. オリジナルのNovember 17, 2006時点におけるアーカイブ。.
- ^ Fuerst JA (2005). “Intracellular compartmentation in planctomycetes”. Annual Review of Microbiology 59 (1): 299–328. doi:10.1146/annurev.micro.59.030804.121258. PMID 15910279.
- ^ Santarella-Mellwig R, Pruggnaller S, Roos N, Mattaj IW, Devos DP (2013). “Three-dimensional reconstruction of bacteria with a complex endomembrane system”. PLOS Biology 11 (5): e1001565. doi:10.1371/journal.pbio.1001565. PMC 3660258. PMID 23700385.
- ^ a b c Castelle CJ, Banfield JF (March 2018). “Major New Microbial Groups Expand Diversity and Alter our Understanding of the Tree of Life”. Cell 172 (6): 1181–1197. doi:10.1016/j.cell.2018.02.016. PMID 29522741.
- ^ a b Lake, J A; Henderson, E; Oakes, M; Clark, M W (1984-06). “Eocytes: a new ribosome structure indicates a kingdom with a close relationship to eukaryotes.” (英語). Proceedings of the National Academy of Sciences 81 (12): 3786–3790. doi:10.1073/pnas.81.12.3786. ISSN 0027-8424.
- ^ Cavalier-Smith T (March 2002). “The phagotrophic origin of eukaryotes and phylogenetic classification of Protozoa”. Int. J. Syst. Evol. Microbiol. 52 (Pt 2): 297–354. doi:10.1099/00207713-52-2-297. PMID 11931142.
- ^ Barry ER, Bell SD (December 2006). “DNA replication in the archaea”. Microbiology and Molecular Biology Reviews 70 (4): 876–87. doi:10.1128/MMBR.00029-06. PMC 1698513. PMID 17158702.
- ^ Lane N (2015). The Vital Question – Energy, Evolution, and the Origins of Complex Life. W. W. Norton. p. 77. ISBN 978-0-393-08881-6
- ^ Forterre, Patrick (2006). “Three RNA cells for ribosomal lineages and three DNA viruses to replicate their genomes: A hypothesis for the origin of cellular domain”. PNAS 103 (10): 3669–3674. Bibcode: 2006PNAS..103.3669F. doi:10.1073/pnas.0510333103. PMC 1450140. PMID 16505372.
参照項目[編集]
- 細菌の細胞構造 - 細菌の専門的な解剖学と生理学
- Combrex - 原核生物ゲノムの機能アノテーションなどのデータベース
- 細胞の進化 - 細胞の進化的起源およびその後の進化的発展
- 有性生殖の進化 - 有性生殖をする多細胞生物が共通祖先種から進化してきた過程
- 古細菌ゲノムの配列決定リスト - ゲノムの塩基配列が解読された古細菌の一覧
- 配列決定された細菌ゲノムのリスト - ゲノムの塩基配列が決定された真正細菌の一覧
- 海洋原核生物 - 海洋環境に生息する海洋細菌および海洋古細菌
- モネラ界 (または原核生物界) - 古細菌と細菌を含む旧式の生物界
- ナノバクテリア - かつて提唱されていた細菌属
- ナノーブ - 岩石と堆積物の微細な粒子状構造
- パラカリオン・ミョウジネンシス(Parakaryon myojinensis) - 原核生物と真核生物の間の過渡期にある可能性のある分類学上ユニークな単細胞生物
- ProGlycProt - 原核生物の糖鎖および糖タンパク質の実験的に検証されたデータベース