Celkern


| Celbiologie |
|---|
| De dierlijke cel |
 |
| Componenten van een dierlijke cel: |
| Portaal |
De celkern of nucleus is het door een membraan omsloten deel van een cel waarin het genetisch materiaal (DNA) is opgeslagen. Alle levende wezens waarvan de cellen een kern bevatten, worden ingedeeld bij de eukaryoten: dit zijn de planten, dieren, schimmels en de eencellige protisten.[a]
In de celkern is vrijwel al het DNA van het organisme opgeslagen.[b] Het DNA regelt de productie van eiwitten, die maken dat het hele organisme kan functioneren: alle erfelijke eigenschappen worden aangestuurd door informatie uit de celkern. Hierdoor wordt de celkern ook wel gezien als het 'controlecentrum' van de cel. Stoornissen in de organisatie van de celkern liggen ten grondslag aan diverse aandoeningen, reden waarom de celkern ook vanuit medisch oogpunt veel is onderzocht.[1]
De inhoud van de celkern, het kernplasma, wordt omsloten door een dubbel kernmembraan. Om transport van kleine moleculen mogelijk te maken bevat het verder ondoordringbare kernmembraan vele kernporiën. Grotere moleculen, zoals eiwitten en RNA-transcripten, worden actief met behulp van dragereiwitten door de poriën getransporteerd. Bij dierlijke cellen wordt de celkern verstevigd door een netwerk van filamenten, de kernlamina.
Hoewel de celkern in het verleden vaak gezien werd als een eenvoudig lichaampje, heeft de inhoud van de celkern een uiterst georganiseerde architectuur. Onder een elektronenmicroscoop zijn afzonderlijke gebieden van eiwitten, RNA-moleculen en delen van de chromosomen te onderscheiden in een welbepaalde samenhang.[2]
Structuur
[bewerken | brontekst bewerken]Eukaryoten zijn organismen die hun DNA opslaan in een afzonderlijk cellulair compartiment (organel) genaamd celkern of nucleus. Tot de eukaryoten behoren complexe levensvormen: de protisten, schimmels, wieren, planten en dieren, inclusief de mens. In dierlijke cellen is de celkern het grootste organel, dat met behulp van een lichtmicroscoop over het algemeen duidelijk zichtbaar is. Bij zoogdieren bereikt de celkern meestal een grootte van ongeveer 6 micrometer (μm), wat overeenkomt met ongeveer 10 procent van het totale celvolume.[3] De inhoud van de celkern wordt het kernplasma genoemd en is te vergelijken met het cytoplasma van de gehele cel. De dikke grondvloeistof van het kernplasma, het nucleosol, bevat de eiwitten en moleculen die nodig zijn voor het in stand houden en tot expressie brengen van het genetisch materiaal.[4]
Kernmembraan en poriën
[bewerken | brontekst bewerken]

(1) kernmembraan, (2) ringstructuur die de basis vormt van de porie, (3) tussenspaken, (4) korf en
(5) de cytoplasmafilamenten.
(1) kernmembraan, (2) ringstructuur die de basis vormt van de porie, (3) tussenspaken, (4) korf en
(5) de cytoplasmafilamenten.
Het kernmembraan vormt een aaneengesloten barrière rond de celkern en scheidt het genetisch materiaal van het omringende cytoplasma. Het voorkomt dat macromoleculen vrijelijk kunnen diffunderen tussen het kernplasma en het cytoplasma.[5] Het kernmembraan bestaat uit twee parallel aan elkaar afgezette membranen die gescheiden zijn door een tussenruimte van 10 tot 50 nanometer (nm). Het buitenste kernmembraan loopt over in de membraan van het endoplasmatisch reticulum. De ruimte tussen de membranen wordt perinucleaire ruimte genoemd.[5]
Kernporiën, de holle eiwitcomplexen die het moleculair verkeer in en uit de celkern verzorgen, zijn gelijkmatig over het kernmembraan verspreid. Ze zijn uit nucleoporines samengesteld, dat zijn grote structuureiwitten. De poriën hebben een gemiddeld molecuulgewicht van ongeveer 125 miljoen dalton.[6] Het eigenlijke kanaal waardoorheen moleculen getransporteerd worden is 5–10 nm in diameter. Aan de randen van de opening bevinden zich verschillende regulerende systemen. Via de openingen kunnen kleine, hydrofiele moleculen passief bewegen. Grotere moleculen, zoals nucleïnezuren en eiwitten, kunnen de poriën niet vrijelijk passeren. Deze moleculen worden actief – dat wil zeggen onder verbruik van energie – in en uit de celkern vervoerd.
Bij zoogdieren bevat de celkern ongeveer 3000 tot 4000 kernporiën.[c] De poriën zijn opgebouwd uit een ringstructuur met een achtvoudige rotatiesymmetrie.[7] Deze ring ligt op de plek waar de binnenste en buitenste membranen fuseren (in elkaar omklappen) en zo een opening vormen. Aan de ring is een korfvormige structuur gehecht die zich uitstrekt naar het kernplasma, en acht dradige filamenten die in het cytoplasma reiken. Beide structuren dienen om passage van transporteiwitten te begeleiden.[6]
Het transport van eiwitten, ribosoomdelen en nucleïnezuren door de kernporiën wordt gecontroleerd door transportfactoren die karyoferinen worden genoemd. Karyoferinen die het verkeer naar de kern verzorgen heten importines en karyoferinen die het verkeer uit de kern verzorgen heten exportines. Karyoferinen binden aan de te transporteren moleculen in het cytoplasma door herkenning van een signaalsequentie.[8] Na binding vervoeren ze het molecuul via interacties met de reguleringssystemen door de poriën heen.
Nucleaire lamina
[bewerken | brontekst bewerken]In dierlijke cellen is de celkern verstevigd door de zogenaamde nucleaire lamina, ook wel kernlamina genoemd. Dit is een vezelig netwerk van intermediaire filamenten dat nodig is voor het handhaven van structuur, vorm en beweeglijkheid. Ook speelt de lamina een rol bij het tot expressie brengen van het genetisch materiaal.[1] Bij sessiele organismen zoals schimmels en planten is de kernlamina afwezig.[d] De kernlamina staat in verbinding met het cytoskelet via membraaneiwitten aan de buitenkant van de celkern. De lamina vormt een verankeringspunt voor vele structuren, zowel inwendige (chromatine en chromosomen), als uitwendige (kernporiën).[3]
De kernlamina is voornamelijk opgebouwd uit het eiwit lamine.[10] Laminen zijn ketens van gevlochten monomeren die gevormd worden in het cytoplasma.[e] Via poriën gaan de ketens de celkern in, waar ze na samenvoeging met andere eiwitten worden opgenomen in de kernlamina. Ook aan de buitenkant van de kernmembraan binden laminen vast, zoals emerinen en nesprinen. Zij gaan interacties aan met het cytoskelet en zorgen daarmee dat de celkern zich op een vaste plek binnen het cytoplasma positioneert.
Het kan voorkomen dat de genen die voor laminen coderen muteren, waardoor deze eiwitten verkeerd worden aangemaakt. Een ontwikkelingsdefect van de kernlamina is bij mensen in verband gebracht met enkele zeldzame erfelijke aandoeningen die bekendstaan als laminopathieën. De meest bekende laminopathie is de ziekte progeria, die zich kenmerkt door vroegtijdige verouderingsverschijnselen bij kinderen. De exacte mechanismen die progeria veroorzaken zijn nog grotendeels onduidelijk, maar de meeste onderzoeken suggereren dat de oorzaak ligt bij mutaties in het lamine-eiwit.[1][12]

Chromosomen
[bewerken | brontekst bewerken]De celkern bevat het grootste deel van het genetisch materiaal van de cel.[b] Bij veel eukaryoten is het DNA in de kern rond eiwitten gewonden die histonen worden genoemd. Gedurende het grootste deel van de celcyclus – met name de periode waarin de cel niet deelt – zijn de histonen in elkaar vastgedraaid tot compacte draden (chromatine). Wanneer de cel zich gereedmaakt voor de mitose, wordt het chromatine gedeeltelijk ontrold om het DNA te kopiëren. Wanneer al het DNA gekopieerd is, trekt het zich samen tot staafvormige structuren, de chromosomen. Dit proces is doorgaans goed zichtbaar onder de lichtmicroscoop. Tijdens de celdeling splitsen de chromosomen uiteen in gelijke kopieën, zodat twee dochtercellen kunnen ontstaan die allebei beschikken over een identiek genoom.
De verdeling van het chromatine over de celkern is niet uniform door verschillende mate van ontvouwing ten behoeve van DNA-transcriptie. Het chromatine dat minder compact en vrijer in de celkern ligt wordt euchromatine genoemd. Het bevat de genen die veelvuldig door de cel tot expressie worden gebracht en dus voortdurend toegankelijk moeten zijn voor enzymen. Het chromatine dat daarentegen dichter is opgevouwen en zich meer aan de randen van de celkern bevindt wordt heterochromatine genoemd, en bevat het DNA dat weinig of niet door enzymen afgelezen wordt, zoals de sequenties van telomeren of centromeren.[15]
Doorsnede van twee dierlijke celkernen. De chromosomen zijn rood, het kernmembraan is blauw en de microtubuli zijn groen gekleurd. Schaal: 5 μm. | Ruimtelijke opname van twee dochterkernen. Deze dierlijke dochtercellen zijn in het laatste stadium van de deling: telofase. Het spoelfiguur is bruin, het cytoskelet groen en de nog gecondenseerde chromosomen blauw. |
Bij een aantal auto-immuunziekten, zoals systemische lupus erythematodes, richten de antilichamen van het lichaam zich tegen bepaalde onderdelen van het chromatine, zoals de nucleosomen.[16] Dergelijke antilichamen staan bekend als antinucleaire antistoffen (ANA's) en maken dat het immuunsysteem de eigen celkern aanziet als lichaamsvreemd. ANA’s komen ook voor bij de ziekte multiple sclerose als onderdeel van algemene stoornissen van het immuunsysteem.[17] In het geval van progeria is de rol van antilichamen bij het veroorzaken van auto-immuunsymptomen niet duidelijk.
Nucleolus
[bewerken | brontekst bewerken]
De nucleolus is een amorfe, membraanloze structuur in het kernplasma die voornamelijk uit RNA en bepaalde eiwitten bestaat. De nucleolus vormt zich rond specifieke delen van het chromatine, namelijk het DNA dat voor ribosomaal RNA codeert, de zogenaamde rDNA-sequenties. De vorming van dit ribosomaal RNA en de assemblage ervan met r-eiwitten tot ribosomen is de voornaamste functie van de nucleolus.
De grootte van de nucleolus reflecteert zijn activiteit: wanneer veel rRNA wordt gesynthetiseerd in de celkern, zal dit met eiwitten aggregeren tot een samenhangend lichaam. De grootte van de nucleolus is dus sterk afhankelijk van cellulaire activiteit, celgroei en celdifferentiatie. Wanneer de expressie van het rDNA wordt stilgelegd, ontwikkelt de nucleolus zich nauwelijks.[18]
De vorming van ribosomaal RNA gebeurt in de nucleolus met behulp van het enzym RNA-polymerase I. Het rDNA wordt overgeschreven naar een lang pre-rRNA-molecuul, dat vervolgens in een aantal delen gesplitst wordt en zich met ribosomale eiwitten organiseert tot een ribosoomdeel. Deze processen van transcriptie, posttranscriptionele modificatie en assemblage worden ondersteund door kleine RNA-moleculen genaamd snoRNA's.[f] De ribosoomdelen zijn de grootste structuren die vanuit de celkern doorheen de kernporiën worden getransporteerd. Arriverende in het cytoplasma koppelen de ribosoomdelen aan elkaar en verzorgen dan de eiwitsynthese.
Overige kernlichamen
[bewerken | brontekst bewerken]
Hoewel de term kernlichaam in informele zin vaak gebruikt wordt om de nucleolus aan te duiden, zijn er verschillende andere structuren in de celkern ontdekt die als afzonderlijk beschouwd dienen te worden. Belangrijke voorbeelden zijn Cajallichamen, clastosomen en PML-lichamen.[2][19]
Sommige kernlichaampjes kunnen ontstaan als gevolg van bepaalde ziekteprocessen. Dit is bijvoorbeeld het geval bij de spierziekte nemaline myopathie. Deze aandoening wordt veroorzaakt door een mutatie in het eiwit actine. Actine is nodig voor de opbouw van het cytoskelet en is in spiercellen rijkelijk aanwezig. Bij mensen met nemaline myopathie zal het gemuteerde actine in de celkern van spiercellen aggregeren; het klontert samen tot kleine lichaampjes, die met een krachtige microscoop zichtbaar zijn.[20]
Cajallichamen
[bewerken | brontekst bewerken]Over het algemeen bevat de celkern één tot tien compacte Cajallichamen. De diameter van deze lichaampjes kan variëren van 0,2 tot 2,0 μm, afhankelijk van het celtype en de soort. Wanneer ze onder een elektronenmicroscoop worden bekeken lijken ze op een ronde kluwen van draden.[g] Cajallichamen zijn betrokken bij RNA-processing, verwerking van snoRNA en diverse histon-mRNA-modificaties.[22]
Naast de Cajallichamen komen de vergelijkbare Gemini-lichamen of gems in de celkern voor. Gems komen qua structuur sterk overeen met de Cajallichamen: de twee zijn zelfs met geavanceerde microscopie nauwelijks te onderscheiden.[h] Het exacte verschil in functie tussen de twee lichaampjes is nog niet opgehelderd.[23] Gems lijken een rol te spelen in het ondersteunen van de vorming van snRNP-moleculen (kleine RNA-complexen die een rol spelen in splicing).[24]

(1) cytoplasma, (2) kernmembraan, (3) nucleolus, (4) paraspeckles.
Clastosomen
[bewerken | brontekst bewerken]Clastosomen zijn kleine, zeldzame kernlichamen (0,2 tot 0,5 μm), die een ringvormig uiterlijk hebben vanwege hun inkapseling.[25] Clastosomen zijn gewoonlijk niet in cellen aanwezig. Ze vormen zich onder sterk proteolytische omstandigheden en verdwijnen weer zodra de proteolyse-activiteit afneemt (bijvoorbeeld na het toedienen van protease-inhibitors). Ook bij osmotische stress kunnen de kernlichaampjes ontstaan.[26] Clastosomen zijn onder andere betrokken bij afbraak van eiwitten.[27]
PML-lichamen
[bewerken | brontekst bewerken]Promyelocytenleukemie-lichamen (PML-lichamen) zijn eiwitrijke structuren die verspreid over het kernplasma voorkomen en 0,1 tot 1,0 μm groot zijn. Ze zijn vernoemd naar hun belangrijkste bestanddeel, het promyelocytenleukemie-eiwit (PML). De lichaampjes kunnen zeer snel veranderen in aantal en chemische samenstelling. Er zijn aanwijzingen dat PLM-lichamen een rol spelen bij het tegengaan van tumorvorming, door schadelijke eiwitten in het kernplasma weg te vangen.[28]
Microscopie
[bewerken | brontekst bewerken]Kennis van de celkern wordt grotendeels verworven aan de hand van microscopisch onderzoek. Er bestaat een breed scala aan microscopische technieken die het mogelijk maakt om de celkern of onderdelen ervan in groot detail te bestuderen. Bij fluorescentiemicroscopie worden structuren in de kern, zoals het chromatine of het kernlamina, selectief gekleurd met behulp van een fluorescent molecuul. Omdat bij fluorescentiemicroscopie gewerkt kan worden met levende cellen, kan men begrip krijgen van beweging, interacties en dynamiek van cellulaire processen. Na de ontwikkeling van de elektronenmicroscoop werd de architectuur van de celkern tot op de moleculaire schaal ontrafeld.[29]
- Fluorescentiemicroscopie van cellen waarin de celkern gekleurd is met DAPI
- HeLa-cellen. De celkernen fluoresceren blauw. Roze duidt op delingsactiviteit.
- HeLa-cellen. Het cytoskelet is rood gekleurd. Kernen fluoresceren groen.
- Epitheelcellen van longarteriën. Kernen zijn blauw, mitochondriën oranje.
Functies
[bewerken | brontekst bewerken]Compartimentalisatie
[bewerken | brontekst bewerken]
De celkern is in de eerste plaats een afscheidend compartiment: het genetisch materiaal wordt op een gerichte manier van de rest van cel gescheiden, zodat de gevoelige DNA-moleculen afgeschermd worden van de buitenwereld en de processen van transcriptie en DNA-replicatie in een gecontroleerde omgeving kunnen verlopen.[30]
Door de scheiding is er continu communicatieverkeer nodig tussen het cytoplasma en kernplasma. Veel processen in het cytoplasma verlopen onder invloed van enzymen. De informatie voor de aanmaak van enzymen ligt opgeslagen in de celkern, maar de aanmaak zelf (de translatie) vindt plaats buiten de celkern. Wanneer een proces in de cel aan- of uitgeschakeld moet worden, kan een molecuul dat in het proces meespeelt naar de celkern gaan en daar de productie van enzymen reguleren.[i]
De verschillende RNA-moleculen die in de celkern worden gevormd, ondergaan vaak specifieke modificaties voordat ze naar het cytoplasma worden getransporteerd. Messenger-RNA (mRNA) moet bijvoorbeeld splicing ondergaan, transfer-RNA (tRNA) moet zichzelf lokaal opvouwen tot een klaverbladstructuur en ribosomaal RNA (rRNA) moet zich met eiwitten tot een ribosoom organiseren.[3] Wanneer een onverwerkt RNA-molecuul de celkern verlaat, is deze zelden functioneel.

Instandhouding van DNA
[bewerken | brontekst bewerken]In de celkern vindt replicatie van DNA plaats. Tijdens de replicatie worden de DNA-moleculen die zich in de celkern bevinden volledig gekopieerd, zodat bij de celdeling twee dochtercellen ontstaan die over dezelfde genetische informatie beschikken. Replicatie is een complex proces waarbij veel verschillende eiwitten zijn betrokken. De twee nucleotidestrengen van het DNA worden door het enzym helicase uit elkaar gehaald, waarna in beide richtingen nieuwe complementaire strengen worden gesynthetiseerd door DNA-polymerase. Nadat de replicatie is voltooid kunnen de DNA-moleculen condenseren tot chromosomen en uiteensplitsen voor de celdeling.
In het kernplasma zijn veel enzymen aanwezig die het DNA voortdurend controleren op beschadigingen. Zulke beschadigingen veranderen de ruimtelijke configuratie van de DNA-helixstructuur en kunnen door DNA-reparatiemoleculen worden opgespoord. De reparatiemoleculen werken vaak zeer efficiënt, waardoor schade aan DNA sterk wordt beperkt. DNA-reparatie is van essentieel belang voor de integriteit van het genoom. Veel genen die betrokken zijn bij reparatie en bescherming van DNA zijn een bepalende factor voor de levensduur van een individu.[32]
Genexpressie
[bewerken | brontekst bewerken]In eukaryoten vinden transcriptie en translatie plaats in afzonderlijke cellulaire compartimenten: transcriptie verloopt binnen de celkern, translatie verloopt in het cytoplasma. Er is sprake van een scheiding in ruimte en in tijd.[3] Bij prokaryoten zijn de twee processen nauw aaneengeschakeld: de translatie van bacterieel mRNA kan al beginnen terwijl de transcriptie nog gaande is. Door de ruimtelijke scheiding van transcriptie en translatie zijn eukaryoten in staat genexpressie op ingewikkelde manieren te reguleren, waardoor er veel meer structuren en functies ontwikkeld kunnen worden dan bij prokaryoten.[33]
Verwerking van mRNA
[bewerken | brontekst bewerken]Een andere belangrijke functie van de celkern is het reguleren van posttranscriptionele modificaties: wijzigingen aan het nieuw gevormde messenger-RNA. Het is essentieel dat nieuw gesynthetiseerde mRNA-moleculen (pre-mRNA) in de celkern gemodificeerd worden voordat ze naar het cytoplasma worden vervoerd; mRNA dat zonder modificaties in het cytoplasma terechtkomt, wordt snel afgebroken.[34] De drie voornaamste modificaties van pre-mRNA zijn het aanbrengen van een 5'-cap, het toevoegen van een poly(A)-staart en bovenal splicing.
Splicing van mRNA wordt uitgevoerd door een eiwitcomplex dat het spliceosoom wordt genoemd. Tijdens de splicing worden introns – korte regio's die niet coderen voor eiwitten – uit het pre-mRNA verwijderd. De resterende exons worden aan elkaar gekoppeld tot een compleet, transleerbaar molecuul (het mature mRNA). Doordat exons op verschillende manieren kunnen worden samengevoegd, kunnen verschillende mRNA-moleculen worden gevormd uit een enkel pre-mRNA. Dit proces van alternatieve splicing maakt het mogelijk uit een beperkte hoeveelheid DNA veel verschillende eiwitten te vormen.[6]
Dynamiek en regulatie
[bewerken | brontekst bewerken]Transport
[bewerken | brontekst bewerken]Elk van de kernporiën in het kernmembraan kan per seconde duizenden moleculen gecontroleerd laten passeren.[3] Het transport náár de celkern bestaat voornamelijk uit eiwitten (zoals laminen, DNA- en RNA-polymerase), nucleotiden, signaalmoleculen en lipiden; het uitgaand transport bestaat uit RNA-moleculen en ribosoomdelen. Kleine deeltjes kunnen vrijelijk door de kernporiën heen bewegen door middel van passieve diffusie.[35] Grotere deeltjes passeren de poriën met snelheden die afnemen met het molecuulgewicht: een groot eiwit passeert trager dan een klein eiwit. Voor het transport van grote moleculen is hulp nodig van dragereiwitten genaamd karyoferinen. Voor de invoer zorgen importines, voor de uitvoer exportines.
De energie die nodig is voor de invoer en uitvoer van stoffen door kernporiën, wordt gehaald uit de concentratiegradiënt van het energierijke molecuul GTP (een stof vergelijkbaar met ATP).[j] De verbindende factor tussen dit gradiënt en de karyoferinen is het enzym Ran, dat tussen de celkern en het cytoplasma circuleert. Wanneer Ran zich in het kernplasma bevindt, gaat het een binding aan met GTP; in het cytoplasma bindt het met het molecuul GDP. Het Ran-GTP-complex zorgt ervoor dat importines hun invoermolecuul loslaten, en dat exportines hun uitvoermolecuul juist binden. Het omgekeerde geldt voor Ran-GDP.[8]
Alle RNA-moleculen die in de celkern worden gevormd, worden naar buiten getransporteerd door gespecialiseerde exporteiwitten. Alleen wanneer alle posttranscriptionele modificaties en verdere afwerkingen aan het RNA zijn voltooid, gaan de exporteiwitten een binding aan met het RNA. Ook deze exporteiwitten maken gebruik van de GTP-gradiënt, maar op basis van een ander mechanisme, aangezien het hier gaat om eenrichtingsverkeer.
Opbouw en afbraak
[bewerken | brontekst bewerken]
Gedurende één celcyclus vindt volledige opbouw en afbraak van de celkern plaats. Wanneer een cel zich gereedmaakt voor deling, worden de structurele elementen van de celkern – het kernmembraan en de lamina – systematisch ontmanteld. In de meeste eukaryotische cellen vindt ontmanteling van de kern plaats tijdens de profase (het eerste stadium van de mitose). Bij sommige eencellige eukaryoten, zoals gistcellen, blijft de celkern tijdens de deling intact. De dochterchromosomen bewegen dan naar de tegenovergelegen uiteinden van de celkern, en uiteindelijk splitst deze in tweeën. In hogere eukaryoten worden de chromosomen door een spoelfiguur naar beide uiteinden van de cel getrokken.[k] Na insnoering en deling van het cytoplasma vormt zich een nieuw kernmembraan rond de chromosomen.
Om er zeker van te zijn dat de microtubuli van het spoelfiguur zich aan de chromosomen kunnen vasthechten, wordt het kernmembraan rond de chromosomen tijdig afgebroken. Als deze te veel intact blijft, komt de mitose niet op gang.[36] Het ontmantelingsproces van het kernmembraan en de lamina wordt gereguleerd door eiwitkinases die onder andere de laminen in de celkern voorzien van een fosfaatgroep (fosforylering). De lamine-eiwitten laten van elkaar los waardoor de celkern desintegreert. Tegen het eind van de mitose worden de fosfaatgroepen weer verwijderd, waardoor de structuureiwitten weer bijeenkomen en de celkern zich hervormt.[36]
Kwantiteit
[bewerken | brontekst bewerken]Verreweg de meeste eukaryotische cellen hebben een enkele celkern. Bij gespecialiseerde celtypen kan de celkern echter afwezig zijn, of juist in meervoud voorkomen. Kernloze cellen kunnen ontstaan wanneer de cel door een fout onevenredig deelt, zodat de ene dochtercel een kern mist en de andere twee kernen heeft. Meestal is een afwijkend aantal kernen echter het gevolg van normale processen, zoals bij de kernloze rode bloedcellen. Dwarsgestreepte spierweefsels zijn opgebouwd uit cellen die versmolten zijn, waardoor er meerdere kernen in een individuele cel aanwezig kunnen zijn.[37] Ook bij schimmels en eencelligen is meerkernigheid geen zeldzaam fenomeen.
Kernloze cellen
[bewerken | brontekst bewerken]Cellen die geen celkern bevatten zijn uitsluitend opgebouwd uit cytoplasma en zijn daarom niet in staat om dochtercellen te produceren. Een bekend voorbeeld van kernloze lichaamscellen zijn rode bloedcellen. Rode bloedcellen ontwikkelen zich in het beenmerg via een proces genaamd erytropoëse, waarbij ze hun kern en organellen verliezen. Tijdens de differentiatie van een erytroblast naar een reticulocyt – de voorlopers van een rode bloedcel – wordt de kern fysiek uit de cel verdreven. Men vermoedt dat dit de cel klein en flexibel genoeg maakt om door haarvaten te kunnen bewegen.[38] Mutagene stoffen kunnen ervoor zorgen dat de bloedcellen in wording te vroeg aan de bloedbaan worden afgegeven. Hierdoor ontstaan er erytrocyten met gereduceerde "microkernen".[39]
In bedektzadigen bestaat een vergelijkbaar proces voor zeefcellen. Zeefcellen vormen lange, aaneengesloten vaten waarlangs water en voedingsstoffen getransporteerd worden. Gedurende de differentiatie van zeefcellen degenereren de celkern, de tonoplast en andere organellen, zodat er in de floëemcellen ruimte ontstaat voor efficiënt watertransport.[40]
Meerkernige cellen
[bewerken | brontekst bewerken]
Er bestaan diverse levensvormen die volledig of gedeeltelijk zijn opgebouwd uit meerkernige cellen. De meeste hogere schimmels bijvoorbeeld, vormen op een vast stadium in hun levenscyclus tweekernige schimmeldraden.[41] Eencellige eukaryoten (protisten), zoals radiolariën en dinoflagellaten, kunnen ook van nature twee of meer kernen bevatten. Bijzonder aan deze organismen is dat de kernen elk een aparte afkomst hebben: één kern is van de dinoflagellaat en de andere kern van een symbiotische diatomee.[42] Verschillende groenwieren en roodwieren (zoals Chara en Griffithsia) vormen coenocytische cellen waarin meermaals kerndelingen plaatsvinden.[43]
Bij de mens zijn de cellen van de skeletspieren versmolten tot weefselstructuren die syncytia genoemd worden. In het syncytium kunnen de kernen vrij rondbewegen. Ze komen voornamelijk voor in het perifere gedeelte van de cellen, om zo ruimte te maken voor de myofibrillen (spiereenheden). Andere meerkernige cellen in het menselijk lichaam zijn de osteoclasten: speciale beencellen die nieuw botweefsel aanleggen. Bij ontstekingen en vermoedelijk ook bij de ontwikkeling van tumoren kan het voorkomen dat twee witte bloedcellen (monocyten en macrofagen) fuseren tot een meerkernige reuzencel.[44][45]
Evolutie
[bewerken | brontekst bewerken]Omdat de celkern de definiërende eigenschap is van eukaryoten, is de evolutionaire oorsprong ervan al lange tijd onderwerp van wetenschappelijke discussie. Er zijn verschillende hypothesen voorgelegd die het bestaan van de celkern in evolutionaire termen verklaren, maar geen ervan wordt algemeen geaccepteerd.[46] De ontwikkeling van de celkern en andere organellen, zoals het mitochondrion en de chloroplast, zijn cruciale stappen geweest in de evolutie van het leven.
Oorsprong van de celkern
[bewerken | brontekst bewerken]De oorsprong van de celkern kan verklaard worden door middel van het syntrofische model. Deze hypothese gaat uit van een symbiotische associatie tussen bacteriën en archaea, twee oude groepen organismen die van zichzelf geen celkern bevatten. Er wordt verondersteld dat de symbiose tot stand kwam toen ruwweg 2 miljard jaar geleden een voorouderlijk archaeon door een voorouderlijke bacterie werd opgenomen. Door vele generaties samen te leven verloor de archaeon zijn oorspronkelijke stofwisseling. De bacterie groeide en uiteindelijk veranderde de archaeon in een primitieve celkern: een compartiment met RNA en DNA dat een fysiologische eenheid vormde met de bacterie.[47][48]
Deze ontstaanshypothese van de celkern wordt ondersteund door verschillende argumenten. Ten eerste is het DNA en de genetische machinerie van eukaryoten zeer vergelijkbaar met dat van archaea.[49] Daarnaast zijn er bacteriën bekend die motiliteit vertonen, multicellulaire complexen kunnen vormen en eiwitten bezitten die overeenkomen met die van eukaryoten. Dit deed vermoeden dat eukaryotische cellen een bacteriële oorsprong hebben.[50]
Een tweede hypothese stelt dat eukaryotische cellen ontstaan zijn uit primitieve bacteriën die in structuur overeenkomen met tegenwoordige planctomyceten: bacteriën waarin membraancompartimenten zijn geëvolueerd.[51] In deze bacteriën komt een 'kernmembraan' voor waarin het bacterieel DNA en RNA afgeschermd worden van de rest van de cel. De cellulaire structuur van planctomyceten is een belangrijke aanwijzing voor een niet-symbiotische oorsprong van de celkern.[46]
Endosymbiose
[bewerken | brontekst bewerken]
Er zijn sterke aanwijzingen dat mitochondriën en plastiden van oorsprong zelfstandige prokaryoten waren die door een voorouderlijke cel werden opgenomen. In plaats van de opgenomen prokaryoot te verteren, maakte de gastheercel gebruik van de stofwisseling van de prokaryoot, waardoor de twee ingesteld samen gingen leven (endosymbiose). Na verloop van tijd verloor de endosymbiont een groot deel van zijn genetisch materiaal. Veel van zijn genen werden overgedragen naar de kern van de gastheercel,[l] een verschijnsel dat endosymbiotische genoverdracht wordt genoemd.[52]
Dankzij endosymbiose ontstonden onder meer de eerste eencellige roodwieren en groenwieren. Later in de evolutie ondergingen deze organismen een secundaire endosymbiose: ze werden zelf opgenomen door een andere eukaryotische cel. Een bepaalde groep wieren, de chlorarachniofyten, zou op deze manier ontstaan zijn. De chloroplasten van deze wieren zijn door vier membranen omgeven en bevatten zelfs nog een rudimentaire celkern, de zogenaamde nucleomorf.[53]
Ontdekkingsgeschiedenis
[bewerken | brontekst bewerken]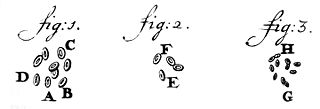
De celkern was een van de eerste celbiologische ontdekkingen. De oudst bekende tekening waarin cellen met een celkern zijn afgebeeld, werd gemaakt door Antoni van Leeuwenhoek (1632–1723) en dateert uit begin 18e eeuw. In een preparaat van rode bloedcellen uit zalmen[m] constateerde hij een "holte", de celkern.[54]
De celkern werd gedetailleerder beschreven door de Schotse botanicus Robert Brown in 1831. Brown bestudeerde de epidermiscellen van orchideeën onder de microscoop en zag daarbij in iedere cel een ondoorzichtig gebied, dat hij "areola" of "nucleus" noemde.[55] Bij zijn beschrijvingen gaf hij nog geen mogelijke functie van de celkern.

In 1838 kwam Matthias Schleiden op het idee dat de celkern een rol speelt bij het genereren van nieuwe cellen, waarbij hij de naam "cytoblast" (celbouwer) introduceerde. In zijn experimenten beweerde hij te zien dat nieuwe cellen zich rond deze "cytoblasten" verzamelden. Franz Meyen was een sterke tegenstander van deze opvatting. Hij geloofde dat celkernen zeldzaam waren, en verklaarde het vermenigvuldigen van cellen in termen van deling. Het idee dat cellen spontaan uit een "cytoblast" ontstonden was bovendien in tegenspraak met de latere celtheorie van Robert Remak (1852) en Rudolf Virchow (1855), die stelde dat elke cel uit een andere cel voortkwam ("Omnis cellula e cellula"). De functie van de celkern bleef lange tijd onduidelijk.[56]
Tussen 1877 en 1878 publiceerde Oscar Hertwig een reeks onderzoeken over de voortplanting van zee-egels, waaruit bleek dat de kern van de zaadcel tijdens de bevruchting versmelt met de kern van een eicel.[57] Voor het eerst werd gesuggereerd dat een individu zich ontwikkelt vanuit een (enkele) celkern, wat veel discussie teweegbracht. Hertwig bevestigde zijn bevindingen in andere diergroepen, waaronder amfibieën en weekdieren. In 1884 kwam ook Eduard Strasburger tot dezelfde conclusie voor de bevruchting in planten. Vanaf die periode werd erfelijkheid meer en meer met de celkern in verband gebracht.
De functie van de celkern als drager van genetische informatie werd pas duidelijk nadat de mitose werd ontdekt en deze nieuwe kennis aan het begin van de 20e eeuw samengevoegd werd met de wetten van Mendel (chromosoom-erfelijkheidstheorie).[56] Na de uitvinding van de elektronenmicroscoop en fluorescentiemicroscoop vanaf de jaren 30 konden structuur en dynamiek van de celkern in groot detail worden beschreven.
Zie ook
[bewerken | brontekst bewerken]Noten
- ↑ De naam eukaryoot is dan ook een verwijzing naar het hebben van een kern (eu-, "echt" en karyon, "kern"). Organismen die geen omsloten celkern hebben, worden prokaryoot genoemd (de bacteriën en archaea).
- ↑ a b Een zeer klein gedeelte van het genoom, het mitochondriaal DNA bevindt zich in de mitochondriën. Ook plastiden hebben hun eigen DNA, bijvoorbeeld het chloroplast-DNA.[14]
- ↑ Dit aantal varieert enorm per celtype, van een paar honderd kernporiën in gliacellen tot bijna 20.000 poriën in purkinjecellen (zenuwcellen van de hersenschors).[3]
- ↑ De kernlamina lijkt een evolutionaire aanpassing te zijn aan de beweeglijke levenswijze van dieren. Defecten in de ontwikkeling van het kernlamina leiden veelal tot spieraandoeningen.[9]
- ↑ Lamine-monomeren bevatten een herhalende alfa-helixstructuur waardoor ze gemakkelijk polymeriseren en zich in elkaar vastdraaien tot een touwachtige keten. Afbraak en opbouw van deze ketens wordt dynamisch gereguleerd.[11]
- ↑ Veel snoRNA's zijn introns die afkomstig zijn uit spliced messenger-RNA, coderende voor andere genen die betrokken zijn bij ribosoomfuncties.[18]
- ↑ Dit zijn afzettingen van het eiwit coiline.[21] Coilinecomplexen zijn minuscule, discrete pakketjes die in de celkern voorkomen binnen dichte distributiefoci.
- ↑ De lichaampjes danken hun naam Gemini (tweelingen) aan dit feit.[21]
- ↑ Een dergelijk reguleringsmechanisme komt bijvoorbeeld voor in de glycolyse. Hexokinase is een enzym dat verantwoordelijk is voor de eerste stap van glycolyse: de omzetting van glucose in glucose-6-fosfaat. Wanneer de concentraties van glucose-6-fosfaat te hoog worden, verplaatst een regulator-eiwit het hexokinase naar de kern, waar het een repressorcomplex vormt die de expressie van het hexokinase-gen stillegt.[31]
- ↑ GTP (guaninetrifosfaat) is voornamelijk aanwezig in de celkern, en GDP (guaninedifosfaat) in het cytoplasma. Dit concentratieverschil vormt een zogenaamd gradiënt.[3]
- ↑ De chromosomen verkeren op dit moment in een verdubbelde toestand. De twee kopieën, die elk de helft van het gerepliceerde chromosoom vormen, worden chromatiden genoemd. Tijdens de celdeling splitsen ze in tegenovergestelde richting uiteen. Zie deze figuur.
- ↑ Van de duizenden genen die in de oorspronkelijke prokaryoot voorkwamen, zijn er nog maar 10 tot 200 in tegenwoordige organellen over.[52]
- ↑ In tegenstelling tot rode bloedcellen van zoogdieren bevatten die van veel andere gewervelden wel een celkern.
Bronnen
- ↑ a b c (en) Rowat AC, Lammerding J, Herrmann H, Aebi U. (2008). Towards an integrated understanding of the structure and mechanics of the cell nucleus. Bioessays 30 (3): 226–236. PMID 18293361. DOI: 10.1002/bies.20720.
- ↑ a b (en) Rippe, K. (2007). Dynamic organization of the cell nucleus. Current Opinion in Genetics & Development 17 (5): 373-380. DOI: 10.1016/j.gde.2007.08.007.
- ↑ a b c d e f g (en) Alberts, B (2015). Molecular biology of the Cell, 6th. Garland Science, 649–657. ISBN 978-0815340720.
- ↑ (en) Clegg JS (1984). Properties and metabolism of the aqueous cytoplasm and its boundaries. The American Journal of Physiology 246 (2 Pt 2): R133-51. PMID 6364846. DOI: 10.1152/ajpregu.1984.246.2.R133.
- ↑ a b (en) Paine PL, Moore LC, Horowitz SB (1975). Nuclear envelope permeability. Nature 254 (5496): 109–14. PMID 1117994. DOI: 10.1038/254109a0.
- ↑ a b c (en) Lodish H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J (2004). Molecular Cell Biology, 5th. WH Freeman, New York. ISBN 978-0-7167-2672-2.
- ↑ (en) Shulga N, Mosammaparast N, Wozniak R, Goldfarb DS (2000). Yeast nucleoporins involved in passive nuclear envelope permeability. The Journal of Cell Biology 149 (5): 1027–38. PMID 10831607. PMC 2174828. DOI: 10.1083/jcb.149.5.1027.
- ↑ a b (en) Pemberton LF, Paschal BM (2005). Mechanisms of receptor-mediated nuclear import and nuclear export. Traffic 6 (3): 187–98. PMID 15702987. DOI: 10.1111/j.1600-0854.2005.00270.x.
- ↑ (en) Mans BJ, Anantharaman V, Aravind L, Koonin EV (2004). Comparative genomics, evolution and origins of the nuclear envelope and nuclear pore complex. Cell Cycle 3 (12): 1612–37. PMID 15611647. DOI: 10.4161/cc.3.12.1316.
- ↑ (en) Goldman RD, Gruenbaum Y, Moir RD, Shumaker DK, Spann TP (2002). Nuclear lamins: building blocks of nuclear architecture. Genes & Development 16 (5): 533–47. PMID 11877373. DOI: 10.1101/gad.960502.
- ↑ (en) Stuurman N, Heins S, Aebi U (1998). Nuclear lamins: their structure, assembly, and interactions. Journal of Structural Biology 122 (1-2): 42–66. PMID 9724605. DOI: 10.1006/jsbi.1998.3987.
- ↑ (en) Mounkes LC, Stewart CL (2004). Aging and nuclear organization: lamins and progeria. Current Opinion in Cell Biology 16 (3): 322–7. PMID 15145358. DOI: 10.1016/j.ceb.2004.03.009.
- ↑ (en) Schermelleh L, Carlton PM, Haase S (2008). Subdiffraction multicolor imaging of the nuclear periphery with 3D structured illumination microscopy. Science (journal) 320 (5881): 1332–6. PMID 18535242. DOI: 10.1126/science.1156947.
- ↑ (en) Lodish H, Berk A, Zipursky SL, et al. (2000). Molecular Cell Biology, 4th edition. W.H. Freeman, New York, "Organelle DNAs". ISBN 0-7167-3136-3. Gearchiveerd op 13 september 2021. Vrije toegang tot hoofdstuk.
- ↑ (en) Grigoryev SA, Bulynko YA, Popova EY (2006). The end adjusts the means: heterochromatin remodelling during terminal cell differentiation. Chromosome Research 14 (1): 53–69. PMID 16506096. DOI: 10.1007/s10577-005-1021-6.
- ↑ (en) Rothfield NF, Stollar BD (1967). The relation of immunoglobulin class, pattern of anti-nuclear antibody, and complement-fixing antibodies to DNA in sera from patients with systemic lupus erythematosus. The Journal of Clinical Investigation 46 (11): 1785–94. PMID 4168731. PMC 292929. DOI: 10.1172/JCI105669.
- ↑ (en) Barned S, Goodman AD, Mattson DH (1995). Frequency of anti-nuclear antibodies in multiple sclerosis. Neurology 45 (2): 384–5. PMID 7854544. DOI: 10.1212/WNL.45.2.384.
- ↑ a b (en) Hernandez-Verdun D (2006). Nucleolus: from structure to dynamics. Histochemistry and Cell Biology 125 (1-2): 127–37. PMID 16328431. DOI: 10.1007/s00418-005-0046-4.
- ↑ (en) Dundr M, Misteli T (2001). Functional architecture in the cell nucleus. The Biochemical Journal 356 (Pt 2): 297–310. PMID 11368755. PMC 1221839. DOI: 10.1042/0264-6021:3560297.
- ↑ (en) Goebel HH, Warlo I (1997). Nemaline myopathy with intranuclear rods--intranuclear rod myopathy. Neuromuscular Disorders 7 (1): 13–9. PMID 9132135. DOI: 10.1016/S0960-8966(96)00404-X.
- ↑ a b (en) Matera AG, Frey MR (1998). Coiled bodies and gems: Janus or gemini?. American Journal of Human Genetics 63 (2): 317–21. PMID 9683623. PMC 1377332. DOI: 10.1086/301992.
- ↑ Cioce M, Lamond AI (2005). Cajal bodies: a long history of discovery. Annual Review of Cell and Developmental Biology 21: 105–31. PMID 16212489. DOI: 10.1146/annurev.cellbio.20.010403.103738.
- ↑ (en) Navascues J, Berciano MT, Tucker KE, Lafarga M, Matera AG (June 2004). Targeting SMN to Cajal bodies and nuclear gems during neuritogenesis. Chromosoma 112 (8): 398–409. PMID 15164213. PMC 1592132. DOI: 10.1007/s00412-004-0285-5.
- ↑ (en) Matera AG (1998). Of coiled bodies, gems, and salmon. Journal of Cellular Biochemistry 70 (2): 181–92. PMID 9671224.
- ↑ (en) Lafarga M, Berciano MT, Pena E. (2002). Clastosome: a subtype of nuclear body enriched in 19S and 20S proteasomes, ubiquitin, and protein substrates of proteasome. Molecular Biology of the Cell 13 (8): 2771–82. PMID 12181345. PMC 117941. DOI: 10.1091/mbc.e02-03-0122.
- ↑ (en) Sampuda KM, Riley M, Boyd L (2017). Stress induced nuclear granules form in response to accumulation of misfolded proteins in Caenorhabditis elegans. BMC Cell Biology 18 (1): 18. PMID 28424053. PMC 5395811. DOI: 10.1186/s12860-017-0136-x.
- ↑ (en) Carmo-Fonseca M, Berciano MT, Lafarga M (2010). Orphan nuclear bodies. Cold Spring Harbor Perspectives in Biology 2 (9): a000703. PMID 20610547. PMC 2926751. DOI: 10.1101/cshperspect.a000703. Vrije toegang
- ↑ (en) Niall M. Adams & Paul S. Freemont (eds.) (2010). Advances in Nuclear Architecture. Springer Science & Business Media. DOI:10.1007/978-90-481-9899-3_1, "Nuclear Subdomains and Cancer". ISBN 9789048198993.
- ↑ (en) Alberts B, Johnson A, Lewis J, Morgan D, Raff M, Roberts K, Walter P. (2015). Molecular biology of the Cell, 6th. Garland Science, "Chapter 9: Visualizing Cells", 529–562. ISBN 978-0815340720. Vrije toegang tot hoofdstuk.
- ↑ (en) Devos DP, Gräf R, Field MC. (2014). Evolution of the nucleus. Current Opinion in Cell Biology 28: 8–15. PMID 24508984. PMC 4071446. DOI: 10.1016/j.ceb.2014.01.004.
- ↑ (en) Berg, J. (2015). Biochemistry, 8th edition. W. H. Freeman and Company, New York, 470-474. ISBN 978-1-4641-2610-9.
- ↑ (en) Browner WS, Kahn AJ, Ziv E, Reiner AP. (2004). The genetics of human longevity. Am J Med 117 (11): 851–60. PMID 15589490. DOI: 10.1016/j.amjmed.2004.06.033.
- ↑ (en) Berg, J.; Tymoczko, J.; Gatto, GJ. & Stryer, L. (2015). Biochemistry, 8th edition. W. H. Freeman and Company, New York, 871–872. ISBN 978-1-4641-2610-9..
- ↑ (en) Gagliardi D, Dziembowski A. (2018). 5′ and 3′ modifications controlling RNA degradation: from safeguards to executioners. Philos Trans R Soc Lond B Biol Sci. 373 (1762): 20180160. PMID 30397097. DOI: 10.1098/rstb.2018.0160.
- ↑ (en) Watson JD, Baker TA, Bell SP, Gann A, Levine M, Losick R (2004). Molecular Biology of the Gene, 5th. Peason Benjamin Cummings; CSHL Press., "Ch9–10". ISBN 978-0-8053-9603-4.
- ↑ a b (en) Lippincott-Schwartz, J. (2002). Cell biology: ripping up the nuclear envelope. Nature 416 (6876): 31–2. PMID 11882878. DOI: 10.1038/416031a.
- ↑ (en) Bruusgaard JC, Liestøl K, Ekmark M, Kollstad K & Gundersen K. (2003). Number and spatial distribution of nuclei in the muscle fibres of normal mice studied in vivo. The Journal of physiology 551 (2): 467–478. PMID 12813146. DOI: 10.1113/jphysiol.2003.045328. Vrije toegang
- ↑ (en) Gregory T.R. (2001). The Bigger the C-Value, the Larger the Cell: Genome Size and Red Blood Cell Size in Vertebrates. Blood Cells, Molecules and Diseases 27 (5): 830–843. PMID 11783946. DOI: 10.1006/bcmd.2001.0457.
- ↑ (en) Hutter KJ, Stöhr M (1982). Rapid detection of mutagen induced micronucleated erythrocytes by flow cytometry. Histochemistry 75 (3): 353–62. PMID 7141888. DOI: 10.1007/bf00496738.
- ↑ (en) Raven, P. (2013). Biology of Plants, 8th edition. W.H. Freeman Publishers, "23: Cells and tissues of the plant body", 547–552. ISBN 9781464113512. Gearchiveerd op 21 februari 2019.
- ↑ (en) Wallen RM, Perlin MH (2018). An Overview of the Function and Maintenance of Sexual Reproduction in Dikaryotic Fungi. Front Microbiol 9: 503. PMID 29619017. PMC 5871698. DOI: 10.3389/fmicb.2018.00503. Vrije toegang
- ↑ (en) Imanian B, Pombert JF, Dorrell RG, Burki F, Keeling PJ (2012). Tertiary endosymbiosis in two dinotoms has generated little change in the mitochondrial genomes of their dinoflagellate hosts and diatom endosymbionts. PLOS ONE 7 (8): e43763. PMID 22916303. PMC 3423374. DOI: 10.1371/journal.pone.0043763. Vrije toegang
- ↑ (en) Mine, I.; Menzel, D.; Okuda, K. (2008). Morphogenesis in giant-celled algae. Int. Rev. Cell Mol. Biol. International Review of Cell and Molecular Biology 266: 37–83. DOI: 10.1016/S1937-6448(07)66002-X.
- ↑ (en) McInnes A, Rennick DM (1988). Interleukin 4 induces cultured monocytes/macrophages to form giant multinucleated cells. The Journal of Experimental Medicine 167 (2): 598–611. PMID 3258008. PMC 2188835. DOI: 10.1084/jem.167.2.598.
- ↑ (en) Goldring SR, Roelke MS, Petrison KK, Bhan AK (1987). Human giant cell tumors of bone identification and characterization of cell types. The Journal of Clinical Investigation 79 (2): 483–91. PMID 3027126. PMC 424109. DOI: 10.1172/JCI112838.
- ↑ a b (en) Pennisi E (2004). Evolutionary biology. The birth of the nucleus. Science 305 (5685): 766–8. PMID 15297641. DOI: 10.1126/science.305.5685.766.
- ↑ (en) LóPez-García P., Moreira D. (2001). Symbiosis. Cellular Origin, Life in Extreme Habitats and Astrobiology. Springer, Dordrecht. DOI:10.1007/0-306-48173-1_8, "The Syntrophy Hypothesis for the Origin of Eukaryotes". ISBN 978-1-4020-0189-5.
- ↑ (en) Margulis L, Dolan MF, Guerrero R. (2000). The chimeric eukaryote: Origin of the nucleus from the karyomastigont in amitochondriate protists. PNAS 97 (13): 6954-6959. DOI: 10.1073/pnas.97.13.6954.
- ↑ (en) Horiike T, Hamada K, Kanaya S, Shinozawa T. (2001). Origin of eukaryotic cell nuclei by symbiosis of Archaea in Bacteria is revealed by homology-hit analysis. Nat Cell Biol. 3 (2): 210–214. PMID 11175755.
- ↑ (en) López-García P, Moreira D (2006). Selective forces for the origin of the eukaryotic nucleus. BioEssays 28 (5): 525–33. PMID 16615090. DOI: 10.1002/bies.20413.
- ↑ (en) Fuerst JA (2005). Intracellular compartmentation in planctomycetes. Annual Review of Microbiology 59: 299–328. PMID 15910279. DOI: 10.1146/annurev.micro.59.030804.121258.
- ↑ a b (en) Timmis, J., Ayliffe, M., Huang, C. et al. (2004). Endosymbiotic gene transfer: organelle genomes forge eukaryotic chromosomes. Nat Rev Genet 5 (2): 123–135. PMID 14735123. DOI: 10.1038/nrg1271.
- ↑ De Groef, B. & Roels, P. (2009). De wetenschap van het leven. Over eenheid in biologische diversiteit. Acco Leuven, Den Haag, 29–32. ISBN 978-90-334-7538-2.
- ↑ Leeuwenhoek, A. van: Opera Omnia, seu Arcana Naturae ope exactissimorum Microscopiorum detecta, experimentis variis comprobata, Epistolis ad varios illustres viros. J. Arnold et Delphis, A. Beman, Lugdinum Batavorum 1719–1730. Geciteerd volgens: Dieter Gerlach, Geschichte der Mikroskopie. (2009). Verlag Harri Deutsch, Frankfurt am Main, Duitsland, p. 89. ISBN 978-3-8171-1781-9.
- ↑ (en) Brown, Robert (1866). On the Organs and Mode of Fecundation of Orchidex and Asclepiadea. Miscellaneous Botanical Works I: 511–514.
- ↑ a b (de) Cremer, Thomas (1985). Von der Zellenlehre zur Chromosomentheorie. Springer Verlag, Berlin, Heidelberg, New York, Tokyo. ISBN 978-3-540-13987-4. Online versie
- ↑ (en) Clift D, Schuh M (2013). Restarting life: fertilization and the transition from meiosis to mitosis (Box 1). Nature Reviews Molecular Cell Biology 14 (9): 549–62. PMID 23942453. PMC 4021448. DOI: 10.1038/nrm3643.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Cell nucleus op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Literatuur
- Algemeen
- (en) Alberts, B. (2015). Molecular Biology of The Cell, 6th edition. Garland Science, New York. ISBN 978-0-8153-4464-3.
- (en) Kierszenbaum, A. & Tres, L. (2015). Histology and Cell Biology: An Introduction to Pathology, 4. Elsevier Health Sciences. ISBN 9780323313353.
- (en) Misteli T, Spector DL. (2011). The Nucleus. Cold Spring Harbor Laboratory Press. ISBN 9780879698942.
- (en) Pollard TD, Earnshaw WC, Lippincott-Schwartz J. (2007). Cell Biology. Elsevier Health Sciences, Philadelphia. ISBN 9781437700633.
- Prinsen, J. & van der Leij, F. (2015). De bouwstenen van het leven. Wageningen Academic Publishers. ISBN 978-90-8686-270-2.
- Steven A. & Lowe J. (1997). Histologie van de mens. Bohn Stafleu van Loghum, Houten. ISBN 9789031324354.
- Reviews
- (en) Lamond AI, Earnshaw WC (1998). Structure and function in the nucleus. Science 280 (5363): 547–53. DOI: 10.1126/science.280.5363.547.
- (en) Pederson T. (2011). The nucleus introduced. Cold Spring Harbor perspectives in biology, 3(5), a000521. DOI:10.1101/cshperspect.a000521
- (en) Lusk C. & King M. (2017). The nucleus: keeping it together by keeping it apart. Curr Opin Cell Biol. 44: 44-50. DOI: 10.1016/j.ceb.2017.02.001.
- (en) Dundr M, Misteli T. (2001). Functional architecture in the cell nucleus. Biochem. J. 356: 297–310. DOI: 10.1042/bj3560297.
Externe links
- Cellnucleus.com Informatie over de structuur en functie van de celkern, Universiteit van Alberta.




