Estryfikacja

Estryfikacja – reakcja chemiczna, w wyniku której powstają estry. Najczęściej zachodzi ona pomiędzy kwasami (głównie karboksylowymi) i alkoholami (szerzej: związkami zawierającymi grupę hydroksylową), niemniej możliwe i często stosowane są inne metody syntezy estrów np. z bezwodników czy chlorków kwasowych.
Reakcja estryfikacji z użyciem kwasu i alkoholu, której produktem ubocznym jest woda, jest zazwyczaj reakcją równowagową. Aby zapewnić jej wysoką wydajność, należy z układu reakcji usuwać przynajmniej jeden z produktów i jest nim najczęściej woda.
Estryfikacja Fischera
[edytuj | edytuj kod]Estryfikacja kwasu karboksylowego z alkoholem przy obecności katalitycznej ilości kwasu siarkowego lub innego silnego kwasu mineralnego została opisana przez Emila Fischera[1] i nazywana jest estryfikacją Fischera[2]. Aby uzyskać wysoką wydajność tego procesu, trzeba z układu reakcji na bieżąco usuwać przez destylację tworzący się ester, wodę lub oba naraz.
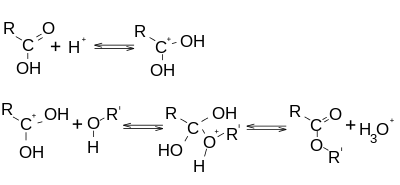
Przebieg katalizowanej silnym kwasem mineralnym estryfikacji Fischera wygląda następująco:
Na początku kation hydroniowy przyłącza się do atomu tlenu grupy karbonylowej. Następnie do powstałego karbokationu przyłącza się cząsteczka alkoholu. Wytworzony w ten sposób nietrwały związek rozkłada się z wydzieleniem kationu hydroniowego.
W analogiczny sposób zachodzi estryfikacja w przypadku kwasów nieorganicznych, np. estryfikacja gliceryny mieszaniną nitrującą, w wyniku której powstaje triazotan glicerolu (nitrogliceryna) lub estryfikacja alkoholi alifatycznych kwasem azotawym prowadząca do powstania azotynów alkilu.
Inne metody estryfikacji
[edytuj | edytuj kod]W wielu przypadkach, szczególnie dla aromatycznych kwasów karboksylowych estryfikację Fischera zastępuje się estryfikacją katalizowaną zasadowo. Jako katalizatory stosuje się najczęściej silnie zasadowe aminy (np. pirydynę). W przypadku estryfikacji katalizowanej, zasadowo istnieje też możliwość uniknięcia konieczności oddestylowywania produktów, poprzez zastosowanie dicyckloheksylokarbodiimidu DCC lub diizopropylokarbodiimidu DIC, który wiąże się ilościowo z wodą, zaś powstający N,N'-dicykloheksylomocznik wytrąca się z mieszaniny reakcyjnej jako osad[3].
W przemyśle reakcję estryfikacji prowadzi się często z użyciem halogenków acylowych lub bezwodników kwasowych, stosując technikę reakcji na granicy faz. Halogenek lub bezwodnik kwasowy umieszcza się w jednym rozpuszczalniku, zaś alkohol w drugim. Reakcja zachodzi wówczas na styku obu faz, dzięki czemu nie występuje konieczność przesuwania jej równowagi. W reakcji z użyciem halogenków produktem ubocznym nie jest woda, lecz halogenowodór, który można usuwać z układu reakcji poprzez obecność amin (np. trietyloamina, pirydyna, piperydyna) tworzących stałe halogenowodorki wypadające z układu reakcji w postaci osadu.
Wadą estryfikacji z użyciem halogenków kwasów karboksylowych jest ich wysoka cena i problem z utylizacją powstających halogenowodorków amin. Wadą stosowania bezwodników jest również ich wysoka cena oraz fakt, że reakcji efektywne używana jest tylko połowa jego masy, gdyż ubocznie tworzy się kwas karboksylowy, który w warunkach prowadzenia syntezy nie reaguje z alkoholem.
Przypisy
[edytuj | edytuj kod]- ↑ Fischer, Emil, Speier, Arthur. Darstellung der Ester. „Berichte der deutschen chemischen Gesellschaft”. 28 (3), s. 3252–3258, 1895. DOI: 10.1002/cber.189502803176.
- ↑ F.A. Carey, R.J. Sundberg: Advanced Organic Chemistry. Part A. Structure and Mechanisms. Springer, 2007, s. 664. ISBN 978-0-387-44897-8.
- ↑ Huczyński, Adam, Łowicki, Daniel, Brzezinski, Bogumil, Bartl, Franz. Spectroscopic, mass spectrometry, and semiempirical investigations of a new 2-(2-methoxyethoxy)ethyl ester of Monensin A and its complexes with monovalent cations. „Journal of Molecular Structure”. 879 (1–3), s. 14–24, 2008. DOI: 10.1016/j.molstruc.2007.08.004.