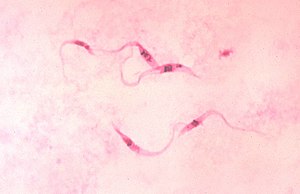
Doença de Chagas

| Doença de Chagas | |
|---|---|
| Imagem microscópica do Trypanosoma cruzi, o agente infeccioso da Doença de Chagas | |
| Especialidade | infecciologia, parasitologia |
| Classificação e recursos externos | |
| CID-10 | B57 |
| CID-9 | 086 |
| CID-11 | 1365585570 |
| DiseasesDB | 13415 |
| MedlinePlus | 001372 |
| eMedicine | med/327 |
| MeSH | D014355 |
Doença de Chagas ou Tripanossomíase americana é uma doença tropical parasitária causada pelo protozoário Trypanosoma cruzi e transmitida principalmente por insetos da subfamília Triatominae. Os sintomas mudam ao longo do curso da infecção. Na fase inicial, eles podem não estar presentes ou podem ser: febre, gânglios linfáticos aumentados, dor de cabeça e inchaço no local da mordida. Após 8-12 semanas, os indivíduos entram na fase crônica da doença e em 60-70% nunca desenvolvem outros sintomas. Os 30 a 40% restantes apresentam sintomas adicionais de 10 a 30 anos após a infecção inicial. Isto inclui o alargamento dos ventrículos do coração em 20 a 30% levando a insuficiência cardíaca. A dilatação do esôfago ou o alargamento do cólon também podem ocorrer em 10% das pessoas.
T. cruzi é transmitido para humanos e outros mamíferos principalmente pela via vetorial, geralmente através do contagio com as fezes de insetos hematófagos da subfamília Triatominae, popularmente denominados de "barbeiros" (p. ex.: Triatoma infestans). A doença pode também ser transmitida através de transfusão de sangue, transplante de órgãos, ingestão de alimentos contaminados com o parasita e da mãe para o feto. O diagnóstico precoce da doença é feito pela detecção do parasita no sangue, utilizando um microscópio. A forma crônica é diagnosticada pela presença de anticorpos para T. cruzi no sangue.
A prevenção ocorre principalmente pela eliminação dos barbeiros e em evitar suas picadas. Outros esforços de prevenção incluem a triagem do sangue usado para transfusões. Infecções precoces são tratáveis com a medicação benznidazol ou nifurtimox. Eles quase sempre resultam em cura se forem dados no início, no entanto, tornam-se menos eficazes quanto mais tempo se passa após contrair a doença. Quando utilizados na forma crônica podem retardar ou prevenir o desenvolvimento de sintomas em fase terminal. Benznidazol e nifurtimox causam efeitos colaterais temporários em até 40% das pessoas, incluindo doenças de pele, toxicidade cerebral e irritação do sistema digestório.
Estima-se que 7 000 000-8 000 000 pessoas, sobretudo no México, América Central e América do Sul, têm a doença de Chagas. Isso resulta em cerca de 12 500 mortes por ano desde 2006. A maioria das pessoas com a doença são indivíduos de baixa renda e grande parte das pessoas com a doença não percebem que estão infectadas. Movimentos populacionais em grande escala têm expandido as áreas onde os casos da doença de Chagas são encontrados e estes passaram a incluir muitos países da Europa e nos Estados Unidos. Essas áreas também têm visto um aumento nos casos até 2014. A doença foi descrita pela primeira vez em 1909 por Carlos Chagas, do qual recebeu o nome. Ela afeta mais de 150 outras espécie de animais. Atualmente, o médico e pesquisador hispano-brasileiro Pedro Albajar Viñas é o responsável pelo programa da OMS para o combate da doença de Chagas.[1]
Transmissão
[editar | editar código-fonte]
Nas áreas endêmicas, o principal mecanismo de transmissão é o vetorial, ou seja, através de um inseto vetor da subfamília Triatominae,[3] principalmente dos gêneros Triatoma, Rhodnius e Panstrongylus.[4] O inseto infecta-se com Trypanosoma cruzi ao alimentar-se de sangue de animais ou humanos contaminados. De hábitos noturnos, ele esconde-se durante o dia em fendas nas paredes e telhados, e emerge à noite, quando os habitantes estão dormindo. Por causa da tendência de picar a face das pessoas, o inseto é popularmente conhecido como "barbeiro" ou "chupão". Após a picada e a ingestão de sangue, ele defeca próximo ao local. O prurido intenso no local da picada ajuda as formas infectantes de T. cruzi (denominadas de tripomastigotas), nas fezes, a penetrarem na ferida da picadura, mas elas também podem penetrar por mucosas intactas, como a conjuntival.[3]
Uma vez dentro do hospedeiro, o tripomastigota invade as células próximas à inoculação, onde diferenciam-se em amastigotas intracelulares. Os amastigotas multiplicam-se por divisão binária e diferenciam-se em tripomastigotas, que são liberados na corrente sanguínea, infectando células de tecidos variados, e este ciclo então é repetido diversas vezes. As manifestações clínicas são resultado deste ciclo infeccioso. Os tripomastigotas circulantes não se replicam (diferente da tripanossomíase africana). E a replicação só recomeça quando os parasitas entram em outras células ou são ingeridos por outro vetor.[3]
Como doença caracteristicamente rural, tradicionalmente acomete pessoas de origem interiorana que habitam ou habitaram casas de baixa qualidade, onde o vetor facilmente se aloja e coloniza.[5] Vegetação densa (como a das florestas tropicais) e habitats urbanos não são ideais para o estabelecimento do ciclo de transmissão humano. No entanto, em regiões onde o habitat silvestre e sua fauna são reduzidos pela exploração econômica e ocupação humana, como em áreas recém-desmatadas, áreas de cultura da Leopoldinia piassaba e algumas partes da região amazônica, um ciclo de transmissão humano pode desenvolver-se quando os insetos procuram por novas fontes de alimentação.[6]
T. cruzi pode também ser transmitido por transfusões de sangue. Com a exceção dos derivados sanguíneos (como anticorpos fracionados), todos os componentes do sangue são infecciosos. O parasita permanece viável a 4 °C por até no mínimo 18 dias ou mais de 250 dias quando mantido em temperatura ambiente. Não está claro se o T. cruzi pode ser transmitido por meio de componentes do sangue congelados e descongelados.[7]
Outros modos de transmissão incluem o transplante de órgãos, amamentação e por exposição laboratorial acidental.[8] A doença de Chagas também pode ser passada de uma mulher grávida para seu filho (transmissão congênita) através da placenta, com uma prevalência entre as gestantes na América do Sul de 4 a 64,4%, com 0,1 a 7% destas mulheres transmitindo a infecção para os fetos. Essa forma de transmissão constitui um problema em ascensão na saúde pública e é uma das responsáveis pela urbanização dos casos e pela disseminação da doença em áreas não endêmicas.[9]
A transmissão oral, que antes era tida como uma via pouco frequente de infecção, atualmente é considerada como a via de transmissão prevalente, principalmente devido ao consumo de açaí.[10] Em 1991, trabalhadores rurais no estado da Paraíba, Brasil, foram infectados ao ingerir comida contaminada; transmissão também foi documentada pela ingestão de suco de açaí e caldo de cana infectados.[11][12][13][14][15] Um surto em 2007 em 103 crianças numa escola na Venezuela foi atribuído a contaminação do suco de goiaba.[16]
A doença de Chagas é um problema emergente na Europa, em vista de a grande maioria dos casos de infecção crônica serem assintomáticos e por causa de migrantes provenientes da América Latina.[17]
Patologia
[editar | editar código-fonte]Uma vez em contato com o parasita, seja qual for a via de infecção, o parasita se dissemina pelo sangue e vasos linfáticos na forma de tripomastigota, possuindo tropismo por células musculares (lisas, esqueléticas e especialmente cardíacas), células de Schwann, neurônios e macrófagos. Nessas células interagem com receptores de membrana e são internalizados, de modo que são encerrados no interior de um fagossomo. A partir da fusão desse compartimento com o lisossomo, contendo solução de pH ácido, os T. cruzi irão se diferenciar de sua forma infectante (tripomastigota) para a forma replicativa (amastigota) com perda do flagelo e escape do fagolisossomo para o citoplasma da célula infectada. Nela irão se replicar e posteriormente lisar a célula, retornando à forma tripomastigota e se disseminando. Esse ciclo por si só é relevante para se entender a etiologia dos sinais e sintomas clínicos da forma aguda, mas a forma crônica, devido à redução da parasitemia e sua replicação pelo controle exercido pelo sistema imune, é insuficiente para explicar os sinais e sintomas da fase crônica da doença.[18]
Vários estudos realizados até hoje já apontaram o papel da resposta imunológica tardia como provável responsável pelas manifestações cardíacas e coloesofágicas características da fase crônica. Essa resposta é de caráter autoimune, desencadeada por uma possível reação cruzada de antígenos do parasita com antígenos teciduais do hospedeiro, levando à agressão dessas mesmas células (sobretudo cardiomiócitos e neurônios) por citotoxicidade induzida por linfócitos T Cd8+ e anticorpos produzidos por plasmócitos autorreativos.[18]
Essa resposta autoimune, em conjunto com a lesão inicial provocada pelo parasita na fase aguda, leva à fibrose e/ou necrose em diversos tecidos corporais, sobretudo a musculatura cardíaca, e que se manifesta como arritmias, insuficiência cardíaca e tromboembolismos (sobretudo a alterações vasculares, estase sanguínea e lesão do endocárdio). Já o megaesôfago e o megacólon se devem à extensa desnervação do plexo mioentérico, sobretudo de neurônios parassimpáticos, o que acarreta na perda do peristaltismo e perda dos reflexos de abertura e fechamento do esfíncter esofágico inferior e do esfíncter anal interno. Com isso ocorre acúmulo de resíduos sólidos, levando à constipação e disfagia, e como resposta adaptativa a essa condição de estresse, as células musculares lisas do esôfago e do cólon sofrem hiperplasia e hipertrofia.[18]
Sinais e sintomas
[editar | editar código-fonte]

A doença apresenta dois estágios em seres humanos: uma fase aguda, que ocorre pouco tempo após a infecção, e uma fase crônica, que se desenvolve ao longo de muitos anos.[19]
A fase aguda ocorre durante as primeiras semanas ou meses desde a infecção. Geralmente, ela não é notada por ser assintomática ou por exibir apenas sintomas moderados que não são únicos da doença de Chagas. Os sintomas podem incluir febre, fadiga, dor no corpo, dor de cabeça, exantema, perda de apetite, diarreia e vômitos. Os sinais no exame físico podem incluir aumento moderado do fígado, do baço e de linfonodos, e inchaço no local da picada do barbeiro (o chagoma).[5]
O marcador mais conhecido da fase aguda da doença de Chagas é chamado sinal de Romaña. O sinal é caracterizado pelo edema das pálpebras do mesmo lado do rosto em que se localiza a ferida produzida pela picada do barbeiro, onde as fezes foram depositadas pelo inseto ou mesmo quando acidentalmente esfregadas para dentro do olho. Raramente, crianças e adultos morrem durante a fase aguda da doença, porém pode ocorrer uma grave inflamação do músculo cardíaco (miocardite) ou do cérebro (meningoencefalite), que colocam a vida em risco.[19] A fase aguda também pode ser grave em pessoas com o sistema imunitário comprometido.[3]
Se houver o desenvolvimento de sintomas durante a fase aguda, eles geralmente se resolvem espontaneamente dentro de três a oito semanas em aproximadamente 90% dos indivíduos.[20][21] Embora os sintomas se resolvam, mesmo com o tratamento, a infecção persiste e entra em sua fase crônica. Dos indivíduos com doença de Chagas crônica, 60–80% jamais desenvolverão sintomas (chamada doença de Chagas crônica indeterminada), enquanto 20–40% desenvolverão sintomas cardíacos e/ou problemas digestivos (chamada doença de Chagas crônica determinada). Em 10% dos indivíduos, a doença progride diretamente da fase aguda para uma forma clínica sintomática da doença de Chagas.[20][21]
A doença crônica sintomática (determinada) afeta vários sistemas do organismo, como nervoso, digestório e cardíaco. Cerca de dois terços das pessoas com sintomas crônicos apresentam danos ao coração, incluindo a miocardiopatia dilatada, que causa anormalidades do ritmo cardíaco e pode resultar em morte súbita. Cerca de um terço dos pacientes apresenta danos ao sistema digestório, resultando em dilatação do trato digestivo (megacólon e megaesôfago), acompanhados de grave emagrecimento. A dificuldade de deglutição (secundária à acalásia) pode ser o primeiro sintoma dos distúrbios digestivos e pode levar à desnutrição.[22]
20% a 50% dos indivíduos com envolvimento intestinal também exibem acometimento cardíaco.[22] Mais de 10% das pessoas cronicamente infectadas desenvolvem neurite, que resulta em alterações sensoriais e dos reflexos tendinosos. Casos isolados exibem envolvimento do sistema nervoso central, incluindo demência, confusão, encefalopatia crônica e perdas sensoriais e motoras.[23]
As manifestações clínicas da doença de Chagas se devem à morte de células nos tecidos envolvidos no ciclo infeccioso do parasita, induzindo a respostas inflamatórias, lesões celulares e fibrose. Por exemplo, o amastigoto intracelular destrói os neurônios intramurais do sistema nervoso autônomo do intestino e do coração, levando ao megacólon e aos aneurismas cardíacos, respectivamente. Se não tratada, a doença de Chagas pode ser fatal, na maioria dos casos por danificação do tecido muscular cardíaco.[22]
Há uma considerável variação geográfica na ocorrência das complicações cardíacas e de dilatações gastrointestinais em pacientes com doença de Chagas crônica. Na maioria dos países da América do Sul, as dilatações são quase tão comuns quanto o comprometimento cardíaco. Mas na Colômbia, Venezuela, América Central e México as dilatações são praticamente desconhecidas. Não se sabe se fatores do hospedeiro ou diferenças nas cepas do parasita causariam estes diferentes padrões de expressão clínica da doença.[19]
Diagnóstico
[editar | editar código-fonte]Na fase aguda, a presença do T. cruzi é diagnóstica para a doença de Chagas. Essa fase é caracterizada pela alta parasitemia, o que permite um diagnóstico parasitológico.[24] O parasita, em sua forma móvel (tripomastigota), pode ser detectado por exame microscópico direto no esfregaço de sangue fresco ou da camada leucocitária; ou pela preparação de esfregaços corados com Giemsa ou Leishman.[5] Microscopicamente, o T. cruzi pode ser confundido com o Trypanosoma rangeli, que não é patogênico para humanos.[25] O T. cruzi pode também ser isolado por cultura em meios específicos (por exemplo NNN, LIT), tanto na fase aguda como na crônica.[26][27]
A fase crônica da enfermidade é caracterizada pela baixa parasitemia e alto nível de anticorpos,[26] diminuindo a eficiência da identificação direta do parasita. Portanto, outros métodos são empregados durante esta fase, entre eles a hemoaglutinação indireta (IFA), Imunofluorescência indireta (IIF), enzyme-linked immunosorbent assay (ELISA), quimioluminescência, TESA-blot, reação em cadeia da polimerase (PCR), teste imunocromatográfico de fluxo lateral e pelo xenodiagnóstico,[24] onde percevejos não infectados são alimentados com o sangue do paciente suspeito, e então seus intestinos são examinados para a detecção do parasita.[28] Algumas vantagens e desvantagens podem ser citadas com relação aos métodos acima: o método PCR obtém alta sensibilidade e especificidade, mas é complexo e necessita laboratório e pessoal especializados; o método ELISA requer sensitização e leva horas para ser conduzido, além de requerer laboratório e pessoal profissional; o teste imunocromatográfico de fluxo lateral obtém resultado em questão de minutos, mas somente resultados qualitativos.[29]
Prevenção
[editar | editar código-fonte]
Atualmente, ainda não existe uma vacina contra a doença de Chagas[30] e a prevenção é, em geral, focada em eliminar o inseto vetor com a utilização de sprays e tintas contendo inseticidas (piretroides sintéticos) e em melhorar as condições de saneamento e habitação nas áreas rurais.[31] Para os moradores de áreas urbanas que vão passar temporadas, como férias ou acampamentos em regiões endêmicas, recomenda-se o uso de mosquiteiros. Algumas medidas de controle incluem:
- Uma armadilha contendo uma levedura pode ser utilizada para monitorar infestações de certas espécies de triatomíneos (Triatoma sordida, Triatoma brasiliensis, Triatoma pseudomaculata e Panstrongylus megistus);[32]
- Foram apresentados resultados promissores com o tratamento dos habitats de vetores com o fungo Beauveria bassiana;[33]
- Pode-se selecionar simbiontes do Triatominae através de paratransgênese.[34]
Inúmeras vacinas estão sendo testadas atualmente. A vacinação com o Trypanosoma rangeli tem produzido resultados positivos em modelos animais.[35] Mais recentemente, o potencial de vacinas com DNA para imunoterapia da doença de Chagas nas fases aguda e crônica tem sido testado por vários grupos de pesquisadores.[36]
Antigamente, a transfusão de sangue era o segundo modo mais comum de transmissão da doença de Chagas, mas, com o desenvolvimento e a implementação do controle dos bancos de sangue, houve uma redução dramática desse risco na última década. A doação de sangue em todos os países endêmicos da América Latina é submetida a uma pesquisa para Chagas. O teste está sendo expandido para outros países, como França, Espanha e Estados Unidos, que apresentam populações significativas ou em crescimento de imigrantes oriundos de áreas endêmicas.[37][38] Na Espanha, os doadores são avaliados com questionários para identificar indivíduos em risco de exposição à doença de Chagas para realizar a triagem.[38]
O Food and Drug Administration (FDA), órgão responsável pela aprovação de medicamentos nos EUA, aprovou dois testes para Chagas e publicou manuais que recomendam a triagem de qualquer sangue ou tecido doados.[38][39] Apesar de esses testes não serem obrigatórios nos EUA, estima-se que atualmente 75-90% das doações são testadas para Chagas, incluindo todas as unidades coletadas pela Cruz Vermelha Americana, o que corresponde a 40% de todo o suprimento sanguíneo do país.[39][40] O Chagas Biovigilance Network relata a incidência atual de produtos sanguíneos positivos para Chagas nos Estados Unidos, segundo o que é notificado pelos laboratórios utilizando os testes de rastreio aprovados pelo FDA em 2007.[41]
Tratamento
[editar | editar código-fonte]Na doença de Chagas, o tratamento é baseado em drogas antiparasitárias, para aniquilar o parasita, e no controle dos sinais e sintomas da infecção. O tratamento tem como objetivo reduzir a velocidade de acometimento do sistema nervoso parassimpático. Os distúrbios autonômicos provocados pela doença podem resultar, eventualmente, em megaesôfago, megacólon e miocardiopatia dilatada acelerada.[19] O tratamento logra prognóstico favorável quando a doença é diagnosticada e tratada na fase aguda, ao passo que a eficácia do tratamento diminui enquanto a doença progride.[29]
Medicamentos
[editar | editar código-fonte]O tratamento antiparasitário é mais eficiente no início da infecção, mas não está limitado à fase aguda. As drogas de escolha incluem os derivados azóis e nitro, tais como o benznidazol[42] e o nifurtimox. Ambos os agentes são limitados na sua capacidade de atingir a cura parasitológica (uma eliminação completa do T. cruzi do organismo), especialmente em pacientes cronicamente infectados, e já foram relatados casos de resistência a essas drogas.[43]
Estudos sugerem que o tratamento antiparasitário leva à cura parasitológica em cerca de 60–85% dos adultos e em mais de 90% das crianças tratadas no primeiro ano desde a fase aguda da doença de Chagas. Crianças (idades entre seis e 12 anos) com a doença crônica apresentam uma taxa de cura de aproximadamente 60% com o benznidazol. Apesar de a taxa de cura diminuir com o tempo em que o adulto está infectado com a doença de Chagas, o tratamento com benznidazol tem se mostrado capaz de postergar o início do acometimento cardíaco em adultos com doença de Chagas crônica.[20][22]
O tratamento da infecção crônica em mulheres antes ou durante a gravidez não parece reduzir a probabilidade de a doença ser transmitida para o bebê. Da mesma forma, não está claro se o tratamento profilático da infecção crônica é benéfico em pessoas que serão submetidas à imunossupressão (por exemplo, em recipientes de transplantes de órgãos) ou em pessoas que já são imunossuprimidas (por exemplo, em pessoas infectadas pelo vírus HIV).[22]
Complicações
[editar | editar código-fonte]No estado crônico, o tratamento envolve o controle das manifestações clínicas da doença. Por exemplo, marcapassos e medicamentos para arritmias (ritmo irregular dos batimentos cardíacos), como a amiodarona, podem ser muito benéficos para alguns pacientes com acometimento cardíaco crônico,[44] enquanto a cirurgia pode ser necessária no megacólon. Apesar disso, a doença não tem cura nessa fase. A doença crônica do coração causada pela doença de Chagas tem sido, hoje, uma indicação comum de transplante cardíaco. Até recentemente, contudo, a doença de Chagas era considerada uma contraindicação para esse procedimento, pois acreditava-se que o parasita poderia se aproveitar da imunossupressão após a cirurgia para retomar o acometimento do coração.[45]
Notou-se que as taxas de sobrevida em pacientes com Chagas poderiam aumentar significativamente com a administração de doses menores de drogas imunossupressoras, como a ciclosporina. Recentemente, tem sido demonstrado que o tratamento direto do músculo cardíaco com células-tronco através do transplante de células da medula óssea reduz dramaticamente os riscos de insuficiência cardíaca em pacientes com doença de Chagas.[46]
Epidemiologia
[editar | editar código-fonte]
A doença de Chagas afeta de 8 a 10 milhões de pessoas vivendo em países endêmicos da América Latina, com um adicional de 300 000–400 000 vivendo em países não endêmicos, como Espanha e Estados Unidos. Estima-se que anualmente ocorrem 41 200 novos casos em países endêmicos e que 14 400 crianças nascem com Chagas congênito todos os anos.[20][22] Em 2010, a doença resultou em aproximadamente 10 300 mortes em comparação com 9 300 em 1990.[47] Estima-se que a taxa de mortalidade anual seja em torno de 14 000.[48] No Brasil, estimativas recentes apontam que entre 2 e 3 milhões de pessoas estejam infectadas, e que ocorram cerca de 6 000 mortes anualmente.[49]
A doença está presente em 18 países do continente americano, estendendo-se do sul dos Estados Unidos até o norte da Argentina.[3] Chagas existe em duas zonas ecológicas diferentes. Na região do Cone Sul, o principal vetor vive no interior ou nos arredores das habitações humanas. Na América Central e no México, as principais espécies vetoras vivem tanto no interior das casas como em áreas desabitadas. Em ambas as zonas, a doença de Chagas ocorre quase exclusivamente em áreas rurais, onde os triatomíneos procriam e se alimentam das mais de 150 espécies de 24 famílias de mamíferos domésticos e selvagens, bem como de humanos, que servem de reservatórios naturais do T. cruzi.[50]
Embora os triatomíneos também se alimentem do sangue de pássaros, estes parecem ser imunes à infecção e não são considerados reservatórios do T. cruzi. Mesmo quando colônias de insetos são erradicadas de uma casa ou de abrigos de animais nas redondezas, eles podem re-emergir de plantas ou animais que fizeram parte do ciclo silvático (referente a animais selvagens) do parasita. Esse fenômeno é especialmente provável em zonas com vegetações abertas misturadas a agrupamentos de árvores e interpostas por habitações humanas.[51]
A doença de Chagas crônica permanece um importante problema de saúde pública em muitos países da América Latina, apesar das medidas efetivas de higiene e prevenção, como a eliminação dos insetos transmissores. Entretanto, algumas conquistas foram alcançadas na luta contra a doença na América Latina, como a redução de 72% da incidência da infecção em crianças e adultos jovens nos países da Iniciativa do Cone Sul e pelo menos três países (Uruguai em 1997, Chile em 1999 e Brasil em 2006) foram certificados como livres da transmissão vetorial e transfusional.[22][52][53] Na Argentina, a transmissão vetorial foi interrompida em 13 das 19 províncias endêmicas e progressos significativos têm sido feitos nesse sentido no Paraguai e na Bolívia.[52]
O monitoramento para T. cruzi do sangue doado e dos doadores de componentes sanguíneos e de órgãos sólidos, assim como dos doadores de células, tecidos e produtos de células e tecidos, é mandatório nos países endêmicos de Chagas e tem sido implementado.[54] Há, aproximadamente, 300 000 pessoas infectadas vivendo nos Estados Unidos, o que é provavelmente resultado da imigração de países latino-americanos.[55] Com o aumento dos movimentos populacionais, a possibilidade de transmissão por transfusão de sangue se tornou mais substancial nos Estados Unidos. A transfusão de sangue e produtos de tecidos é ativamente monitorada nos Estados Unidos, diminuindo, portanto, o risco.[56]
Histórico
[editar | editar código-fonte]
A enfermidade foi nomeada em homenagem ao médico e epidemiologista brasileiro Carlos Chagas, que foi o primeiro a descrevê-la em 1908-1909,[57][58][59] mas a doença não foi vista como um problema maior de saúde pública até a década de 1960 (a epidemia da doença de Chagas no Brasil na década de 1920 foi amplamente ignorada[60]). Chagas descobriu que o intestino dos triatomíneos abrigava um protozoário flagelado, uma nova espécie do gênero Trypanosoma, e foi capaz de provar experimentalmente que poderia ser transmitida a saguis do gênero Callithrix que haviam sido picados pelo inseto infectado. Estudos posteriores demonstraram que o macaco-de-cheiro (do gênero Saimiri) também era vulnerável à infecção.[61]
Diferente do que se observa habitualmente na pesquisa das doenças, Chagas descreveu primeiro o vetor, o parasita e seu ciclo vital para depois identificar a enfermidade à qual esses agentes estavam relacionados. Após tentativas frustradas, o T. cruzi foi identificado primeiro em um gato doméstico e depois no sangue de uma menina febril, na cidade de Lassance, Minas Gerais, mesmo local em que Chagas desenvolveu as primeiras pesquisas sobre a doença. A menina Berenice, de dois anos, foi o primeiro paciente com a doença de Chagas a ser descrito.[62] Chagas foi o único pesquisador, até o momento, que descreveu uma patologia por completo, descobrindo agente etiológico, vetor, hospedeiros, ciclo epidemiológico e as manifestações clínicas em humanos.[63][64]
Carlos Chagas descreveu o parasita patogênico como Trypanosoma cruzi em 1909,[57] em homenagem a Oswaldo Cruz, médico e epidemiologista brasileiro que combateu com sucesso epidemias de febre amarela, varíola e peste bubônica no Rio de Janeiro e outras cidades no começo do século XX. No mesmo ano recombinou o nome científico do parasita para Schizotrypanum cruzi, após reconhecer particularidades biológicas no ciclo reprodutivo que o diferenciava dos demais parasitas do gênero Trypanosoma.[65] Em 1912, Delanoë e Delanoë descreveram o parasita Pneumocystis carinii, demonstrando que as particularidades do ciclo reprodutivo observadas por Chagas eram na verdade de um outro parasita, fazendo com que Chagas retomasse o uso de Trypanosoma cruzi.[66][67]
Na Argentina, a doença é conhecida como mal de Chagas-Mazza, em homenagem ao médico argentino Salvador Mazza, que em 1926 começou a investigar a enfermidade e que nos anos seguintes tornou-se o principal pesquisador da doença naquele país.[68]
Existe a hipótese de que Charles Darwin possa ter sofrido de doença de Chagas, como resultado de uma picada do chamado "grande besouro preto dos Pampas" (vinchuca). O episódio foi relatado por ele em seu diário da viagem do Beagle como tendo ocorrido em março de 1835, a leste dos Andes, próximo a Mendoza. Darwin era jovem e gozava de boa saúde, mas seis meses depois adoeceu por quase um mês perto de Valparaíso, e em 1837, quase um ano depois de ter regressado à Inglaterra, começou a sofrer de um estranho grupo de sintomas, tornando-se incapacitado na maior parte do resto de sua vida. As tentativas de testar os restos mortais de Darwin na Abadia de Westminster usando técnicas modernas de PCR foram negadas pelo curador.[69]
Pesquisa
[editar | editar código-fonte]O desenvolvimento de uma vacina eficaz ou de novos medicamentos é crucial, e talvez o próximo passo mais esperado e importante na luta contra a doença de Chagas.[70] Diversos grupos de pesquisadores estão trabalhando no desenvolvimento de novas terapias, incluindo vacinas com base no DNA e em antígenos,[71][72][73] bem como em outras drogas anti-Trypanosoma, incluindo agentes químicos que inibem competitivamente a função de enzimas essenciais do T. cruzi.[70] Entre os novos compostos estão inibidores da prolina-racemase,[74] da esqualeno-sintase,[75] da cisteíno protease,[76] da purina,[77] do esterol 14-demetilase[78][79] e inibidores de enzimas envolvidas no metabolismo da tripanotiona.[80] Peptídeos antimicrobianos presentes na pele de sapos do gênero Phyllomedusa (P. oreades e P. distincta), denominados dermaseptinas, demonstraram atividade anti-Trypanosoma cruzi in vitro.[81] Outro estudo identificou que a lactona sesquiterpênica, dehidroleucodina (DhL), afeta o crescimento de Trypanosoma cruzi na fase epimastigota em meio de cultura.[82] Outro estudo in vitro demonstrou que componentes do chá verde (as catequinas) podem ser eficazes contra o T. cruzi.[83]
Experimentalmente, vários derivados de triazois têm sido testados, incluindo D0870,[84] posaconazol,[85] ravuconazol,[86] albaconazol[87] e TAK-187.[88] Entre eles, o posaconazol tem demonstrado resultados promissores no tratamento de ratos com infecções agudas e crônicas,[89] e foi proposto como candidato para ensaios clínicos com pacientes infectados.[90] Um grupo de pesquisadores da Faculdade de Medicina de Ribeirão Preto (FMRP/USP) vem desenvolvendo novas drogas experimentais fundamentadas na capacidade do óxido nítrico em matar o parasita.[91][92][93] Existem também diversas propostas do uso de extratos naturais como adjuvantes ao tratamento de pacientes da doença de Chagas. Por exemplo, pesquisadores brasileiros propuseram o uso de extratos de venenos de formigas ricos em alcaloides, ao observar forte inibição de diferentes fases de vida do parasito por experimentos in vitro. [94]
A doença de Chagas tem um sério impacto econômico no mundo. O custo do tratamento nos Estados Unidos é estimado em US$900 milhões anualmente, que inclui hospitalização e dispositivos médicos como marcapassos. O custo global é estimado em US$7 bilhões.[95]
Apesar de ser a principal enfermidade parasitária do Ocidente, a doença de Chagas é considerada uma das doenças negligenciadas. Embora seja prevenível e potencialmente erradicável, recursos insuficientes têm sido destinados à pesquisa e desenvolvimento de inovações diagnósticas e terapêuticas para Chagas.[96] Em resposta a essa crise, organizações do terceiro setor, como a Drugs for Neglected Diseases initiative, em colaboração com universidades e instituições públicas de biotecnologia, têm buscado o desenvolvimento de novos fármacos e vacinas para o controle da doença de Chagas.[97]
Cultura popular
[editar | editar código-fonte]Algumas menções à doença de Chagas podem ser encontradas na literatura não médica. Monteiro Lobato, em seu livro Mr. Slang e o Brasil, de 1927, denunciou "o monstruoso quadro patológico que [Carlos Chagas] entrevira na paisagem rude dos sertões à guisa de um círculo inédito de Dante".[62] Mais tarde, em 1972, em sua obra Teresa Batista Cansada de Guerra, o escritor baiano Jorge Amado enumera as moléstias da pobreza que assolam o sertão, dentre elas a doença de Chagas: "Se não fossem a bexiga, o tifo, a malária, o analfabetismo, a lepra, a doença de Chagas, a xistossomose, outras tantas meritórias pragas soltas no campo, como manter e ampliar os limites das fazendas do tamanho de países, como cultivar o medo, impor o respeito e explorar o povo devidamente?".[98]
Mesmo antes da descoberta da doença de Chagas, em 1872, o Visconde de Taunay faz em Inocência uma das mais famosas descrições da doença, que seria semelhante ao alargamento do esôfago observado em alguns pacientes com a forma crônica de Chagas. O chamado "mal do engasgo" é assim relatado por um dos personagens: "O que me 'aflege' mais é que há comidas então que não me passam pela goela... Boto os pedacinhos no bucho e parece-me que dentro tenho um bolo que me está a subir e descer pela garganta...".[99]
Ver também
[editar | editar código-fonte]
Referências
- ↑ Salabert, Eva. Entrevista de Salud al día. Dr. Pedro Albajar, WebConsultas Revista de Salud y bienestar (em espanhol)
- ↑ Costa, J.; Peterson, A.T.; Beard, C.B. (2002). «Ecologic niche modeling and differentiation of populations of Triatoma brasiliensis Neiva, 1911, the most important Chagas' disease vector in northeastern Brazil (Hemiptera, Reduviidae, Triatominae)». American Journal of Tropical Medicine and Hygiene. 67 (5): 516-520. PMID 12479554
- ↑ a b c d e «DPDx – Trypanosomiasis, American. Fact Sheet» (em inglês). Centers for Disease Control (CDC). Consultado em 25 de junho de 2014
- ↑ Costa, J.; Peterson, T.A. (2011). «Ecological niche modeling as a tool for understanding distributions and interactions of vectors, hosts, and etiologic agents of Chagas disease». Advances in Experimental Medicine and Biology. 710: 59-70. ISSN 0065-2598. doi:10.1007/978-1-4419-5638-5_7
- ↑ a b c Kashiwabara, Y.B.; Paiva, R.M.R.A.; Nakaoka, V.Y.; Silva, E.; Kashiwabara, T.G.B. (2010). «Doença de Chagas - Revisão de Literatura». Brazilian Journal of Surgery and Clinical Research. 4 (3): 49-52
- ↑ Teixeira, A.R.; Monteiro, P.S.; Rebelo, J.M. (2001). «Emerging Chagas disease: trophic network and cycle of transmission of Trypanosoma cruzi from palm trees in the Amazon». Emerging Infectious Diseases. 7 (1): 100–112. PMC 2631687
 . PMID 11266300. doi:10.3201/eid0701.010115
. PMID 11266300. doi:10.3201/eid0701.010115 - ↑ Wendel, S. (2010). «Transfusion transmitted Chagas disease: Is it really under control?». Acta Tropica. 115 (1–2): 28–34. PMID 20044970. doi:10.1016/j.actatropica.2009.12.006
- ↑ Wanderley, D.M.V.; Corrêa, F.M.A. (1995). «Epidemiology of Chagas' heart disease». São Paulo Medical Journal. 113 (2): 742-749. doi:10.1590/S1516-31801995000200003
- ↑ Diaz-Luján, C.; Triquell, M.F.; Mezzano, L.; Fretes, R.E. (2012). Zheng, J., ed. Recent Advances in Research on the Human Placenta. Shanghai: InTech. pp. 127–148. ISBN 978-953-51-0194-9
- ↑ «Açaí contaminado é o grande motivo por trás da Doença de Chagas». Veja Saúde. Consultado em 18 de dezembro de 2020
- ↑ Benchimol-Barbosa, P.R. (2006). «The oral transmission of Chagas' disease: an acute form of infection responsible for regional outbreaks». International Journal of Cardiology. 112 (1): 132–133. PMID 16600406. doi:10.1016/j.ijcard.2005.11.087
- ↑ Benchimol-Barbosa, P.R. (2010). «Trends on acute Chagas' disease transmitted by oral route in Brazil: steady increase in new cases and a concealed residual fluctuation». International Journal of Cardiology. 145 (3): 494–496. PMID 19762096. doi:10.1016/j.ijcard.2009.08.030
- ↑ «Chagas' disease (American trypanosomiasis) in southern Brazil» (PDF). CDR Weekly. 15 (13). 2005. Consultado em 25 de junho de 2014. Arquivado do original (PDF) em 16 de maio de 2008
- ↑ Shikanai-Yasuda, M.A.; Marcondes, C.B.; Guedes, L.A. (1991). «Possible oral transmission of acute Chagas' disease in Brazil». Revista do Instituto de Medicina Tropical de São Paulo. 33 (5): 351–357. PMID 1844961. doi:10.1590/S0036-46651991000500003
- ↑ da Silva Valente S.A.; de Costa Valente, V.; Neto, H.F. (1999). «Considerations on the epidemiology and transmission of Chagas disease in the Brazilian Amazon». Memórias do Instituto Oswaldo Cruz. 94 (Suppl 1): 395–398. PMID 10677763. doi:10.1590/s0074-02761999000700077
- ↑ de Noya, B.A.; Díaz-Bello, Z.; Colmenares, C.; Ruiz-Guevara, R.; Mauriello, L.; Zavala-Jaspe, R.; Suarez, J.A.; Abate, T.; Naranjo, L.; Paiva, M.; Rivas, L.; Castro, J.; Márques, J.; Mendoza, I.; Acquatella, H.; Torres, J.; Noya, O. (2010). «Large urban outbreak of orally acquired acute Chagas disease at a school in Caracas, Venezuela». The Journal of Infectious Diseases. 201 (9): 1308–1315. PMID 20307205. doi:10.1086/651608
- ↑ Roca, C.; Pinazo, M.J.; López-Chejade, P.; Bayó, J.; Posada, E.; López-Solana, J.; Gállego, M.; Portús, M.; Gascón, J.; Chagas-Clot Research Group (2011). «Chagas Disease among the Latin American Adult Population Attending in a Primary Care Center in Barcelona, Spain». PLoS Neglected Tropical Diseases. 5 (4): e1135. PMC 3082512
 . PMID 21572511. doi:10.1371/journal.pntd.0001135
. PMID 21572511. doi:10.1371/journal.pntd.0001135 - ↑ a b c Neto, Vicente Amato; et al. (2008). Parasitologia: uma abordagem clínica. Rio de Janeiro: Elsevier. pp. 130–132
- ↑ a b c d Guerrant, RL; Walker, DH; Weller, PF. «93: American Trypanosomiasis (Chagas' Disease)». Tropical Infectious Diseases Principles, Pathogens, & Practice 2 ed. Philadelphia: Churchill Livingstone Elsevier. pp. 1082–1094
- ↑ a b c d Rassi, A.; Rassi, A.; Marin-Neto, J.A. (2010). «Chagas disease». Lancet. 375 (9723): 1388–1402. PMID 20399979. doi:10.1016/S0140-6736(10)60061-X
- ↑ a b Bern, C.; Montgomery, S.P.; Herwaldt, B.L.; et al. (2007). «Evaluation and treatment of chagas disease in the United States: a systematic review». Journal of American Medical Association. 298 (18): 2171–2181. PMID 18000201. doi:10.1001/jama.298.18.2171
- ↑ a b c d e f g Kirchhoff, L.V. (17 de dezembro de 2010). «Chagas Disease (American Trypanosomiasis)» (em inglês). eMedicine. Consultado em 12 de maio de 2010
- ↑ Córdova, E.; Maiolo, E.; Corti, M.; Orduña, T. (2010). «Neurological manifestations of Chagas' disease». Neurolology Research. 32 (3): 238–244. PMID 20406601. doi:10.1179/016164110X12644252260637
- ↑ a b Pereira, P.C.M.; Navarro, E.C. (2013). «Challenges and perspectives of Chagas disease: a review». Journal of Venomous Animals and Toxins including Tropical Diseases. 19. 34 páginas. doi:10.1186/1678-9199-19-34
- ↑ Dias, J.C.P.; Coura, J.R. (1997). Clínica e terapêutica da doença de Chagas: uma abordagem prática para o clínico geral. Rio de Janeiro: FIOCRUZ. 486 páginas. ISBN 85-85676-31-0
- ↑ a b Portela-Lindoso, A.A.B.; Shikanai-Yasuda, M.A. (2003). «Doença de Chagas crônica: do xenodiagnóstico e hemocultura à reação em cadeia da polimerase». Revista de Saúde Pública. 37 (1): 107-115. doi:10.1590/S0034-89102003000100016
- ↑ Bezerra, R.C.; Neto, V.A. (2010). «Trypanosoma cruzi, hemocultura: uma abordagem prática». Revista Brasileira de Clínica Médica. 8 (3): 205-207
- ↑ Brumpt, E. (1914). «Le xénodiagnostic. Application au diagnostic de quelques infections parasitaires et en particulier à la trypanosomose de Chagas». Bulletin de la Société de Pathologie Exotique. 7 (10): 706–710
- ↑ a b Rocha-Gaso, María-Isabel; Villarreal-Gómez, Luis-Jesús; Beyssen, Denis; Sarry, Frédéric; Reyna, Marco-Antonio; Ibarra-Cerdeña, Carlos-Napoleón (15 de novembro de 2017). «Biosensors to Diagnose Chagas Disease: A Brief Review». Sensors (em inglês). 17 (11). 2629 páginas. doi:10.3390/s17112629
- ↑ «A killer that preys on the poor: Chagas disease» (PDF). Médecins Sans Frontières: Activity Report 2003/2004 (em inglês). Consultado em 29 de agosto de 2008. Arquivado do original (pdf) em 17 de dezembro de 2008
- ↑ Zerba, E.N. (1999). «Susceptibility and resistance to insecticides of Chagas disease vectors» (PDF). Medicina (Buenos Aires). 59 (Suppl 2): 41–46
- ↑ Pires, H.H.; Lazzari, C.R.; Diotaiuti, L.; Lorenzo, M.G. (2000). «Performance of yeast-baited traps with Triatoma sordida, Triatoma brasiliensis, Triatoma pseudomaculata, and Panstrongylus megistus in laboratory assays». Revista Panamena de Salud Publica. 7 (6): 384–388. PMID 10949899. doi:10.1590/S1020-49892000000600005
- ↑ Luz, C.; Rocha, L.F.; Nery, G.V.; Magalhães, B.P.; Tigano, M.S. (2004). «Activity of oil-formulated Beauveria bassiana against Triatoma sordida in peridomestic areas in Central Brazil». Memórias do Instituto Oswaldo Cruz. 99 (2): 211–8. PMID 15250478. doi:10.1590/S0074-02762004000200017
- ↑ Beard, C.B.; Cordon-Rosales, C.; Durvasula, R.V. (2002). «Bacterial symbionts of the Triatominae and their potential use in control of Chagas disease transmission». Annual Review of Entomology. 47: 123–141. PMID 11729071. doi:10.1146/annurev.ento.47.091201.145144
- ↑ Basso, B.; Moretti, E.; Fretes, R. (2008). «Vaccination with epimastigotes of different strains ofTrypanosoma rangeli protects mice against Trypanosoma cruzi infection». Memórias do Instituto Oswaldo Cruz. 103 (4): 370–374. PMID 18660992. doi:10.1590/S0074-02762008000400010
- ↑ Dumonteil, E.; Escobedo-Ortegon, J.; Reyes-Rodriguez, N.; Arjona-Torres, A.; Ramirez-Sierra, M. (2004). «Immunotherapy of Trypanosoma cruzi Infection with DNA Vaccines in Mice». Infection and Immunity. 72 (1): 46–53. PMC 343959
 . PMID 14688079. doi:10.1128/IAI.72.1.46-53.2004
. PMID 14688079. doi:10.1128/IAI.72.1.46-53.2004 - ↑ Castro, E. (2009). «Chagas' disease: lessons from routine donation testing». Transfus Med. 19 (1): 16–23. PMID 19302451. doi:10.1111/j.1365-3148.2009.00915.x
- ↑ a b c Gascon, J.; Bern, C.; Pinazo, M.J. (2009). «Chagas disease in Spain, the United States and other non-endemic countries». Acta Tropica. 115 (1–2): 22–27. PMID 19646412. doi:10.1016/j.actatropica.2009.07.019
- ↑ a b «FDA Approves Chagas Disease Screening Test for Blood, Tissue and Organ Donors» (em inglês). FDA. Consultado em 12 de maio de 2010
- ↑ «Infectious Disease Testing» (em inglês). American Red Cross. Consultado em 12 de maio de 2010. Arquivado do original em 18 de abril de 2010
- ↑ «Chagas' Biovigilance Network» (em inglês). Advancing Transfusion and Cellular Therapies Worldwide. Consultado em 12 de maio de 2010
- ↑ Garcia, S.; Ramos, C.O.; Senra, J.F. (2005). «Treatment with Benznidazole during the Chronic Phase of Experimental Chagas' Disease Decreases Cardiac Alterations». Antimicrobial Agents and Chemotherapy. 49 (4): 1521–1528. PMC 1068607
 . PMID 15793134. doi:10.1128/AAC.49.4.1521-1528.2005
. PMID 15793134. doi:10.1128/AAC.49.4.1521-1528.2005 - ↑ Buckner, F.S.; Wilson, A.J.; White, T.C.; Van Voorhis, W.C. (1998). «Induction of Resistance to Azole Drugs in Trypanosoma cruzi». Antimicrob Agents Chemother. 42 (12): 3245–3250. PMC 106029
 . PMID 9835521
. PMID 9835521 - ↑ Dubner, S.; Schapachnik, E.; Riera, A.R.; Valero, E. (2008). «Chagas disease: state-of-the-art of diagnosis and management». Cardiology Journal. 15 (6): 493–504. PMID 19039752
- ↑ Bocchi, E.A.; Bellotti, G.; Mocelin, A.O. (1996). «Heart transplantation for chronic Chagas' heart disease». The Annals of Thoracic Surgery. 61 (6): 1727–1733. PMID 8651775. doi:10.1016/0003-4975(96)00141-5
- ↑ Vilas-Boas, F.; Feitosa, G.S.; Soares, M.B. (2006). «Resultados iniciais do transplante de células de medula óssea para o miocárdio de pacientes com insuficiência cardíaca de etiologia chagásica». Arquivos Brasileiros de Cardiologia. 87 (2): 159–166. PMID 16951834. doi:10.1590/S0066-782X2006001500014
- ↑ Lozano, R.; et al. (2012). «Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010». Lancet. 380 (9859): 2095–2128. PMID 23245604. doi:10.1016/S0140-6736(12)61728-0
- ↑ World Health Organization (2010). «Chagas'disease(American trypanosomiasis) factsheet». The Weekly Epidemiological Record. 34: 334–336
- ↑ Martins-Melo, F.R.; Ramos Jr., A.N.; Alencar, C.H.; Lange, W.; Heukelbach, J. (2012d). «Mortality of Chagas'disease in Brazil: spatial patterns and definition of high-risk areas». Tropical Medicine & International Health. 17 (9): 1066–1075. doi:10.1111/j.1365-3156.2012.03043.x
- ↑ Morel, C.M.; Lazdins, J. (2003). «Chagas disease». Nature Reviews Microbiology. 1 (1): 14–15. PMID 15040175. doi:10.1038/nrmicro735
- ↑ Pinto-Dias, J.C. (1992). «Epidemiology of Chagas disease». In: Wendel S, Brener Z, Camargo ME, Rassi A (eds.). Chagas Disease – American Trypanosomiasis: its impact on transfusion and clinical medicine. ISBT Brazil '92. XXII Congress of the International Society of Blood Transfusion. XX Brazilian Congress of Hematology. Extraordinary Congress of the Brazilian College of Hematology. São Paulo: Editorial ISBT Brazil. Consultado em 11 de setembro de 2008
- ↑ a b «The Southern Cone Initiative: an update». Special Programme for Research and Training in Tropical Diseases (TDR) (em inglês). WHO. 2004. Consultado em 29 de agosto de 2008. Arquivado do original em 22 de setembro de 2009
- ↑ Massad, E. (2008). «The elimination of Chagas' disease from Brazil». Epidemiology and Infection. 136 (9): 1153–1164. PMC 2870925
 . PMID 18053273. doi:10.1017/S0950268807009879
. PMID 18053273. doi:10.1017/S0950268807009879 - ↑ Castro, E. (2009). «Chagas' disease: lessons from routine donation testing». Transfusion Medicine. 19 (1): 16–23. PMID 19302451. doi:10.1111/j.1365-3148.2009.00915.x
- ↑ «Medical Encyclopedia: Chagas disease» (em inglês). National Institutes of Health. Consultado em 11 de setembro de 2008
- ↑ Kirchhoff, L.V. (1993). «American trypanosomiasis (Chagas' disease) – a tropical disease now in the United States». The New England Journal of Medicine. 329 (9): 639–644. PMID 8341339. doi:10.1056/NEJM199308263290909
- ↑ a b Chagas, C. (1909). «Neue Trypanosomen». Vorläufige Mitteilung Arch. Schiff. Tropenhyg. 13: 120–122
- ↑ Redhead, S.A.; Cushion, M.T.; Frenkel, J.K.; Stringer, J.R. (2006). «Pneumocystis and Trypanosoma cruzi: nomenclature and typifications». Journal of Eukaryotic Microbiology. 53 (1): 2–11. PMID 16441572. doi:10.1111/j.1550-7408.2005.00072.x
- ↑ Kropf, S.P.; Sá, M.R. «The discovery of Trypanosoma cruzi and Chagas disease (1908–1909): tropical medicine in Brazil». História, Ciências Saúde-Manguinhos. 16 (Suppl 1): 13–34. PMID 20027916
- ↑ Coutinho, M. (junho de 1999). «Review of Historical Aspects of American Trypanosomiasis (Chagas' Disease) by Matthias Perleth». Isis. 90 (2). 397 páginas. JSTOR 237120. doi:10.1086/384393
- ↑ Hulsebos, L.H.; Choromanski, L.; Kuhn, R.E. (1989). «The effect of interleukin-2 on parasitemia and myocarditis in experimental Chagas' disease». Journal of Protozoology. 36 (3): 293–298. PMID 2499678
- ↑ a b Kropf, S.P (2009). Doença de Chagas, Doença do Brasil : ciência, saúde e nação, 1906-1962. Rio de Janeiro: Editora FIOCRUZ. ISBN 9788575411759. doi:10.7476/9788575413159
- ↑ «History of Chagas disease» (em inglês). Chagasdisease.org. Consultado em 25 de junho de 2014
- ↑ Kropf, S.Pe.; Sá, M.R. (2009). «The discovery of Trypanosoma cruzi and Chagas disease (1908-1909): tropical medicine in Brazil». História, Ciências, Saúde-Manguinhos. 16 (Suppl. 1): 13-34. doi:10.1590/S0104-59702009000500002
- ↑ Chagas, C. (1909). «Nova tripanozomiase humana: Estudos sobre a morfolojia e o ciclo evolutivo do Schizotrypanum cruzi n. gen., n. sp., ajente etiolojico de nova entidade morbida do homem». Memórias do Instituto Oswaldo Cruz. 1 (2): 159–218. ISSN 0074-0276. doi:10.1590/S0074-02761909000200008
- ↑ Delanoë, P.; Delanoë, M. (1912). «Sur les rapports des kystes de Carini du poumon des rats avec le Trypanosoma lewisi». Comptes rendus de l'Academie des sciences. 155: 658–661
- ↑ Chagas, C. (1913). «Revisão do cyclo evolutivo do "Trypanosoma Cruzi"». Brazil-Médico. 27. 225 páginas
- ↑ «Enfermedad de Chagas – Mazza» (em espanhol). Asociación Lucha Contra el Mal de Chagas. Consultado em 15 de setembro de 2011. Arquivado do original em 16 de setembro de 2011
- ↑ Adler, D. (1989). «Darwin's Illness». Israel Journal of Medical Science. 25 (4): 218–221. PMID 2496051
- ↑ a b Bonney, K.M (2014). «Chagas disease in the 21st Century: a public health success or an emerging threat?». Parasite. 21. 11 páginas. doi:10.1051/parasite/2014012
- ↑ Dumonteil, E.; Escobedo-Ortegon, J.; Reyes-Rodriguez, N.; Arjona-Torres, A.; Ramirez-Sierra, M.J (2004). «Immunotherapy of Trypanosoma cruzi infection with DNA vaccines in mice». Infection and Immunity. 72 (1): 46-53. doi:10.1128/IAI.72.1.46-53.2004
- ↑ Zapata-Estrella, H.; Hummel-Newell, C.; Sanchez-Burgos, G.; Escobedo-Ortegon, J.; Ramirez-Sierra, M.J.; Arjona-Torres, A.; Dumonteil, E (2006). «Control of Trypanosoma cruzi infection and changes in T-cell populations induced by a therapeutic DNA vaccine in mice». Immunology Letters. 103 (2): 186-191. doi:10.1016/j.imlet.2005.11.015
- ↑ Gupta, S.; Garg, N.J (2013). «TcVac3 induced control of Trypanosoma cruzi infection and chronic myocarditis in mice». PLoS One. 8 (3): e59434. doi:10.1371/journal.pone.0059434
- ↑ Berneman, A.; Montout, L.; Goyard, S.; Chamond, N.; Cosson, A.; d'Archivio, S.; Gouault, N.; Uriac, P.; Blondel, A.; Minoprio, P (2013). «Combined approaches for drug design points the way to novel proline racemase inhibitor candidates to fight Chagas' disease». PLoS One. 8 (4): e60955. doi:10.1371/journal.pone.0060955
- ↑ Urbina, J.A.; Concepcion, J.L.; Rangel, S.; Visbal, G.; Lira, R (2002). «Squalene synthase as a chemotherapeutic target in Trypanosoma cruzi and Leishmania mexicana». Molecular and Biochemical Parasitology. 125 (1–2): 35–45. PMID 12467972. doi:10.1016/S0166-6851(02)00206-2
- ↑ Engel, J.C.; Doyle, P.S.; Hsieh, I.; McKerrow, J.H. (1998). «Cysteine Protease Inhibitors Cure an Experimental Trypanosoma cruzi Infection». The Journal of Experimental Medicine. 188 (4): 725–734. PMC 2213346
 . PMID 9705954. doi:10.1084/jem.188.4.725
. PMID 9705954. doi:10.1084/jem.188.4.725 - ↑ Berg, M.; Van der Veken, P.; Goeminne, A.; Haemers, A.; Augustyns, K (2010). «Inhibitors of the purine salvage pathway: a valuable approach for antiprotozoal chemotherapy?». Current Medical Chemistry. 17 (23): 2456-2481. doi:10.2174/092986710791556023
- ↑ Buckner, F.S (2008). «Sterol 14-demethylase inhibitors for Trypanosoma cruzi infections». Advances In Experimental Medicine And Biology. 625: 61-80. doi:10.1007/978-0-387-77570-8_6
- ↑ Villalta, F.; Dobish, M.C.; Nde, P.N.; Kleshchenko, Y.Y.; Hargrove, T.Y.; Johnson, C.A.; Waterman, M.R.; Johnston, J.N.; Lepesheva, G.I. (2013). «VNI cures acute and chronic experimental Chagas disease». The Journal of infectious diseases. 208 (3): 504–511. PMC 3698996
 . PMID 23372180. doi:10.1093/infdis/jit042
. PMID 23372180. doi:10.1093/infdis/jit042 - ↑ Fairlamb, A.H.; Cerami, A (1992). «Metabolism and functions of trypanothione in the Kinetoplastida». Annual Reviews Microbiology. 46: 695–729. PMID 1444271. doi:10.1146/annurev.mi.46.100192.003403
- ↑ Brand, G.D.; Leite, J.R.; Silva, L.P. (2002). «Dermaseptins from Phyllomedusa oreades and Phyllomedusa distincta. Anti-Trypanosoma cruzi activity without cytotoxicity to mammalian cells». Journal of Biological Chemistry. 277 (51): 49332–49340. PMID 12379643. doi:10.1074/jbc.M209289200
- ↑ Brengio, S.D.; Belmonte, S.A.; Guerreiro, E.; Giordano, O.S.; Pietrobon, E.O.; Sosa, M.A. (2000). «The sesquiterpene lactone dehydroleucodine (DhL) affects the growth of cultured epimastigotes of Trypanosoma cruzi». J Parasitol. 86 (2): 407–412. ISSN 0022-3395. PMID 10780563. doi:10.1645/0022-3395(2000)086[0407:TSLDDA]2.0.CO;2
- ↑ Paveto, C.; Güida, M.C.; Esteva, M.I.; Martino, V.; Coussio, J.; Flawiá, M.M.; Torres, H.N. (2004). «Anti-Trypanosoma cruzi Activity of Green Tea (Camellia sinensis) Catechins». Antimicrobial Agents and Chemotherapy. 48 (1): 69–74. PMC 310206
 . PMID 14693520. doi:10.1128/AAC.48.1.69-74.2004
. PMID 14693520. doi:10.1128/AAC.48.1.69-74.2004 - ↑ Molina, J.; Brener, Z.; Romanha, A.J.; Urbina, J.A (2000). «In vivo activity of the bis-triazole D0870 against drug-susceptible and drug-resistant strains of the protozoan parasite Trypanosoma cruzi». Journal of Antimicrobial Chemotherapy. 46 (1): 137-140. doi:10.1093/jac/46.1.137
- ↑ Molina, J.; Martins-Filho, O.; Brener, Z.; Romanha, A.J.; Loebenberg, D.; Urbina, J.A (2000). «Activities of the triazole derivative SCH 56592 (posaconazole) against drug-resistant strains of the protozoan parasite Trypanosoma (Schizotrypanum) cruzi in immunocompetent and immunosuppressed murine hosts». Antimicrobial Agents and Chemotherapy. 44 (1): 150-155. PMC 89642

- ↑ Urbina, J.A.; Payares, G.; Sanoja, C.; Lira, R.; Romanha, A.J (2003). «In vitro and in vivo activities of ravuconazole on Trypanosoma cruzi, the causative agent of Chagas disease». International Journal of Antimicrobial Agents. 21 (1): 27-38. doi:10.1016/S0924-8579(02)00273-X
- ↑ Guedes, P.M.; Urbina, J.A.; de Lana, M.; Afonso, L.C.; Veloso, V.M.; Tafuri, W.L.; Machado-Coelho, G.L.; Chiari, E.; Bahia, M.T (2004). «Activity of the new triazole derivative albaconazole against Trypanosoma (Schizotrypanum) cruzi in dog hosts». Antimicrobial Agents and Chemotherapy. 48 (11): 4286-4292. doi:10.1128/AAC.48.11.4286-4292.2004
- ↑ Urbina, J.A.; Payares, G.; Sanoja, C.; Molina, J.; Lira, R.; Brener, Z.; Romanha, A.J (2003). «Parasitological cure of acute and chronic experimental Chagas disease using the long-acting experimental triazole TAK-187. Activity against drug-resistant Trypanosoma cruzi strains». International Journal of Antimicrobial Agents. 21 (1): 39-48. doi:10.1016/S0924-8579(02)00274-1
- ↑ Ribeiro, I.; Sevcsik, A.-M.; Alves, F.; Diap, G.; Don, R.; Harhay, M.O.; Chang, S.; Pecoul, B (2009). «New, Improved Treatments for Chagas Disease: From the R&D Pipeline to the Patients». PLoS Neglected Tropical Diseases. 3 (7): e484. doi:10.1371/journal.pntd.0000484
- ↑ Urbina, J.A.; Docampo, R (2003). «Review Specific chemotherapy of Chagas disease: controversies and advances». Trends in Parasitology. 19 (11): 495-501. doi:10.1016/j.pt.2003.09.001
- ↑ Machado, F.S.; Tanowitz, H.B.; Texeira, M.M (2010). «New drugs for neglected infectious diseases: Chagas' disease». British Journal of Pharmacology. 160 (2): 258–259. doi:10.1111/j.1476-5381.2010.00662.x
- ↑ Guedes, P.M.M.; Oliveira, F.S.; Gutierrez, F.R.; da Silva, G.K.; Rodrigues, G.J.; Bendhack, L.M.; Franco, D.W.; Do Valle Matta, M.A.; Zamboni, D.S.; da Silva, R.S.; Silva, J.S (2010). «Nitric oxide donor trans-[RuCl([15]aneN4)NO]2+ as a possible therapeutic approach for Chagas' disease». British Journal of Pharmacology. 160 (2): 270–282. doi:10.1111/j.1476-5381.2009.00576.x
- ↑ Silva, J.J.N.; Guedes, P.M.M.; Zottis, A.; Balliano, T.L.; Silva, F.O.N.; Lopes, L.G.F.; Ellena, J.; Oliva, G.; Andricopulo, A.D.; Franco, D.W (2010). «Novel ruthenium complexes as potential drugs for Chagas's disease: enzyme inhibition and in vitro/in vivo trypanocidal activity». British Journal of Pharmacology. 160 (2): 260–269. doi:10.1111/j.1476-5381.2009.00524.x
- ↑ Silva, Rafael C. M. Costa; Fox, Eduardo G. P.; Gomes, Fabio M.; Feijó, Daniel F.; Ramos, Isabela; Koeller, Carolina M.; Costa, Tatiana F. R.; Rodrigues, Nathalia S.; Lima, Ana P. (dezembro de 2020). «Venom alkaloids against Chagas disease parasite: search for effective therapies». Scientific Reports (em inglês). 10 (1). 10642 páginas. ISSN 2045-2322. doi:10.1038/s41598-020-67324-8
- ↑ Schmuñis, G (2013). «Status of and cost of Chagas disease worldwide». The Lancet infectious diseases. 13 (4): 283–284. PMID 23395247. doi:10.1016/S1473-3099(13)70032-X
- ↑ Feasey, N.; Wansbrough-Jones, M.; Mabey, D.C.W.; Solomon, A.W (2009). «Neglected Tropical Diseases». British Medical Bulletin. 93 (1). 179 páginas. doi:10.1093/bmb/ldp046
- ↑ Hotez, P.J.; Dumonteil, E.; Woc-Colburn, L.; Serpa, J.A.; Bezek, S.; et al. (2012). «Chagas disease: 'The new HIV/AIDS of the Americas'». PLoS Neglected Tropical Diseases. 6 (5): e1498. PMC 3362306
 . PMID 22666504. doi:10.1371/journal.pntd.0001498
. PMID 22666504. doi:10.1371/journal.pntd.0001498 - ↑ Amado, J (1972). Tereza Batista Cansada de Guerra 1 ed. São Paulo: Livraria Martins Editora. p. 162
- ↑ Gurgel, C.B.M.; Magdalena, C.V.; Prioli, L.F (2009). «A tripanossomíase americana antes de Carlos Chagas». Cad Saúde Colet. 17 (4): 827-39
Leitura adicional
[editar | editar código-fonte]- Brener, Z.; Andrade, Z.; Barral-Neto, M. (eds.). Trypanosoma cruzi e doença de Chagas, 2.ª edição. Rio de Janeiro: Guanabara Koogan Ed., 2000.
- Dias, J.C.P.; Coura, J.R. (eds.). Clínica e Terapêutica da Doença de Chagas: um manual para o clínico geral. Rio de Janeiro: Editora Fiocruz, 1997.
- Gontijo, E.D.; Rocha, M.C. (eds.).Manejo clínico em doença de Chagas. Brasília: Fundação Nacional de Saúde, Ministério da Saúde, 1998.
- Storino, R.; Milei, J. (eds.).Enfermedad de Chagas. Buenos Aires: Doyma Argentina, 1994.
Ligações externas
[editar | editar código-fonte]- «Médicos sem Fronteiras: A descoberta da doença de Chagas está fazendo 100 anos» 🔗
- «Programa Integrado da Doença de Chagas»
- «"Doença de Chagas" material do curso de Medicina da Universidade Federal Fluminense»
- «UOL: Doença de Chagas é tão antiga nas Américas quanto a presença humana»
- «Biblioteca Virtual Carlos Chagas: A doença de Chagas»
- «Exposição Virtual Carlos Chagas: A doença de Chagas»
- «Chagas information at the U.S. Centers for Disease Control» 🔗 (em inglês)
- «Chagas information from the Drugs for Neglected Diseases initiative» 🔗 (em inglês)
- «Norma Andrews's seminar: Trypanosoma cruzi and Chagas Disease» (em inglês)
- «UNHCO site on Chagas Disease» (em inglês)