Вроджений гіпотиреоз

| Вроджений гіпотиреоз | |
|---|---|
 | |
| Спеціальність | ендокринологія |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 5A00.0 |
| МКХ-10 | E00, E03.0, E03.1 |
| МКХ-9 | 243 |
| DiseasesDB | 6612 |
| MeSH | D003409 |
| | |
Вроджений гіпотиреоз — захворювання, викликане зниженням або повним випадінням функції щитоподібної залози, яке існує при народженні.
Вроджений гіпотиреоз являє собою особливу форму гіпофункції щитоподібної залози. Вона вражає пацієнтів у той період розвитку, коли вся нервова система є дуже чутливою і може пошкодитися через тривалу нестачу гормонів щитоподібної залози. Якщо безпосередньо після народження не виявити порушення і не скоригувати його, то це приведе до розвитку кретинізму.
У більшості випадків спричиняється зниження функції щитоподібної залози через порушення розвитку органа в ембріональному періоді (агенезія чи дисгенезія). При цьому розвивається повна функціональна неспроможність тканин щитоподібної залози або ж вона занадто мала. Причина цих пошкоджень невідома. Лише в одиничних випадках змогли встановити генні мутації, які відігравали певну роль для розвитку щитоподібної залози, серед них FOXE1, що кодує тиреоїдний фактор транскрипції 2 (TTF-2) і PAX8-ген, що кодує Paired-Box-Protein 8 (PAX-8).[1]
Поряд з цим бувають порушення синтезу гормонів щитоподібною залозою, яка закладена у всьому іншому правильно. Вроджені порушення синтезу тироксину успадковуються по аутосомно-рецесивному типу, дефекти рецепторів до гормонів щитоподібної залози успадковуються аутосомно-домінантно. В загальному близько 85% всіх вроджених гіпофункцій щитоподібної залози є спорадичними, інші 15% — спадково обумовленими.[1]
В окремих випадках гіпофункція має перехідну (тимчасову) природу. Такі випадки спричиняються попаданням через плаценту до дитини медикаментів чи материнських блокуючих антитіл, дифіцитом йоду чи навпаки надмірним його споживанням. Порушення гіпоталамо-гіпофізарної системи — так звана центральна, вторинна чи третинна гіпофункція — зі зниженою продукцією тиреотропного гормону (ТТГ) чи тиреотропін-рилізінг-гормону (ТРГ, тиреоліберин) є екстремально рідкісним явищем, однак вони не виявляються при звичайному скринінговому обстеженні.[2]
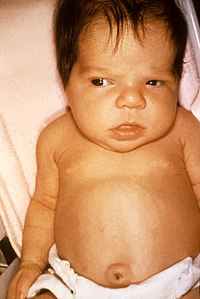
Хоча гормони щитоподібної залози мають дуже велике значення для розвитку майже всіх систем органів, більшість дітей при народжені спочатку нічим не вирізняються. Це обумовлено материнським гормонам щитоподібної залози, які проникають через плаценту, і як мінімум частково захищають навіть ті плоди, в яких щитоподібна залоза повністю відсутня. В пуповинній крові цих дітей концентрація тироксину (Т4) становить від 33% до 50% від рівня здорових дітей. У 5% найважчих випадків можуть кидатися в очі велике тім'ячко, значне незрощення черепних швів, великий язик і пупкова грижа.[1] З посиленням розпаду материнського тироксину з'являються нові симптоми. Такі немовлята погано смокчуть, страждають закрепами, байдужі до навколишнього середовища і багато сплять. Часто їх потрібно спеціально будити для годування. Голос може бути грубим і хриплим, шкіра на дотик холодна, слабкий тонус м'язів (гіпотонія), рефлекси ослаблені. Жовтяниця новонароджених, що обумовлена сповільненим дозріванням печінки, може затягнутися. Збільшену щитоподібну залозу (зоб, струма) знаходять в 5-10% дітей, найчастіше при вродженому порушенні синтезу тироксину.[1]
Якщо захворювання не розпізнається і не лікується, на другому-третьому місяці життя проявляється затримка росту. Чим пізніше розпочате лікування, тим нижчим буде розумовий розвиток дитини. Якщо почати лікування в перші три місяці, в середньому коефіцієнт інтелекту (IQ) становитиме 89 (розмах 64-107), якщо почати лікування на 4-6 місяці — 71 (розмах 35-96) і якщо лікування вперше застосувалося після шести місяців 54 (розмах 25-80).[1] Іншими віддаленими наслідками є порушення координації дрібної і великої моторики, порушення рівноваги (атаксії), зниження і підвищення м'язового тонусу, порушення мовлення, уваги, косоокість.

Оскільки рання діагностика є надзвичайно важливою для нормального розвитку дітей, діагноз встановлюється у більшості розвинених країн через масове дослідження новонароджених (скринінг новонароджених). В Україні визначають вміст тиреотропного гормону (ТТГ) в так званій сухій краплі.[3] При недостатній продукції гормонів щитоподібної залози ТТГ значно підвищується. Правда, при цьому методі упускаються рідкісні випадки центральнообумовленого вторинного чи третинного гіпотиреозу.[4]
В США більшість скринінг-програм визначають спершу концентрацію Т4 і тільки при зниженні його додатково визначають тиреотропін.[1]
Забір крові мусить бути обов'язково проведений уже на третю добу життя. Якщо новонародженого відпускаються раніше чи переводять, можна провести забір ще раніше. Але тоді аналіз потрібно ще раз повторити.[4]
В позитивному випадку потрібно терміново провести підтверджуючий тест на визначення тиреотропіну, вільного Т3 і Т4.
Якщо результат підтвердить гіпофункцію щитоподібної залози, можна проводитися додаткові обстеження для вияснення природи захворювання. До них належать, крім визначення тиреоглобуліну, обстеження тканин щитоподібної залози і процесу утворення гормонів. Перед усім це візуалізаційні методи: УЗД і сцинтіграфія щитоподібної залози. Оскільки результати досліджень не мають ніякого впливу на лікування, їх не потрібно проводити в обов'язковому порядку.[1] Якщо є дані про захворювання щитоподібної залози у матері, можна визначити схожість форм аутоантитіл щитоподібної залози у матері і дитини. Якщо схожість підтвердиться захворювання може носити перехідний (тимчасовий) характер. При виникненні підозри на надлишок чи недостачу йоду, як причину гіпотиреозу, можна дослідити рівень йоду в сечі.[1]
Враховуючи незворотність пошкодження нервової системи при вродженому гіпотиреозі, лікування потрібно починати якомога раніше. Не потрібно очікувати результатів необов'язкових методів обстежень, лікування мусить починатись безпосередньо після забору крові для підтвердження діагнозу при позитивному результату скринінгу.[2] Мета лікування полягає в якнайшвидшій нормалізації вмісту Т4 і послідуючій нормалізації рівня ТТГ в крові. Усунення дефіциту гормону вирівнюється призначенням левотироксину у відносно високих вихідних дозах. Через два тижні можна зменшити дозування відповідно до результатів контрольного рівня ТТГ і Т4 в крові. В подальшому доза гормону має бути адаптована відповідно до підвищеної потреби обумовленої фізичним розвитком дитини.
При виникненні сумнівів щодо стійкості гіпотиреозу після першого дня народження потрібно зробити перерву у вживанні гормону. На думку американських фахівців це доцільніше, як на четвертому році життя.[2]
В іншому випадку замісна терапія має проводитися по життєво. Якщо доказано, що причиною гіпофункції є недостача йоду, лікування проводять препаратами йоду.
Прогноз для хворих дітей залежить від терміну встановлення діагнозу. Якщо гіпофункція виявлена протягом перших двох тижнів і цілеспрямовано пролікована, то в дорослому віці спостерігається лише невелика різниця в рівні розумового розвитку, шкільній успішності і нейрофізіологічних тестах в порівнянні з здоровими однокласниками чи їх сестрами і братами.[2] Якщо лікування почалося дещо пізніше, фізичний розвиток може ще нормалізуватися, однак розумовий розвиток залишиться зниженим.
- ↑ а б в г д е ж и Kaye C I and the Committee on Genetics: Newborn Screening Fact Sheet. In: Pediatrics 2006; 118:e934-e963 PMID 16950973
- ↑ а б в г American Academy of Pediatrics, American Thyroid Association, Lawson Wilkins Pediatric Endocrine Society: Update of Newborn Screening an Therapy for Congenital Hypthyroidism. In: Pediatrics 2006; 117:2290-2303
- ↑ Офіційний вебсайт Міністерства охорони здоров'я України. Архів оригіналу за 7 липня 2015. Процитовано 8 березня 2012.
- ↑ а б Leitlinie der GNPI. Архів оригіналу за 24 лютого 2008. Процитовано 8 березня 2012.