X-gal

| X-gal | |
|---|---|
 | |
| Ідентифікатори | |
| Номер CAS | 7240-90-6 |
| Номер EINECS | 230-640-8 |
| ChEBI | 75055 |
| SMILES | C1=CC(=C(C2=C1NC=C2OC3C(C(C(C(O3)CO)O)O)O)Cl)Br[1] |
| InChI | InChI=1S/C14H15BrClNO6/c15-5-1-2-6-9(10(5)16)7(3-17-6)22-14-13(21)12(20)11(19)8(4-18)23-14/h1-3,8,11-14,17-21H,4H2/t8-,11+,12+,13-,14-/m1/s1 |
| Номер Бельштейна | 1552604 |
| Властивості | |
| Молекулярна формула | C14H15BrClNO6 |
| Молярна маса | 408,63 г/моль |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
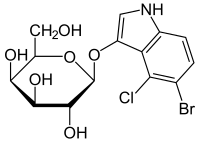
X-gal (або 5-бромо-4-хлоро-3-індоліл-β-D-галактопіранозид) — органічна сполука, що складається із галактози та галоген-заміщеного індолу сполучених О-глікозидним зв'язком. Вперше була синтезована в 1964 році.[2] X-gal широко застосовується в молекулярній біології як індикатор присутності ензима β-галактозидази. Він також застосовується для виявлення цього білка в гістохімії та бактеріології. Після ензиматичного гідролізу X-gal утворює синій нерозчинний барвник близький по структурі до індиго.[3]
X-gal — це похідне лактози, тому він може гідролізувати під впливом β-галактозидази, ензиму який розщеплює β-глікозидний зв'язок в D-лактозі. Після ензиматичного розщеплення X-gal утворює дві хімічні сполуки: галактозу і 5-бромо-4-хлоро-3-гідроксиіндол. Останній спонтанно зазнає окиснювальної димеризації під впливом кисню, утворюючи 5,5'-дибром-4,4'-дихлоро-індиго, нерозчинну хімічну сполуку інтенсивно синього кольору. Оськільки сам X-gal є безкольоровим, поява інтенсивного синього кольору в середовищі може бути індикатором присутності активної β-галактозидази. Цей тест дає змогу використовувати ген β-галактозидази (ген lacZ ) як a ген-репортер в різних експериментах.[4]
В молекулярному клонуванні X-gal засносовується для візуальної оцінки експресії β-галактозидази клітинами в експериментальній техніці, яка називається синьо-білий скринінг. Ця техніка застосовується, щоб відділити продукти успішного клонування від побічних.
Метод синьо-білого скринінгу базується на принципі α-комплементарності гену β-галактозидази, коли фрагмент гену lacZ (так званий lacZα) в плазміді може доповнити інший мутантний ген lacZ (lacZΔM15), що вже є в клітині. Обидва гени самі по собі продукують нефункціональні поліпептиди. В той же час, якщо ці гени експресуються в клітині одночасно, наприклад, у клітинах із геном lacZΔM15 після трансформації плазмідою із lacZα, обидва поліпептида в клітині утворюють функціональну β-галактозидазу. Наявність функціонального ензиму може бути визначена, якщо бактерії вирощуються на чашках Петрі із середовищем, що містить X-gal, оскільки розщеплення і окиснення X-gal в результаті обумовлює блакитний колір відповідних бактеріальних колоній. Якщо під час молекулярного клонування цільовий ген був вставлений в плазміду посередині гену lacZα, успішне клонування призведе до того, що клітини втратять змогу експресувати правильний поліпептид з гену lacZα, в результаті чого клітини втратять здатність утворювати активний ензим в цілому, і відповідні колонії будуть забарвлені в білий колір. Візуально оцінюючи колір бактеріальних колоній, можна відрізнити продукти успішного клонування (білі колонії) від тих, що несуть вихідну плазміду (сині колонії). Прикладом векторів, що використовуються для цієї процедури, є pUC19, pBluescript, pGem-T вектори, які також вимагають використання спеціальних ліній E. coli, таких як DH5α, що містять мутантний lacZΔM15 ген.
X-gal має численні аналоги, які відрізняються ароматичним замісником на галактозі і були розроблені головним чином для того, щоб давати колонії інших кольорів, ніж сині.
| Коротка назва | Довга назва | Колір |
|---|---|---|
| Blue-Gal, Bluo-Gal | 5-бромо-3-індоліл β-D-галактопіранозид | Темно-синій[5] |
| Rose-Gal, Salmon-Gal, Y-Gal, Red-Gal | 6-хлоро-3-індоліл-β-D-галактопіранозид | Рожевий[6] |
| Purple-β-D-Gal | 5-йодо-3-індоліл-β-D-галактопіранозид | Пурпуровий[7] |
| Magenta glucoside, Magenta-GLC, Magenta gal | 5-бромо-6-хлоро-3-індоліл-β-D-галактопіранозид | Фіолетовий[8] |
| Green-β-D-gal | N-метиліндоліл-β-D-галактопіранозид | Зелений[9] |
| MUG, MUGA | 4-метилумбеліферил β-D-галактопіранозид | Флуоресцентний блакитний[10] (λex = 365, λem = 455) |
У двогібридному аналізі, β-галактозидаза може бути використана як репортер, що детектує взаємодію двох білків між собою. В рамках цього методу, геномні бібліотеки можуть бути проскрінені для пошуку взаємодіючих партнерів із використання дріжджів або бактерій як модельних організмів.
- ↑ 7240-90-6
- ↑ Horwitz JP and 7 others, 1964. Substrates for cytochemical demonstration of enzyme activity. I. Some substituted 3-indolyl-β-D-glycopyranosides. Journal of Medicinal Chemistry 7: 574—575
- ↑ Kiernan JA 2007. Indigogenic substrates for detection and localization of enzymes. Biotechnic & Histochemistry 82(2): 73-103.
- ↑ Sandhu, Sardul Singh (2010). Recombinant DNA Technology. I K International Publishing House. с. 116. ISBN 978-9380578446.
- ↑ 5-Bromo-3-indolyl β-D-galactopyranoside. Архів оригіналу за 22 червня 2015. Процитовано 4 лютого 2014.
- ↑ Salmon-Gal - PubChem. Архів оригіналу за 21 лютого 2014. Процитовано 4 лютого 2014.
- ↑ Purple-beta-D-Gal - PubChem. Архів оригіналу за 21 лютого 2014. Процитовано 4 лютого 2014.
- ↑ 5-Bromo-6-chloro-3-indolyl-β-D-glucopyranoside. Архів оригіналу за 22 червня 2015. Процитовано 4 лютого 2014.
- ↑ Green-β-D-Gal - Biotium, Inc. Архів оригіналу за 21 лютого 2014. Процитовано 4 лютого 2014.
- ↑ 4-Methylumbelliferyl β-D-galactopyranoside. Архів оригіналу за 24 вересня 2015. Процитовано 4 лютого 2014.
