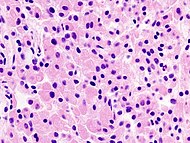
Синдром Нельсона

| Синдром Нельсона | |
|---|---|
| МКБ-11 | 5A70.3 |
| МКБ-10 | E24.1 |
| МКБ-10-КМ | E24.1 |
| OMIM | 125530 |
| DiseasesDB | 8863 |
| eMedicine | ped/1558 |
| MeSH | D009347 |
Синдро́м Не́льсона — заболевание, характеризующееся хронической надпочечниковой недостаточностью, гиперпигментацией кожного покрова, слизистых оболочек и наличием опухоли гипофиза[1]. Данный синдром можно рассматривать как своеобразное осложнение после лечения болезни Кушинга методом двусторонней адреналэктомии, либо длительной терапии хлодитаном[2].
История
[править | править код]Заболевание названо в честь учёного D. H. Nelson, который впервые в 1958 году с соавторами описал пациентку, у которой через 3 года после двусторонней адреналэктомии по поводу болезни Кушинга развилась большая хромофобная аденома гипофиза[3].
Ещё раз описание феномена опубликовано американским эндокринологом доктором Don Nelson с соавторами в 1960 году[4].
Эпидемиология
[править | править код]Синдром Нельсона развивается у пациентов с болезнью Кушинга через разные промежутки времени после тотальной (двусторонней, билатеральной) адреналэктомии от нескольких месяцев до 20 лет. Обычно синдром возникает в молодом возрасте в течение 6 лет после оперативного вмешательства[1].
В последние годы заболевание встречается реже в связи с тем, что двусторонняя адреналэктомия стала применяться только в экстремальных ситуациях[5].
Этиология
[править | править код]Развитие синдрома Нельсона обусловлено ростом исходно имеющейся при болезни Кушинга аденомы гипофиза и провоцируется выпадением ингибирующего влияния кортикостероидов на кортикотрофы аденогипофиза в результате двусторонней адреналэктомии либо сочетания односторонней адреналэктомии с длительной терапией орто-пара-ДДТ (хлодитан, лизодрен)[6].
Патогенез
[править | править код]Патогенез данного синдрома обусловлен возобновлением роста и быстрым прогрессированием аденомы гипофиза, имевшейся у пациентов с болезнью Кушинга, спровоцированного отсутствием или недостаточным ингибирующим действием кортизола на кортикотропы. Данная особенность имеет принципиальное значение для развития синдрома, так как при болезни Аддисона развитие подобных аденом в клинической практике не наблюдается[2].
После удаления надпочечников разрушается физиологическая регуляторная цепь функции надпочечников гипоталамо-гипофизарной системой (суточный ритм секреции и механизм обратной связи), что ведёт к более высокому уровню АКТГ у пациентов с синдромом Нельсона, чем при болезни Кушинга и носит монотонный характер в течение суток, а введение больших доз дексаметазона не приводит к нормализации уровня АКТГ[1].
При синдроме Нельсона формируются макроаденомы, наблюдается выраженный клеточный и ядерный полиморфизм, много митозов, обусловливающих быстрый и агрессивный рост. Развитие синдрома Нельсона наблюдается даже на фоне заместительной терапии кортикостероидами, в случаях когда получаемые дозы препаратов недостаточны для подавления кортикотрофов[2].
Клиническая картина
[править | править код]У пациентов, получающих лечение по поводу болезни Кушинга, ещё сохраняются внешние признаки гиперкортицизма и появляются признаки тяжёлой первичной хронической надпочечниковой недостаточности (похудение, слабость)[2]. Одним из ранних проявлений синдрома является выраженная гиперпигментация кожи и слизистых оболочек[7], как при тяжёлых формах болезни Аддисона.
Клинические проявления синдрома Нельсона складываются из следующих симптомов[1]:
- прогрессирующей гиперпигментации кожного покрова;
- хронической надпочечниковой недостаточности;
- продуцирующей АКТГ опухоли гипофиза (кортикотропиномы);
- офтальмологических и неврологических нарушений.
Этот раздел статьи ещё не написан. |
Диагностика
[править | править код]Основывается на характерных клинических проявлениях и данных анамнеза о предшествующей двусторонней адреналэктомии по поводу болезни Кушинга[2].
Лабораторная и инструментальная диагностика проводится по результатам исследования уровня АКТГ и подтверждения наличия микро или макроаденомы гипофиза, характеристики ее роста, оценки динамики роста аденомы в сравнении с периодом после двусторонней адреналэктомии до развития заболевания. Для кортикотропиномы в условиях удаленных надпочечников характерно повышение уровня АКГТ более 200 пг/мл, а также отсутствие циркадианного ритма секреции. Величина АКТГ отражает активность аденомы и соответствует выраженности гиперпигментации. При быстро растущих аденомах с инфильтративным ростом и резко выраженной гиперпигментацией уровень АКГТ способен достигать 3000 пг/мл и более.[8]
Дифференциальная диагностика
[править | править код]Проводится с болезнью Аддисона (болезнь Кушинга в анамнезе, отсутствие кортикотропиномы)[2].
При синдроме Нельсона следует исключить синдром Кушинга, вызванный эктопированной опухолью, секретирующей АКТГ. Зачастую эктопированные опухоли (как эндокринных желез, так и неэндокринной системы) настолько малы по размерам, что их местонахождение трудно определить, но все они продуцируют АКТГ, что ведёт к гиперплазии коры надпочечников и развитию синдрома Кушинга. Таким образом, синдром Кушинга при эктопированной опухоли сопровождается гиперпигментацией кожного покрова и протекает с яркой клинической симптоматикой гиперкортицизма. После оперативного вмешательства (адреналэктомия) состояние пациентов улучшается, но рост эктопированной опухоли прогрессирует и содержание АКТГ остаётся высоким и гиперпигментация прогрессирует[1].
Лечение
[править | править код]Направлено на достижение компенсации хронической надпочечниковой недостаточности и воздействие на гипоталамо-гипофизарную систему. Применяются различные методы (медикаментозная терапия, лучевое воздействие на гипофиз и хирургическое удаление опухоли), подавляющие секрецию АКТГ и предотвращающие рост и развитие кортикотропиномы. Медикаментозная и лучевая терапия применяются в случаях новообразований, не выходящих за пределы турецкого седла либо в случаях рецидива или частичного терапевтического эффекта после хирургического лечения[1].
Медикаментозная терапия
[править | править код]Подавляющее влияние на секрецию АКТГ оказывают[1]:
- серотониновый блокатор — ципрогептадин;
- стимулятор дофаминовой секреции — бромокриптин;
- стимулятор синтеза ГАМК (гамма-аминомасляной кислоты) в гипоталамусе — конвулекс (вальпроат натрия).
Лучевые методы лечения
[править | править код]Среди лучевых методов лечения используются различные виды облучения: дистанционные (гамма-лучи, протоновый пучок) и интерстициальные (введение непосредственно в ткань гипофиза изотопов 90Y или 198Au)[1].
Облучение области турецкого седла пучком протонов приводило к снижению пигментации и уменьшению секреции АКТГ[9].
Введение 90Y или 198Au в полость турецкого седла дало положительные результаты у всех восьми пациентов[10].
Хирургическое лечение
[править | править код]
Оперативное вмешательство по поводу кортикотропиномы применяется как при микроаденомах, так и при опухолях больших размеров. Последнее время широко вошёл в клиническую практику метод хирургического вмешательства с трассфеноидальным доступом. Данная методика применяется при опухолях, растущих вниз. В случае большой инвазивной, растущей вверх аденомы гипофиза у пациентов с синдромом Нельсона используют трансфронтальный доступ. Результаты хирургического лечения при небольших опухолях лучше, чем при аденомах с распространённым ростом. Микрохирургическая техника обеспечивает в большинстве случаев полное удаление новообразования, однако после применения оперативного метода лечения встречаются рецидивы заболевания[1].
Оперативное вмешательство по поводу болезни Кушинга заключается в проведении одно- или двусторонней адреналэктомии возможно в сочетании с аутотрансплантацией надпочечника — трансплантат размером 10,0х1,5 мм подсаживают в подкожно-жировую клетчатку[11].
Криотерапия
[править | править код]Кроме облучения, разрушение аденомы гипофиза достигается воздействием низких температур (криохирургия) — жидкий азот подводят в область аденомы гипофиза стереотаксическим методом через трансназально-транссфеноидальный доступ[11].
Комбинированная терапия
[править | править код]Нередко при лечении синдрома Нельсона приходится прибегать к комбинированным методам. В случае отсутствия ремиссии заболевания после курса лучевой терапии назначают ципрогентадин, парлодел, конвулекс. В случаях нерадикального удаления опухоли гипофиза хирургическим путём применяют облучение гипофиза, либо препараты, подавляющие секрецию АКТГ[1].
Прогноз
[править | править код]Зависит от динамики развития аденомы гипофиза и степени компенсации надпочечниковой недостаточности — в случаях медленного прогрессирования опухолевого роста и компенсации надпочечниковой недостаточности состояние пациентов длительное время остаётся удовлетворительным.
Трудоспособность ограничена практически во всех клинических случаях. Необходимо диспансерное наблюдение эндокринолога, невролога, офтальмолога.
Профилактика
[править | править код]Большинство авторов признаю́т, что предупредить развитие синдрома Нельсона и больших опухолей гипофиза легче, чем лечить кортикотропиному с распространением процесса за пределы турецкого седла. Профилактический курс лучевой терапии на область турецкого седла у пациентов с болезнью Кушинга, по данным большинства авторов, не предотвращает развитие синдрома[1].
После билатеральной (тотальной, двусторонней) адреналэктомии необходимо ежегодное проведение рентгенологического исследования области турецкого седла, полей зрения и содержания АКТГ в плазме крови[1].
См. также
[править | править код]Примечания
[править | править код]- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Клиническая эндокринология. Руководство / Под ред. Н. Т. Старковой. — 3-е изд., перераб. и доп. — СПб.: Питер, 2002. — С. 81—88. — 576 с. — («Спутник Врача»). — 4000 экз. — ISBN 5-272-00314-4.
- ↑ 1 2 3 4 5 6 Малая энциклопедия врача-эндокринолога / Под ред. А. С. Ефимова. — 1-е изд. — К.: Медкнига, ДСГ Лтд, Киев, 2007. — С. 325-326. — 360 с. — («Библиотечка практикующего врача»). — 5000 экз. — ISBN 966-7013-23-5.
- ↑ Nelson D. H., Meakin J. W., Dealy J. D. et al. ACTH-producing tumor of pituitary gland // New Engl. J. Med. — 1958. — Vol. 259. — P. 161—169.
- ↑ Nelson D., Meakin J., Thorn G. ACTH-producing pituitary tumors following adrenalectomy for Cushing's syndrome (англ.) // Annals of Internal Medicine[англ.] : journal. — 1960. — Vol. 52. — P. 560—569. — PMID 14426442.
- ↑ Kelly P.A., Samandouras G., Grossman A.B., Afshar F., Besser G.M., Jenkins P.J. Neurosurgical treatment of Nelson's syndrome (англ.) // The Journal of Clinical Endocrinology and Metabolism[англ.]. — 2002. — December (vol. 87, no. 12). — P. 5465—5469. — doi:10.1210/jc.2002-020299. — PMID 12466338. Архивировано 13 декабря 2019 года.
- ↑ Эндокринология (краткий справочник) / Под ред. И. И. Дедова. — 1-е изд. — М.: Рус. врач, 1998. — С. 48. — 95 с. — ISBN 5-7724-0014-2.
- ↑ Эндокринология / Под ред. Н. Лавина. — 2-е изд. Пер. с англ. — М.: Практика, 1999. — С. 92. — 1128 с. — 10 000 экз. — ISBN 5-89816-018-3.
- ↑ Синдром Нельсона. Дата обращения: 6 марта 2018. Архивировано 5 мая 2017 года.
- ↑ Kjullberg R. N., Kliman B., Swisher B. J. Radiosurgery for pituitary adenoma with bragg peak proton beam // Pituitary adenomas. — France: Asclepios Publishers, 1980.
- ↑ Cassar J., Doyle F. H., Lewis P. D. et al. Treatment of Nelson`s syndrome by pituitary implantation of yttrium-90, or gold-198 // Brit. med. J. — 1976. — Vol. 2 — P. 269—272.
- ↑ 1 2 Балаболкин М. И. Эндокринология. — 2-е изд., перераб. и доп. — М.: "Универсум паблишинг", 1998. — С. 174—175. — 582 с. — 10 000 экз. — ISBN 5-7736-0018-8.