Reparació de l'ADN

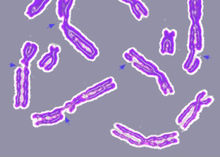
La reparació de l'ADN és el conjunt de processos mitjançant els quals les cèl·lules detecten i reparen els danys soferts per les molècules d'ADN que en codifiquen el genoma.[1] En els éssers humans, tant l'activitat metabòlica normal com els factors ambientals (com ara la radiació) poden causar danys a l'ADN i infligir fins a un milió de lesions moleculars al dia a cada cèl·lula.[2] Moltes d'aquestes lesions causen danys estructurals a la molècula d'ADN i tenen el potencial d'alterar o destruir la capacitat de les cèl·lules de transcriure els gens codificats per l'ADN afectat. Altres lesions produeixen mutacions potencialment nocives en el genoma de la cèl·lula, cosa que afecta la supervivència de les cèl·lules filles després de la mitosi. Així doncs, els mecanismes de reparació de l'ADN responen constantment als danys a l'estructura de l'ADN. Quan fallen els processos normals de reparació de l'ADN i les cèl·lules no moren per apoptosi, es poden produir danys irreparables a l'ADN, incloent-hi trencaments bicatenaris i entrecreuaments de l'ADN,[3][4] que poden conduir al desenvolupament de tumors malignes (càncer) d'acord amb la hipòtesi del doble impacte.
El ritme de reparació de l'ADN depèn de molts factors, com ara el tipus de cèl·lula, la seva edat i el medi extracel·lular. Una cèl·lula que hagi acumulat molts danys a l'ADN o no pugui reparar-los de manera eficaç pot entrar en un de tres estats possibles:
- un estat de repòs irreversible, conegut com a envelliment
- autodestrucció cel·lular, conegut també com a apoptosi o mort cel·lular programada
- una divisió cel·lular no regulada, que pot desembocar en la formació d'un tumor maligne
La capacitat de reparació de l'ADN és vital per la integritat del seu genoma, i per tant, del seu funcionament normal i el de l'organisme. En el cas de molts dels gens que s'havia demostrat que influïen en la longevitat, més tard s'ha revelat que tenen un paper en la reparació i protecció de l'ADN.[5] La incapacitat de corregir lesions moleculars en les cèl·lules que formen gàmetes poden introduir mutacions en el genoma dels seus descendents, influint en el ritme de l'evolució.
Danys a l'ADN
[modifica]Els danys a l'ADN, que es deuen a factors ambientals i als processos metabòlics habituals dins la cèl·lula, tenen lloc a un ritme d'entre mil i un milió de lesions moleculars per cèl·lula per dia.[2] Tot i que això només representa un 0,000165% de les aproximadament 6.000 milions de bases (3.000 milions de parells de bases) del genoma humà, les lesions no reparades en gens crítics (com ara els gens supressors de tumors) poden impedir que una cèl·lula dugui a terme la seva funció i augmentar de manera significativa la possibilitat que es formi un tumor.
La immensa majoria dels danys a l'ADN afecten l'estructura primària de la doble hèlix; és a dir, la química de les bases mateixes és modificada. Aquestes modificacions poden al seu torn destruir l'estructura normal helicoïdal de les molècules, introduint-hi enllaços químics no originals o adductes voluminosos que no caben a l'hèlix doble estàndard. A diferència de les proteïnes i l'ARN, l'ADN sol mancar d'estructura terciària, de manera que no sol haver-hi danys o pertorbacions a aquest nivell. Tanmateix, l'ADN és una superhèlix embolicada al voltant de proteïnes «empaquetadores» anomenades histones (en els eucariotes), i ambdues estructures són vulnerables als efectes dels danys a l'ADN.
Causes dels danys
[modifica]Els danys a l'ADN es poden subdividir en dos tipus principals:
- els danys endògens, com ara atacs per part d'espècies reactives de l'oxigen produïdes a partir de subproductes metabòlics normals (mutació espontània), especialment en el procés de desaminació oxidativa;
- els danys exògens causats per agents externs, com ara:
- Radiació ultraviolada del sol [UV 200-300nm] o altres freqüències de radiació, incloent-hi els rajos X i els rajos gamma.
- Radiació ionitzant.
- Hidròlisi o disrupció tèrmica.
- Algunes toxines vegetals.
- Mutàgens artificials, especialment compostos aromàtics que actuen com a agents intercalants de l'ADN.
- Quimioteràpia i radioteràpia com a tractament contra el càncer.
- Virus que s'integren en el genoma[6]
La replicació d'ADN danyat abans que la cèl·lula es divideixi pot provocar la incorporació de bases errònies davant les danyades. Les cèl·lules filles que hereten aquestes bases errònies porten mutacions en què la seqüència d'ADN original és irrecuperable (excepte en el rar cas d'una reversió de la mutació, o bé més sovint a través de la recombinació genètica tot i que és igualment rar).
Tipus de danys
[modifica]Hi ha quatre tipus principals de danys a l'ADN a causa de processos cel·lulars endògens:
- oxidació de les bases (per exemple, 8-oxo-7,8-dihidroguanina (8-oxoG)) i generació d'interrupcions de la cadena d'ADN per part d'espècies reactives de l'oxigen,
- alquilació de bases (normalment metilació), com ara la formació de 7-metilguanina, 1-metiladenina, O6-metilguanina
- hidròlisi de bases, com ara desaminació, depurinació i depirimidinació.
- malaparellament de bases, a causa d'errors en la replicació de l'ADN, en què s'insereix una base d'ADN errònia en una cadena d'ADN en formació, s'insereix una base que no cal inserir, o no se n'insereix una de necessària.
Els danys causats per agents exògens són de molts tipus. Alguns exemples són:
- la llum UV-B causa entrecreuaments entre bases adjacents de citosina i timina, creant dímers de pirimidina. Això rep el nom de dany directe a l'ADN.
- la llum UV-A provoca la formació de radicals lliures, especialment si hi ha crema solar que ha penetrat a la pell. Això rep el nom de dany indirecte a l'ADN.
- la radiació ionitzant, com ara la que causa la desintegració radioactiva o la dels rajos còsmics, provoca trencaments en les cadenes d'ADN.
- la disrupció tèrmica a temperatures elevades augmenta la velocitat de la despurinització (pèrdua de bases de purina del «tronc» de l'ADN) i dels trencaments de cadenes senzilles. Per exemple, s'observa depurinització hidrolítica en els bacteri termòfils, que viuen en aigües termals a 85-250 °C.[7] En aquestes espècies, la velocitat de despurinització (300 residus de purina per genoma per generació) és massa alta perquè es repari per mitjà dels mecanismes habituals de reparació, de manera que no es pot descartar la possibilitat d'una resposta adaptativa.
- productes químics industrials, com ara el clorur de vinil o l'aigua oxigenada, així com compostos químics ambientals com ara els hidrocarburs policíclics que es troben en el fum, el sutge i el quitrà, provoquen una gran diversitat d'adductes-etenobases d'ADN, bases oxidades, fosfotrièsters alquilats, i entrecreuament de l'ADN, per citar només alguns efectes.
Els danys per radiació UV, l'alquilació/metilació, els danys per rajos X i els danys oxidatius són exemples de danys induïts. Els danys espontanis inclouen la pèrdua d'una base, la desaminació, plegaments dels anells de sucre, i els desplaçaments de tautòmers.
Danys a l'ADN nuclear i a l'ADN mitocondrial
[modifica]En les cèl·lules humanes, i les cèl·lules eucariotes en general, l'ADN es troba en dos punts de la cèl·lula: dins el nucli i dins els mitocondris. L'ADN nuclear (ADNn) existeix en forma de cromatina durant les fases no replicadores del cicle cel·lular, i és condensat en estructures agregades denominades cromosomes durant la divisió cel·lular. En ambdós estats, l'ADN és altament compacte i s'enrotlla al voltant de proteïnes en forma de perla, anomenades histones. Quan una cèl·lula necessita expressar la informació genètica codificada en el seu ADNn, es desenrotlla la regió cromosòmica corresponent, s'expressen els seus gens, i després la regió torna a ser condensada en la seva forma de repòs. L'ADN mitocondrial (ADNmt) es troba dins dels mitocondris (un tipus d'orgànuls), existeix en múltiples còpies, i està estretament associat amb una sèrie de proteïnes per formar un complex anomenat nucleoide. Dins dels mitocondris, les espècies reactives de l'oxigen (ERO) i els radicals lliures, subproductes de la producció constant de trifosfat d'adenosina (ATP) per mitjà de la fosforilació oxidativa, creen un medi altament oxidatiu que se sap que danya l'ADNmt. Un enzim clau a l'hora de compensar la toxicitat d'aquestes espècies és la superòxid dismutasa, que està present tant als mitocondris com al citoplasma de les cèl·lules eucariotes.
Envelliment i apoptosi
[modifica]L'envelliment, un estat irreversible en què la cèl·lula ja no es divideix (mitosi), és una resposta protectora a l'escurçament dels extrems dels cromosomes (telòmers). Els telòmers són llargues regions d'ADN no codificant repetitiu, que delimiten els cromosomes i que es degraden parcialment cada cop que una cèl·lula es divideix (vegeu límit de Hayflick).[8] En canvi, la quiescència és un estat reversible de latència que no té relació amb els danys al genoma (vegeu Cicle cel·lular). L'envelliment de les cèl·lules pot representar una alternativa funcional a l'apoptosi en què la presència física d'una cèl·lula és necessària per a l'organisme,[9] que serveix com a mecanisme d'últim recurs per evitar que una cèl·lula amb l'ADN danyat es repliqui anormalment en l'absència de comunicació cel·lular pro-creixement. La divisió cel·lular incontrolada pot provocar la formació d'un tumor (vegeu Càncer), que és potencialment letal per a l'organisme. Per tant, la inducció de l'envelliment i l'apoptosi és considerada part de l'estratègia de protecció contra el càncer.
Danys a l'ADN i mutacions
[modifica]És important distingir entre els danys a l'ADN i les mutacions, els dos tipus principals d'errors en l'ADN. Els danys a l'ADN i les mutacions són fonamentalment diferents. Aquests danys són en darrer terme anormalitats químiques en l'estructura de l'ADN, com ara trencaments monocatenaris i bicatenaris, residus de 8-hidroxideoxiguanosina, i adductes d'hidrocarburs aromàtics policíclics. Determinades proteïnes poden reconèixer aquestes alteracions a l'ADN, de manera que els poden reparar si hi ha disponible informació redundant per ser copiada, a partir de la seqüència intacta de la cadena d'ADN complementària que no ha sofert aquesta alteració. Si una cèl·lula no repara danys al seu ADN, pot quedar aturada l'expressió d'un gen.
En contrast als danys a l'ADN, una mutació és un canvi en la seqüència de bases de l'ADN, és a dir que no es produeix cap canvi que pugui ser reconegut per les proteïnes encarregades de la correcció d'aquestes alteracions, ja que la seva composició química i estructural és «normal». Les mutacions provinents dels errors de síntesi no pot ser reconeguda pels enzims una vegada el canvi de bases és present en ambdues cadenes de l'ADN, de manera que les mutacions resulten indetectables a la correcció i no són reparades. Les mutacions són replicades durant la divisió cel·lular.
A nivell cel·lular, les mutacions poden provocar canvis en el metabolisme i la proliferació d'aquestes cèl·lules. En el conjunt de cèl·lules d'un organisme, el nombre de cèl·lules mutants augmentarà o disminuirà segons els efectes de la mutació en la capacitat de la cèl·lula per sobreviure i reproduir-se. Tot i que són clarament diferents els uns de les altres, els danys a l'ADN i les mutacions estan relacionats, car els danys a l'ADN provoquen sovint errors de síntesi de l'ADN durant la replicació o la reparació i aquests errors són una causa important de mutacions.
Tenint en compte les propietats dels danys a l'ADN i les mutacions, es pot veure que els danys a l'ADN són un problema especial en cèl·lules que no es divideixen o que ho fan lentament, car els danys no reparats tendeixen a acumular-s'hi amb el temps. D'altra banda, en les cèl·lules que es divideixen ràpidament, els danys a l'ADN no reparats que no maten la cèl·lula evitant-ne la replicació solen provocar errors durant la replicació i, per tant, mutacions.
La gran majoria de mutacions que no tenen un efecte neutre són deletèries per a la supervivència d'una cèl·lula. Així doncs, en una població de cèl·lules d'un teixit amb cèl·lules que es repliquen, les cèl·lules mutants tendeixen a desaparèixer. Tanmateix, les poques mutacions que ofereixen un avantatge per la proliferació cel·lular tendeixen a estendre's de manera clònica a expenses de les cèl·lules veïnes. Aquest avantatge per la cèl·lula és un desavantatge per l'organisme en general, car aquestes cèl·lules mutants proliferen lliurement escapant al control del cicle cel·lular, són les cèl·lules canceroses. Aquells tipus cel·lulars que es divideixen més sovint tendeixen a acumular més fàcilment les mutacions, ja que un cop esdevingudes les mutacions triguen aquestes cèl·lules triguen poc temps a replicar l'ADN i per tant la mutació incorporada resta poc temps amb la còpia inicial de la cadena complementària. Així doncs un cop dividida una de les dues cèl·lules resultants de la divisió haurà "fixat" la variant mutant, essent més difícil que ocorri la correcció.
Així doncs, els danys a l'ADN en cèl·lules que es divideixen sovint són una causa important de càncer, car donen peu a mutacions. En canvi, els danys a l'ADN en cèl·lules que es divideixen poc són probablement una causa important de l'envelliment.
Mecanismes de reparació de l'ADN
[modifica]Les cèl·lules no poden funcionar si els danys a l'ADN corrompen la integritat i accessibilitat d'informació essencial en el genoma (però les cèl·lules romanen aparentment funcionals quan manquen o estan danyats gens «no essencials»). Segons el tipus de danys que ha sofert l'estructura de doble hèlix de l'ADN, han evolucionat una varietat d'estratègies de reparació que restauren la informació perduda. Si és possible, les cèl·lules utilitzen la cadena d'ADN complementària (si no ha estat modificada) o la cromàtide germana com a «plantilla» per tal de restaurar la informació original. Si no hi ha cap plantilla disponible, les cèl·lules utilitzen com a últim recurs un sistema de recuperació propens als errors conegut com a síntesi de translesió.
Els danys a l'ADN alteren la configuració espacial de l'hèlix, la seva topologia, i la cèl·lula és capaç de detectar aquestes alteracions. Una vegada es detecten els danys, unes molècules específiques reparadores de l'ADN s'adhereixen al punt danyat o a prop d'ell, induint altres molècules a adherir-se i formar un complex que permet que tingui lloc la reparació. Els tipus de molècules implicats i el mecanisme de reparació que s'utilitza depèn del tipus de danys que hagi sofert l'ADN i de la fase del cicle cel·lular en què es trobi la cèl·lula.
Inversió directa
[modifica]Se sap que les cèl·lules eliminen tres tipus de danys a l'ADN invertint-los químicament. Aquests mecanismes no requereixen una plantilla, car els tipus de danys que reparen només poden tenir lloc en una de les quatre bases. Aquests mecanismes d'inversió directa són específics a cada tipus de dany i no impliquen la fragmentació del nucli de fosfodièster. La formació de dímers de timina (un tipus comú de dímer de ciclobutil) després d'irradiació amb llum ultraviolada resulta en un enllaç covalent anormal entre bases de timidina adjacents. El procés de fotoreactivació inverteix directament aquest dany per mitjà de l'acció de l'enzim fotoliasa, l'activació del qual depèn necessàriament de l'energia absorbida de la llum blava/UVA (longitud d'ona de 300-500nm) per promoure la catàlisi.[10] Un altre tipus de danys, la metilació de bases de guanina, és directament revertit per la proteïna metilguanina metil transferasa (MGMT), l'equivalent bacterià de la qual rep el nom d'ogt. Es tracta d'un procés exigent en recursos, car cada molècula de MGMT només es pot fer servir una vegada; és a dir, la reacció és estequiomètrica i no catalítica.[11] En bacteris hi ha una resposta generalitzada als agents metilants, coneguda com a resposta adaptativa, i que confereix una certa resistència als agents alquilants després d'una exposició perllongada per mitjà de la sobreregulació dels enzims de reparació de l'alquilació.[12] El tercer tipus de danys a l'ADN invertit per les cèl·lules és una certa metilació de les bases citosina i adenina.
Danys monocatenaris
[modifica]
Quan només una de les dues cadenes de la doble hèlix té un defecte, l'altra pot ser utilitzada com a plantilla per dirigir la correcció de la cadena danyada. Per tal de reparar danys a una de les molècules aparellades d'ADN, existeixen diversos mecanismes de reparació d'excisions, que eliminen el nucleòtid danyat i el substitueixen amb un nucleòtid intacte complementari al que es troba a la cadena d'ADN no danyada.[11]
- Reparació per excisió de base (BER), que repara danys a un únic nucleòtid causats per oxidació, alquilació, hidròlisi o desaminació. La base és eliminada per la glicosilasa i finalment substituïda per síntesi de reparació per l'ADN ligasa.
- Reparació per excisió de nucleòtid (NER), que repara danys que afectin cadenes més llargues, d'entre dos i trenta bases. Aquest procés reconeix canvis grans que distorsionen l'hèlix, com ara dímers de timina, així com trencaments monocatenaris (reparats amb enzims com ara l'UvrABC endonucleasa. Una forma especialitzada de NER, coneguda com a reparació acoblada a transcripció (TCR) desplega enzims NER d'alta prioritat en gens que s'estan transcrivint activament.
- Reparació de malaparellament (MMR), que corregeix errors en la replicació i recombinació de l'ADN que resulten en nucleòtids mal aparellats (però normals, és a dir, no danyats) després de la replicació de l'ADN.
Danys bicatenaris
[modifica]Els trencaments bicatenaris, en què ambdues cadenes de la doble hèlix queden trencades, són especialment perillosos per la cèl·lula, car poden provocar rearranjaments del genoma. Existeixen dos mecanismes que reparen aquests trencaments: la unió d'extrems no homòlegs (NHEJ de l'anglès Non-homologous DNA End Joining) i la reparació recombinativa (també coneguda com a reparació assistida per plantilla o reparació de recombinació homòloga).[11]
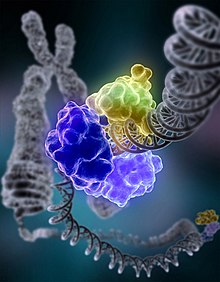
En l'NHEJ l'ADN ligasa IV, una ADN ligasa especialitzada que forma un complex amb el cofactor XRCC4, uneix directament els dos extrems.[13] Per assegurar-se d'una reparació precisa, l'NHEJ es basa en curtes seqüències homòlogues anomenades microhomologies, presents a les cues monocatenàries dels extrems d'ADN que han de ser units. Si aquestes seqüències són compatibles, la reparació sol ser correcta.[14][15][16][17] L'NHEJ també pot causar mutacions durant la reparació. La pèrdua de bases nitrogenades al punt de trencament pot provocar delecions i la unió de translocacions de forma terminal no corresponents. L'NHEJ és especialment important abans que la cèl·lula hagi replicat el seu ADN, car no hi ha cap plantilla que permeti la reparació per recombinació homòloga. Hi ha rutes d'NHEJ "de seguretat" en els eucariotes superiors.[18] A més del seu paper com a "cuidador" del genoma, l'NHEJ és necessària per unir trencaments bicatenaris amb extrems d'agulla de ganxo, causats durant la recombinació V(D)J, el procés que genera la diversitat dels receptors dels limfòcits B i dels limfòcits T al sistema immunitari dels vertebrats.[19]
La reparació recombinant requereix la presència d'una seqüència idèntica o gairebé idèntica que sigui utilitzada com a plantilla per reparar el trencament. La maquinària enzimàtica responsable d'aquest procés és gairebé idèntica a la maquinària responsable del creuament cromosòmic durant la meiosi. Aquesta ruta permet que un cromosoma danyat sigui reparat utilitzant una cromàtide germana (disponible a G2 després de la replicació de l'ADN) o un cromosoma homòleg com a plantilla. Els trencaments bicatenaris causats pels intents de la maquinària replicant de sintetitzar a través d'un trencament monocatenari o una lesió no reparada provoquen un col·lapse de la forqueta de replicació i són generalment reparats per recombinació.
Les topoisomerases provoquen trencaments tant monocatenaris com bicatenaris quan canvien l'estat de superenrotllament de l'ADN, cosa que és especialment habitual en regions situades a prop d'una forqueta de replicació oberta. Aquests trencaments no són considerats danys a l'ADN, car són un intermedi natural del mecanisme bioquímic de les topoisomerases i són immediatament reparats pels enzims que els han creat.
Un grup de científics francesos bombardejaren Deinococcus radiodurans per estudiar el mecanisme de reparació de trencaments bicatenaris en aquest organisme. Almenys dues còpies del genoma, amb trencaments aleatoris de l'ADN, poden formar fragments d'ADN per mitjà d'aparellament. Aleshores, els fragments que s'encavalquen parcialment són utilitzats per sintetitzar les regions homòlogues per mitjà d'un bucle-D en moviment que pot continuar l'extensió fins que troba cadenes corresponents complementàries. A l'últim pas es produeix un creuament per mitjà d'una recombinació homòloga RecA dependent.[20]
Síntesi de translesió
[modifica]La síntesi de translesió és un procés de tolerància dels danys a l'ADN que permet als mecanisme de replicació de l'ADN replicar antigues lesions de l'ADN com ara dímers de timina o llocs AP. Implica la substitució d'ADN polimerases normals per polimerases de translesió especialitzades (com ara l'ADN polimerasa V), que sovint tenen zones actives més grans que poden facilitar la inserció de bases davant de nucleòtids danyats. Es creu que el canvi de polimerases és mitjançat per, entre altres factors, la modificació post-traduccional del factor de processivitat de replicació PCNA. Les polimerases de síntesi de translesió sovint tenen una baixa fidelitat (alta propensió a inserir bases equivocades) en comparació amb les polimerases normals. Tanmateix, moltes són extremament eficients a l'hora d'inserir bases correctes davant de tipus específics de danys. Per exemple la Pol η mitjança una derivació lliure d'errors de les lesions provocades per la radiació UV, mentre que la ζ introdueix mutacions en aquests zones. Des d'un punt de vista cel·lular, el risc d'introduir una mutació puntual durant la síntesi de translesió pot ser preferible a recórrer a mecanismes més dràstics de reparació de l'ADN, que poden causar greus aberracions cromosòmiques o la mort cel·lular.
Resposta global als danys a l'ADN
[modifica]Les cèl·lules exposades a radiacions ionitzants, llum ultraviolada o substàncies químiques són propenses a adquirir múltiples punts de lesions de l'ADN voluminoses i trencaments bicatenaris. A més, els agents que danyen l'ADN també poden danyar altres biomolècules com ara les proteïnes, els carbohidrats, els lípids i l'ARN. L'acumulació de danys, especialment de trencaments bicatenaris o adductes que obstaculitzen les forquetes de replicació, és un dels senyals d'estimulació coneguts d'una resposta global als danys a l'ADN.[21] La resposta global als danys és un acte enfocat a preservar les cèl·lules i desencadena múltiples rutes de reparació macromolecular, derivació de lesions, tolerància o apoptosi. Les característiques comunes de la resposta global són la inducció de múltiples gens, una aturada del cicle cel·lular, i la inhibició de la divisió cel·lular.
Punts de control dels danys a l'ADN
[modifica]Quan es produeixen danys a l'ADN, s'activen punts de control del cicle cel·lular. L'activació dels punts de control atura el cicle cel·lular i dona temps a la cèl·lula de reparar els danys abans de continuar dividint-se. Els punts de control de danys a l'ADN es troben als límits G1/S i G2/M. També existeix un punt de control intra-S. L'activació dels punts de control és regulada per dues cinases mestres, l'ATM i l'ATR. L'ATM respon a trencaments bicatenaris i disrupcions de l'estructura de la cromatina,[22] mentre que l'ATR respon principalment a forquetes de replicació aturades. Aquestes cinases fosforilen dianes en direcció 3′ en una cascada de transducció de senyals, provocant finalment l'aturada del cicle cel·lular. També s'ha identificat una classe de proteïnes mediadores dels punts de control, incloent-hi BRCA1, MDC1 i 53BP1.[23] Aquestes proteïnes semblen necessàries per transmetre el senyal d'activació del punt de control a proteïnes en direcció 3′.
La p53 és una diana important de l'ATM i l'ATR, car és necessària per induir l'apoptosi després dels danys a l'ADN.[24] Al punt de control G1/S, la p53 funciona desactivant el complex CDK2/ciclina E. De manera semblant, la p21 mitjança el punt de control G2/M desactivant el complex CDK/ciclina B.
La resposta SOS dels procariotes
[modifica]La resposta SOS són aquells canvis en l'expressió gènica en Escherichia coli i altres bacteris en resposta a grans danys a l'ADN. El sistema SOS procariota és regulat per dues proteïnes clau: LexA i RecA. L'homodímer de LexA és un repressor transcripcional que s'uneix a seqüències operadores denominades habitualment caixes SOS. Se sap que la LexA regula la transcripció d'aproximadament 48 gens, incloent-hi els gens lexA i recA.[25] Els senyals cel·lulars més comuns que activen la resposta SOS són regions d'ADN monocatenari (ssDNA), que sorgeixen de forquetes de replicació aturades o trencaments bicatenaris i que són processades per l'ADN helicasa per separar les dues cadenes d'ADN.[21] Al primer pas, la proteïna RecA s'uneix a l'ADN monocatenari en una reacció alimentada per la hidròlisi d'ATP, creant filaments de RecA–ssDNA. Els filaments de RecA–ssDNA engeguen l'activitat de LexA autoproteases, que finalment condueix a la fragmentació del dímer de LexA i la posterior degradació de la LexA. La pèrdua del repressor LexA indueix la transcripció dels gens SOS i permet més inducció de senyals, inhibició de la divisió cel·lular i un increment dels nivells de les proteïnes responsables del processament dels danys.
Les caixes SOS són seqüències de 20 nucleòtids de llarg situades a prop de promotors, amb una estructura palindròma i un alt grau de conservació de seqüència. Aquesta distinció en les seqüències de promotors causa una unió diferencial de la LexA a diferents promotors i permet temporitzar la resposta SOS. Lògicament, els gens de reparació de lesions són induïts al principi de la resposta SOS. Les polimerases de translesió, propenses a errors, com ara: UmuCD'2 (també denominada ADN polimerasa V), són induïdes més tard com a últim recurs.[26] Un cop els danys a l'ADN estan reparats o esquivats per mitjà de polimerases o de la recombinació, la quantitat d'ADN monocatenari de les cèl·lules és reduïda. La disminució de la quantitat de filaments de RecA redueix l'activitat fragmentant de l'homodímer de LexA, que posteriorment s'uneix a les caixes SOS a prop dels promotors i restaura l'expressió gènica normal.
Les respostes transcripcionals dels eucariotes als danys a l'ADN
[modifica]Les cèl·lules eucariotes exposades a agents que danyen l'ADN també activen rutes defensives importants per mitjà de la inducció de múltiples proteïnes implicades en la reparació de l'ADN, punts de control del cicle cel·lular, tràfic de proteïnes i la seva degradació. Aquest tipus de resposta transcipcional que abasta el genoma complet és molt complex i està estrictament regulat, permetent una resposta global coordinada als danys. L'exposició del llevat Saccharomyces cerevisiae a agents que danyen l'ADN resulta en perfils de transcripció que s'encavalquen, però que són distints. Les semblances amb la resposta de xoc ambiental indiquen que existeix una ruta de resposta a l'estrès global general al nivell de l'activació transcripcional. En canvi, els diferents tipus de cèl·lules humanes responen diferentment als danys, cosa que indica l'absència d'una resposta global comuna. L'explicació més probable d'aquesta diferència entre les cèl·lules dels llevats i dels humans pot ser l'heterogeneïtat de les cèl·lules dels mamífers. En els animals, els diferents tipus de cèl·lula estan distribuïts entre diferents òrgans, que han desenvolupat diferents sensibilitats als danys a l'ADN.[27]
La resposta global general als danys de l'ADN implica l'expressió de múltiples gens responsables de la reparació de malaparellament, la recombinació homòloga, la reparació per excisió de nucleòtids, els punts de control de danys a l'ADN, l'activació transcripcional global, els gens que controlen la descomposició de l'ARNm i molts altres. La immensa quantitat de danys provocats a la cèl·lula la deixen amb una decisió important; sofrir apoptosi i morir, o sobreviure amb un genoma modificat. Un augment de la tolerància als danys pot conduir a una taxa de supervivència superior, cosa que permet una major acumulació de mutacions. La Rev1 dels llevats i la polimerasa η humana són membres de la família Y d'ADN polimerases presents durant la resposta global als danys a l'ADN i són responsables d'una mutagènesi millorada durant la resposta global als danys a l'ADN en els eucariotes.[21]
La reparació a l'ADN i l'envelliment
[modifica]Efectes patològics d'una reparació de l'ADN deficient
[modifica]
Els animals experimentals amb deficiències genètiques en la reparació de l'ADN sovint presenten una longevitat reduïda i una major incidència de càncer. Per exemple, els ratolins deficients en la ruta NHEJ dominant i en els mecanismes de manteniment dels telòmers pateixen limfoma i infeccions més sovint, i solen tenir una longevitat més curta que la dels ratolins de tipus salvatge.[28] De manera similar, els ratolins deficients en una proteïna clau de reparació i transcripció que desenrotlla les hèlixs d'ADN (helicases) tenen una aparició prematura de malalties relacionades amb l'envelliment, amb el consegüent escurçament de la longevitat.[29] Tanmateix, no totes les deficiències en la reparació de l'ADN produeix exactament els efectes predits; els ratolins deficients en la ruta NER presentaven una longevitat escurçada sense la taxa de mutació més elevada corresponent.[30]
Si la velocitat dels danys a l'ADN supera la capacitat de la cèl·lula de reparar-los, l'acumulació d'errors pot aclaparar la cèl·lula i causar un envelliment prematur, apoptosi o càncer. Les malalties hereditàries associades amb una reparació de l'ADN deficient causen envelliment prematur, una major sensibilitat als cancerígens, i el corresponent major risc de patir càncer (vegeu més avall). D'altra banda, els organismes amb millors sistemes de reparació de l'ADN, com ara Deinococcus radiodurans, l'organisme més resistent a la radioactivitat, presenten una resistència notable als efectes causants de trencaments bicatenaris de la radioactivitat, probablement a causa d'una major eficàcia de la reparació de l'ADN i especialment de l'NHEJ.[31]
Longevitat i restricció de calories
[modifica]
S'ha identificat una sèrie de gens individuals com a factors que influeixen les variacions en la longevitat dins d'una població d'organismes. Els efectes d'aquests gens depenen molt de l'ambient, particularment de la dieta de l'organisme. La restricció calòrica resulta en una major longevitat en una varietat d'organismes, probablement per rutes de percepció de nutrients i un ritme metabòlic més baix. Els mecanismes moleculars pels quals aquesta restricció causa una major longevitat encara no estan clars (vegeu[32] per una discussió del tema); tanmateix, el comportament de molts gens que se sap que estan implicats en la reparació de l'ADN és alterat sota condicions de restricció calòrica.
Per exemple, l'augment de la dosificació gènica del gen SIR-2, que regula l'empaquetament de l'ADN en el cuc nematode Caenorhabditis elegans pot incrementar-ne significativament la longevitat.[33] Se sap que l'homòleg mamífer de SIR-2 indueix factors de reparació de l'ADN en direcció 5′ implicats en l'NHEJ, una activitat que és especialment promoguda en condicions de restricció calòrica.[34] La restricció calòrica ha estat relacionada estretament amb la velocitat de la reparació per excisió de bases en l'ADN nuclear dels rosegadors,[35] tot i que no s'han observat efectes similars en l'ADN mitocondrial.[36]
De manera interessant, el gen AGE-1 de C. elegans, un efector en direcció 5′ de les rutes de reparació de l'ADN, confereix una longevitat dràsticament augmentada en condicions d'alimentació lliure però causa una reducció de l'aptitud reproductiva en condicions de restricció calòrica.[37] Aquesta observació recolza la teoria pleotròpica dels orígens biològics de l'envelliment, que suggereix que els gens que confereixen un gran avantatge evolutiu al principi de la vida seran afavorits per la selecció natural encara que comportin un desavantatge corresponent en un moment posterior de la vida.
Medicina i modulació de la reparació de l'ADN
[modifica]Trastorns hereditaris de la reparació de l'ADN
[modifica]Els defectes en el mecanisme de NER són els responsables de diversos trastorns genètics, incloent-hi:
- xerodèrmia pigmentada: hipersensibilitat a la llum solar i la llum ultraviolada, resultant en una major incidència de càncer de pell i un envelliment prematur
- síndrome de Cockayne: hipersensibilitat a la llum ultraviolada i als productes químics
- tricotiodistròfia: pell sensible, pèl i ungles fràgils
Els dos últims trastorns solen anar acompanyats de retardament mental, cosa que suggereix una major vulnerabilitat de les neurones del desenvolupament.
Altres trastorns de la reparació de l'ADN:
- síndrome de Werner: envelliment prematur i creixement retardat
- síndrome de Bloom: hipersensibilitat a la llum solar, alta incidència de càncers (especialment leucèmia)
- atàxia telangièctasi: sensibilitat a la radiació ionitzant i alguns productes químics
Aquestes malalties reben sovint el nom de "progèries segmentals" ("malalties d'envelliment accelerat"), car els malalts tenen un aspecte envellit i pateixen de malalties relacionades amb l'envelliment a edats anormalment joves.
Altres malalties associades amb un funcionament inapropiat de la reparació de l'ADN inclouen la malaltia de Fanconi, el càncer de pit hereditari i el càncer de còlon hereditari.
La reparació de l'ADN i el càncer
[modifica]Les mutacions heretades que afecten els gens de reparació de l'ADN estan fermament associades amb un elevat risc de càncer en els humans. El càncer colorectal hereditari no associat a poliposi (HNPCC) està fermament associat a mutacions específiques de la ruta de reparació de malaparellament de l'ADN. BRCA1 i BRCA2, dues cèlebres mutacions que confereixen un risc molt elevat de càncer de pit en les seves portadores, estan associades amb un gran nombre de rutes de reparació de l'ADN, especialment l'NHEJ i la recombinació homòloga.
Procediments de teràpia del càncer com ara la quimioteràpia i la radioteràpia funcionen aclaparant la capacitat de les cèl·lules de reparar els danys a l'ADN, resultant en la seva mort. Les cèl·lules que es divideixen més ràpidament (generalment les cèl·lules canceroses) són preferentment afectades. L'efecte secundari és que altres cèl·lules no canceroses però que es divideixen ràpidament, com ara les cèl·lules mare de la medul·la òssia, també són afectades. Els tractaments moderns del càncer intenten detectar els danys a l'ADN en cèl·lules i teixits únicament associats amb el càncer, o bé per mitjans físics (concentrant l'agent terapèutic a la regió del tumor) o bé per mitjans químics (aprofitant alguna característica única de les cèl·lules canceroses del cos).
Evolució
[modifica]Els processos bàsics de la reparació de l'ADN estan extensament conservats entre els procariotes, els eucariotes i fins i tot els bacteriòfags (virus que infecten bacteris); tanmateix, els organismes més complexos, amb genomes més complexos, tenen mecanismes de reparació corresponentment més complexos.[38] La capacitat d'un gran nombre de motius estructurals proteics de catalitzar reaccions químiques rellevants ha tingut un paper significatiu en l'elaboració de mecanismes de reparacio durant l'evolució.[39]
El registre fòssil indica que la vida unicel·lular començà a proliferar a la Terra en algun punt del període Precambrià, tot i que és incert en quin moment aparegueren per primer cop formes de vida recognoscibles com a modernes. Els àcids nucleics esdevingueren el mitjà únic i universal de codificació d'informació genètica, necessitant mecanismes de reparació de l'ADN que han estat heretats en la seva forma bàsica per totes les formes de vida vivents del seu avantpassat comú. L'aparició de l'atmosfera rica en oxigen de la Terra (coneguda com a catàstrofe de l'oxigen) a causa dels organismes fotosintètics, així com la presència de radicals lliures potencialment perjudicials dins la cèl·lula a causa de la fosforilació oxidativa, requerí l'evolució de mecanismes de reparació de l'ADN que es dediquen específicament a contrarestar els tipus de danys causats per l'estrès oxidatiu.
Velocitat del canvi evolutiu
[modifica]A vegades, els danys a l'ADN no són reparats, o són reparats per un mecanisme propens als errors, resultant en canvis respecte a la seqüència original. Quan passa això, les mutacions poden estendre's al genoma de la descendència de la cèl·lula. Si això es produeix en una cèl·lula de línia germinal que finalment produirà un gàmeta, la mutació té potencial per ser transmesa a la descendència de l'organisme. La velocitat de l'evolució en una espècie particular (o, a un nivell més baix, en un gen determinat) és una funció de la velocitat de mutació. Per tant, la velocitat i la precisió dels mecanismes de reparació de l'ADN influeixen en el procés de canvi evolutiu.[40]
Referències
[modifica]- ↑ «Nature Reviews Series: DNA damage» (en anglès). Nature Reviews Molecular Cell Biology, 05-07-2017 [Consulta: 7 novembre 2018].
- ↑ 2,0 2,1 Lodish, H.; Berk, A.; Matsudaira, P.; Kaiser, C. A.; Krieger, M.; Scott, M. P.; Zipursky, S. L.; Darnell, J.. Molecular Biology of the Cell (en anglès). 5a edició. Nova York: W. H. Freeman, 2004, p. 963.
- ↑ Acharya, P. V. «The isolation and partial characterization of age-correlated oligo-deoxyribo-ribonucleotides with covalently linked aspartyl-glutamyl polypeptides» (en anglès). Johns Hopkins Medical Journal. Supplement, 1, 1971, pàg. 254–260. PMID: 5055816.
- ↑ Bjorksten, J.; Acharya, P. V.; Ashman, S.; Wetlaufer, D. B. «Gerogenic fractions in the tritiated rat» (en anglès). Journal of the American Geriatrics Society, 19, 7, 1971, pàg. 561–74. DOI: 10.1111/j.1532-5415.1971.tb02577.x. PMID: 5106728.
- ↑ Browner W. S., Kahn A. J., Ziv E., Reiner A. P., Oshima J., Cawthon R. M., Hsueh W. C., Cummings S. R. «The genetics of human longevity». Am J Med, 117, 11, 2004, pàg. 851–60. DOI: 10.1016/j.amjmed.2004.06.033. PMID: 15589490.
- ↑ Roulston A., Marcellus R. C., Branton P. E. «Viruses and apoptosis». Annu. Rev. Microbiol., 53, 1999, pàg. 577–628. DOI: 10.1146/annurev.micro.53.1.577. PMID: 10547702 [Consulta: 20 desembre 2008].[Enllaç no actiu]
- ↑ Ohta T., Tokishita S., Mochizuki K., Kawase J., Sakahira M., Yamagata H. «UV Sensitivity and Mutagenesis of the Extremely Thermophilic Eubacterium Thermus thermophilus HB27» (PDF). Genes and Environment, 28, 2, 2006, pàg. 56–61. DOI: 10.3123/jemsge.28.56 [Consulta: 14 octubre 2024].
- ↑ Braig M., Schmitt C. A. «Oncogene-induced senescence: putting the brakes on tumor development». Cancer Res, 66, 2006, pàg. 2881–2884. DOI: 10.1158/0008-5472.CAN-05-4006. PMID: 16540631.
- ↑ Lynch M. D. «How does cellular senescence prevent cancer?». DNA Cell Biol, 25, 2, 2006, pàg. 69–78.
- ↑ Sancar A. «Structure and function of DNA photolyase and cryptochrome blue-light photoreceptors». Chem Rev, 103, 6, 2003, pàg. 2203-37. DOI: 10.1021/cr0204348. PMID: 12797829.
- ↑ 11,0 11,1 11,2 Watson J. D., Baker T. A., Bell S. P., Gann A., Levine M., Losick R.. Molecular Biology of the Gene. 5a ed. Peason Benjamin Cummings; CSHL Press, 2004. Vegeu els capítols «9. The Mutability and Repair of DNA» i «10. Homologous Recombination at the Molecular Level».
- ↑ Volkert M. R. «Adaptive response of Escherichia coli to alkylation damage». Environ Mol Mutagen, 11, 2, 1988, pàg. 241-55. DOI: 10.1002/em.2850110210. PMID: 3278898.
- ↑ Wilson T. E., Grawunder U., i Lieber M. R. «Yeast DNA ligase IV mediates non-homologous DNA end joining». Nature, 388, 1997, pàg. 495–498. DOI: 10.1038/41365. PMID: 9242411.
- ↑ Moore J. K., Haber J. E. «Cell cycle and genetic requirements of two pathways of nonhomologous end-joining repair of double-strand breaks in Saccharomyces cerevisiae». Mol Cell Biol, 16, 5, 1996, pàg. 2164–73. DOI: 10.1128/MCB.16.5.2164. PMC: 231204. PMID: 8628283 [Consulta: 14 octubre 2024].
- ↑ Boulton S. J., Jackson S. P. «Saccharomyces cerevisiae Ku70 potentiates illegitimate DNA double-strand break repair and serves as a barrier to error-prone DNA repair pathways». EMBO J., 15, 18, 1996, pàg. 5093-103. PMC: 452249. PMID: 8890183 [Consulta: 14 octubre 2024].
- ↑ Wilson T. E., i Lieber M. R. «Efficient processing of DNA ends during yeast nonhomologous end joining. Evidence for a DNA polymerase beta (Pol4)-dependent pathway». J. Biol. Chem., 274, 1999, pàg. 23599–609. DOI: 10.1074/jbc.274.33.23599. PMID: 10438542 [Consulta: 14 octubre 2024].
- ↑ Budman J, Chu G. «Processing of DNA for nonhomologous end-joining by cell-free extract». EMBO J., 24, 4, 2005, pàg. 849-60. DOI: 10.1038/sj.emboj.7600563. PMC: 549622. PMID: 15692565 [Consulta: 14 octubre 2024].
- ↑ Wang H., Perrault A. R., Takeda Y., Qin W., Wang H., Iliakis G. «Biochemical evidence for Ku-independent backup pathways of NHEJ». Nucleic Acids Res, 31, 18, 2003, pàg. 5377–88. DOI: 10.1093/nar/gkg728. PMC: 203313. PMID: 12954774 [Consulta: 14 octubre 2024].
- ↑ Jung D., Alt F. W. «Unraveling V(D)J recombination; insights into gene regulation». Cell, 116, 2, 2004, pàg. 299–311. DOI: 10.1016/s0092-8674(04)00039-x. PMID: 14744439 [Consulta: 14 octubre 2024].
- ↑ Zahradka K., Slade D., Bailone A., Sommer S., Averbeck D., Petranovic M., Lindner A. B., Radman M. «Reassembly of shattered chromosomes in Deinococcus radiodurans». Nature, 443, 7111, 2006, pàg. 569–573. DOI: 10.1038/nature05160. PMID: 17006450.
- ↑ 21,0 21,1 21,2 Friedberg E. C., Walker G. C., Siede W., Wood R. D., Schultz R. A., Ellenberger T.. DNA Repair and Mutagenesis, part 3.. 2a ed. ASM Press, 2006.
- ↑ Bakkenist C. J., Kastan M. B. «DNA damage activates ATM through intermolecular autophosphorylation and dimer dissociation». Nature, 30, 421, pàg. 499–506. DOI: 10.1038/nature01368. PMID: 12556884.
- ↑ Wei, Qingyi; Lei Li, David Chen. DNA Repair, Genetic Instability, and Cancer. World Scientific, 2007. ISBN 9812700145.
- ↑ Schonthal, Axel H. Checkpoint Controls and Cancer. Humana Press, 2004. ISBN 1588295001.
- ↑ Janion C. «Some aspects of the SOS response system – a critical survey». Acta Biochim Pol, 48, 3, 2001, pàg. 599–610. PMID: 11833768.
- ↑ Schlacher K., Pham P., Cox M. M., Goodman M. F. «Roles of DNA Polymerase V and RecA Protein in SOS Damage-Induced Mutation». Chem. Rev, 106, 2, 2006, pàg. 406–419. DOI: 10.1021/cr0404951. PMID: 16464012.
- ↑ Fry R. C., Begley T. J., Samson L. D. «Genome-wide responses to DNA-damaging agents». Annu Rev Microbiol., 59, 2004, pàg. 357–77. DOI: 10.1146/annurev.micro.59.031805.133658. PMID: 16153173.
- ↑ Espejel S., Martin M., Klatt P., Martin-Caballero J., Flores J. M., Blasco M. A. «Shorter telomeres, accelerated ageing and increased lymphoma in DNA-PKcs-deficient mice». EMBO Rep, 5, 5, 2004, pàg. 503–9. DOI: 10.1038/sj.embor.7400127. PMC: 1299048. PMID: 15105825 [Consulta: 14 octubre 2024].
- ↑ de Boer J., Andressoo J. O., de Wit J., Huijmans J., Beems R. B., van Steeg H., Weeda G., van der Horst G. T., van Leeuwen W., Themmen A. P., Meradji M., Hoeijmakers J. H. «Premature aging in mice deficient in DNA repair and transcription». Science, 296, 5571, 2002, pàg. 1276–9. DOI: 10.1126/science.1070174. PMID: 11950998.
- ↑ Dolle M. E., Busuttil R. A., Garcia A. M., Wijnhoven S., van Drunen E., Niedernhofer L. J., van der Horst G., Hoeijmakers J. H., van Steeg H., Vijg J. «Increased genomic instability is not a prerequisite for shortened lifespan in DNA repair deficient mice». Mutation Research, 596, 1-2, 2006, pàg. 22–35. DOI: 10.1016/j.mrfmmm.2005.11.008. PMID: 16472827.
- ↑ Kobayashi Y., Narumi I., Satoh K., Funayama T., Kikuchi M., Kitayama S., Watanabe H. «Radiation response mechanisms of the extremely radioresistant bacterium Deinococcus radiodurans». Biol Sci Space, 18, 3, 2004, pàg. 134–5. PMID: 15858357.
- ↑ Spindler S. R. «Rapid and reversible induction of the longevity, anticancer and genomic effects of caloric restriction». Mech Ageing Dev, 126, 9, 2005, pàg. 960–6. DOI: 10.1016/j.mad.2005.03.016. PMID: 15927235.
- ↑ Tissenbaum H. A., Guarente L. «Increased dosage of a sir-2 gene extends lifespan in Caenorhabditis elegans». Nature, 410, 6825, 2001, pàg. 227–30. DOI: 10.1038/35065638. PMID: 11242085.
- ↑ Cohen H. Y., Miller C., Bitterman K. J., Wall N. R., Hekking B., Kessler B., Howitz K. T., Gorospe M., de Cabo R., Sinclair D. A. «Calorie restriction promotes mammalian cell survival by inducing the SIRT1 deacetylase». Science, 305, 5682, 2004, pàg. 390–2. DOI: 10.1126/science.1099196. PMID: 15205477.
- ↑ Cabelof D. C., Yanamadala S., Raffoul J. J., Guo Z., Soofi A., Heydari A. R. «Caloric restriction promotes genomic stability by induction of base excision repair and reversal of its age-related decline». DNA Repair [Amsterdam], 2, 3, 2003, pàg. 295–307. DOI: 10.1016/s1568-7864(02)00219-7. PMID: 12547392.
- ↑ Stuart J. A., Karahalil B., Hogue B. A., Souza-Pinto N. C., Bohr V. A. «Mitochondrial and nuclear DNA base excision repair are affected differently by caloric restriction». FASEB J, 18, 3, 2004, pàg. 595–7. DOI: 10.1096/fj.03-0890fje. PMID: 14734635.
- ↑ Walker D. W., McColl G., Jenkins N. L., Harris J., Lithgow G. J. «Evolution of lifespan in C. elegans». Nature, 405, 6784, 2000, pàg. 296–7. DOI: 10.1038/35012693. PMID: 10830948.
- ↑ Cromie G. A., Connelly J. C., Leach D. R. «Recombination at double-strand breaks and DNA ends: conserved mechanisms from phage to humans». Mol Cell., 8, 6, 2001, pàg. 1163–74. DOI: 10.1016/s1097-2765(01)00419-1. PMID: 11779493 [Consulta: 14 octubre 2024].
- ↑ O'Brien P. J. «Catalytic promiscuity and the divergent evolution of DNA repair enzymes». Chem Rev, 106, 2, 2006, pàg. 720–52. DOI: 10.1021/cr040481v. PMID: 16464022.
- ↑ Maresca B., Schwartz J. H. «Sudden origins: a general mechanism of evolution based on stress protein concentration and rapid environmental change». Anat Rec B New Anat., 289, 1, 2006, pàg. 38–46. DOI: 10.1002/ar.b.20089. PMID: 16437551 [Consulta: 14 octubre 2024].
Vegeu també
[modifica]Enllaços externs
[modifica]- Trastorns de la reparació de l'ADN en els humans (anglès)
- Danys a l'ADN i reparació de l'ADN (anglès)