Kaliumtetrachloroaurat(III)
 Van Wikipedia, de gratis encyclopedie
Van Wikipedia, de gratis encyclopedie
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
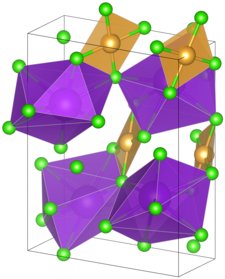 | |||||||||||||||||||
| _ K+ _ Au3+ _ Cl− | |||||||||||||||||||
| Kristallsystem | |||||||||||||||||||
| Raumgruppe | Pc (Nr. 7) | ||||||||||||||||||
| Gitterparameter |
| ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kaliumtetrachloroaurat(III) | ||||||||||||||||||
| Andere Namen | Goldchloridkalium | ||||||||||||||||||
| Verhältnisformel | K[AuCl4] | ||||||||||||||||||
| Kurzbeschreibung | gelb-oranges Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 377,86 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||
| Schmelzpunkt | 300 °C[2] | ||||||||||||||||||
| Löslichkeit | löslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Kaliumtetrachloroaurat, K[AuCl4] ist eine anorganische Verbindung der Tetrachlorogoldsäure mit dem Alkalimetall Kalium.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Kaliumtetrachloroaurat ist ein geruchsloses, gelb-oranges Pulver. Die Verbindung ist unter Normalbedingungen stabil und lichtempfindlich.[1] Der Schmelzpunkt liegt bei ca. 300 °C.[2] Das Kaliumsalz besitzt ein monoklines Kristallsystem mit der Raumgruppe Pc (Raumgruppen-Nr. 7). Die Gitterparameter liegen bei a = 8,671 Å, b = 6,386 Å und c = 12,243 Å. Der Gradzahl des β-Winkels beträgt 95,37°.[3]
Verwendung[Bearbeiten | Quelltext bearbeiten]
In Tonbad ist unter anderem Kaliumtetrachloroaurat(III) enthalten. Die Lösung wird zur Behandlung von Albuminpapier verwendet.
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Das Salz verursacht bei Kontakt mit der Haut, den Augen oder den Atemwegen Reizungen. Die Chemikalie sollte nicht verschluckt werden, da Schäden auftreten können.[2]
Kaliumtetrachloroaurat reagiert heftig mit Ammoniak NH3, starken Oxidationsmitteln und pulverförmigen Metallen. Bei der Verbrennung des Stoffes kann unter anderem Chlorwasserstoff entstehen.[1]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c Eintrag zu Potassium tetrachloroaurate(III) bei Thermo Fisher Scientific, abgerufen am 13. Oktober 2023.
- ↑ a b c d e f Datenblatt Kaliumtetrachloroaurat(III) (PDF) bei Carl Roth, abgerufen am 2. Februar 2019.
- ↑ M. Bonamico, G. Dessy: The crystal structure of anhydrous potassium tetrachloroaurate(III). In: Acta Cryst. 1973, S. 1735–1736, doi:10.1107/S0567740873005406.
