Fluorescéine

| Fluorescéine | |
 | |
| Identification | |
|---|---|
| Synonymes | C.I. 45350 |
| No CAS | (acide) (sel de Na) |
| No ECHA | 100.017.302 |
| No CE | 219-031-8 208-253-0 (Na) |
| Code ATC | S01 |
| PubChem | 16850 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C20H12O5 [Isomères] |
| Masse molaire[1] | 332,306 3 ± 0,018 3 g/mol C 72,29 %, H 3,64 %, O 24,07 %, |
| Propriétés physiques | |
| T° fusion | 315 °C (décomposition)[réf. souhaitée] |
| Propriétés optiques | |
| Spectre d’absorption | λmax 494 nm[2] |
| Précautions | |
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
La fluorescéine (C20H12O5 ou 3H-xanthène-3-one), dont le sel de sodium se nomme fluorescéine sodique ou uranine (C20H10Na2O5), est un composé organique dont la structure comporte deux molécules de phénol liées à un cycle pyrane lui-même connecté en position ortho à un acide benzoïque. Cette substance acide dérivée du xanthène se caractérise par une fluorescence intense d'où elle tire son nom. Tandis que la fluorescéine solide est une poudre brun rougeâtre, les solutions aqueuses sont rouges lorsqu'elles sont vues par transparence mais réfléchissent la lumière blanche dans une teinte vert « fluo ».
Synthèse chimique
[modifier | modifier le code]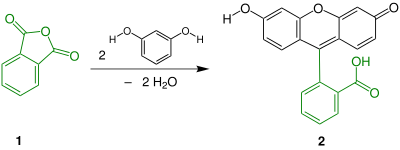
Cette substance a été découverte et synthétisée par Adolf von Baeyer en 1871. Von Baeyer nommera sa découverte « Fluorescein » car il remarque l'importante fluorescence verte, même lorsque le produit est très dilué[3]. Le nom resorcinphthalein sera également utilisé, puisque synthétisée à partir de résorcine et d'anhydride phtalique[4]. Le sel disodique de la fluorescéine est souvent appelé « uranine »[5], car sa couleur rappelle celle de l'ouraline, un verre contenant une faible quantité d'uranium[4].
Usages
[modifier | modifier le code]

Hydrophilie
[modifier | modifier le code]Le caractère hydrophile de la fluorescéine est utilisé dans différents domaines pour colorer l'eau.
Hydrogéologie
[modifier | modifier le code]
Sa couleur étant visible même à faible dose, la fluorescéine est utilisée pour tracer les cours d'eau souterrains, des résurgences, des fuites, etc.
Réseaux d'eaux usées
[modifier | modifier le code]De la même façon, la fluorescéine est utilisée pour les tests sur les réseaux d'eaux usées, pour retrouver le cheminement de réseaux mal connus, identifier les inversions entre réseaux d'eaux usées et pluviales, etc.
Recherche de fuite
[modifier | modifier le code]En recherche de fuite, la fluorescéine est appréciée car elle permet de mettre en évidence tout type de défaut d'étanchéité ou d'infiltration d'eau, que ce soit sur une menuiserie, une étanchéité bitumineuse, une fissure de maçonnerie, un joint de baignoire, etc.
Suivi d'évacuation d'eau de centrales géothermiques
[modifier | modifier le code]Les centrales géothermiques utilisent la fluorescéine pour suivre la propagation des courants d'eau chaude expulsés dans la mer. La centrale géothermique de Bouillante en Guadeloupe utilise cet élément pour vérifier que des sources d'eau chaude détectées en bord de mer sont bien naturelles et non des eaux réchauffées par la sortie de la centrale toute proche.
Industriel
[modifier | modifier le code]Elle permet de détecter la présence de fuites sur des circuits hydrauliques (huile et carburant) complexes, notamment sur les engins à transmission hydraulique (vérin, raccord…).
Sécurité maritime
[modifier | modifier le code]Elle est également utilisée comme moyen de signalisation de secours facilement transportable sur des embarcations de navigation. En cas de nécessité, la tache formée par le produit facilite grandement la détection aérienne, notamment pour des petites embarcations (kayak de mer…).

Domaine médical
[modifier | modifier le code]Elle est utilisée dans certains médicaments (ex. : éosine).
En biologie moléculaire, elle sert à confectionner des sondes pour les hybridations in situ en fluorescence (ou FISH), la PCR en temps réel et l'hybridation génomique comparative.
En ophtalmologie, elle a été très utilisée en injection, pour les angiographies du fond de l'œil en fluorescence, mais en , l'Agence française de sécurité sanitaire des produits de santé (Afssaps) a imposé en accord avec le fabricant la suspension de l'AMM de cette spécialité et le retrait de tous les lots de solution injectable de Fluorescéine Sodique Faure à 20 %, en raison de réactions d'hypersensibilité sévères plus fréquentes avec la fluorescéine à 20 % qu'avec la fluorescéine à 10 % (qui reste autorisée).
Au , 23 cas d'effets indésirables graves, dont cinq cas conclus par la mort du patient, ont été signalés en France avec le remplacement de la fluorescéine par la spécialité AK-Fluor[6]. Les effets secondaires bénins observés sont (isolés ou associés) :
- nausées transitoires avec vomissements (fréquent) ;
- malaise et démangeaisons, éruption cutanée ou urticaire généralisé (plus rarement).
Des effets plus graves peuvent parfois suivre ces symptômes mineurs d'allergie, dans les minutes ou heures suivant l'injection :
- baisse de tension artérielle ;
- œdème de Quincke, manifestations respiratoires (crise d'asthme, détresse respiratoire) ;
et plus rarement :
- chutes brutales de tension artérielle, amenant un état de choc avec éventuelle défaillance cardiaque ;
- troubles cardiaques (arrêt cardiaque, infarctus du myocarde ; exemple : une mort par arrêt cardiaque, suivant l'injection de cinq millilitres de fluorescéïne à 5 % pour une angiographie, est décrite par le journal JAMA en 1979) ;
- troubles neurologiques (convulsions, coma, accident vasculaire cérébral).
Une réaction inflammatoire et douleur locale peuvent résulter d'une diffusion du produit hors de la veine durant l'injection. Les conjonctives, la peau et les urines sont temporairement jaune fluorescent quelques heures après l'examen.
On l'utilise également lors de l'examen de la cornée pour visualiser les lésions de celle-ci : abrasions ou perforation (positivant le signe de Seidel).
En chirurgie, elle peut aider à planifier (en mode préopératoire) plus efficacement des incisions de tissus mous nécrosés, en mettant en évidence la perfusion tissulaire. Elle peut aussi améliorer la prise en charge postopératoire d'infections nécrosantes. Dans les années 1980, un instrument médical dédié à l'évaluation du flux sanguin cutané en fonction de l'apport cutané de fluorescéine sodique est le « dermofluoromètre numérique »[7].
Pour les usages médicaux, en raison du risque rare mais grave d'épilepsie et/ou de choc anaphylactique, la fluorescéine est maintenant souvent remplacée par le vert d'indocyanine (ou ICG, indocyanine green (en)). Le nom commercial de ce produit sur le marché français est « Infracyanine ».
Biologie moléculaire
[modifier | modifier le code]La fluorescéine sert de donneur dans la confection de sondes de PCR en temps réel.
Sécurité, toxicologie, écotoxicologie
[modifier | modifier le code]Toxicologie
[modifier | modifier le code]Des effets indésirables (bénins à mortels) sont signalés pour 1 % à 6 % des utilisateurs selon les études[8],[9],[10],[11]. Des taux plus élevés pourraient refléter des cas susceptibles d'avoir été plus exposés ou ayant déjà présenté des effets indésirables similaires (allergies…). Le risque de réaction indésirable est 25 fois plus élevé si la personne a déjà eu une réaction indésirable[10]. Inversement ce risque diminue chez les personnes ayant antérieurement utilisé (prophylactiquement) des antihistaminiques[12],[13]. Un simple test de piqûre peut aider à identifier les personnes les plus à risque de réaction indésirable[11].
Chez l'humain, en 2006, l'application sur la peau était réputée sûre[14] ; l'injection intradermique peut provoquer des démangeaisons ou des douleurs légères. Et en intraveineuse surtout (mais des inductions orales ou topique ont aussi été signalées), la fluorescéine peut provoquer plusieurs effets indésirables dont des nausées, des vomissements, de l'urticaire, une hypotension aiguë, un malaise vagal, une anaphylaxie voire un choc anaphylactique[15] pouvant entrainer un arrêt cardiaque[14],[16] ou une mort rapide par choc anaphylactique[17],[18].
- La nausée : c'est le symptôme le plus courant. Il est supposé induit par la différence entre le pH intra corporel et le pH du colorant à la fluorescéine de sodium. Aux doses médicamenteuses, elle est généralement transitoire et disparaît rapidement.
- L'urticaire : il peut être mineur à grave. C'est un indice à prendre au sérieux car pouvant signer un début d'anaphylaxie mortelle (il est facilement soulagé par une seule dose d'antihistaminique qui doit être administrée rapidement).
- Crise d'épilepsie généralisée tonico-clonique ; elle est rare mais dangereuse[19],[20], survenant à la suite d'une application intrathécale visant à diagnostiquer une perte de liquide céphalo-rachidien[21] (par exemple à la suite d'un récent traumatisme ou à une intervention chirurgicale sur la zone crânienne[22]). Les effets épileptiques semblent dose-dépendants, et seront transitoires si le taux de fluorescéine injecté est dilué à moins de 5 % ; le risque peut être minimisé en respectant les précautions générales de dose et les bonnes pratiques de ponction lombaire. Pour Rainer Keerl et al. (2009), « Le patient doit être surveillé pendant 24 heures. Un consentement éclairé écrit des patients pour l'utilisation de la fluorescéine est recommandé »[23].
- Le choc anaphylactique : décrit depuis au moins 1950[24] ; rare, il peut survenir en quelques minutes. Les professionnels de santé utilisant de la fluorescéine en injection doivent être prêts à effectuer une réanimation d'urgence.
On évoque souvent les anaphylaxies induites par une injection intraveineuse de fluorescénine, mais des cas d'origine orale ou topique sont également possibles[25],[26] (dont dans un cas d'anaphylaxie avec arrêt cardiaque (ressuscité) après une utilisation topique dans un simple collyre)[16].
Mutagénicité ? Des études ont signalé un éventuel caractère mutagène ou une possible activation photodynamique de plusieurs colorants alimentaires ou cosmétiques (dont coloration pour cheveux) à base de fluorescéine[27] ; plusieurs de ces produits ont ensuite (publication de 1981) été testés sur de l'ADN bactérien (bacterial DNA-repair tests) pour ces deux aspects (activation photochimique et/ou mutagénicité intrinsèque) : 2,4,5,7-tétraiodofluorescéine, sel disodique (érythrosine) ; phloxines (2,4,5,7-tétrabromo-12,15-dichlorofluorescéine ; sel dipotassique et sel disodique du 2,4,5,7-tétraiodo-12,15-dichlorofluorescéine) a été testé (avec et sans éclairage à partir d'une lampe fluorescente à la lumière du jour)[27]. Résultats : l'érythrosine était inactive dans toutes les conditions et les deux colorants à base de phloxine ont été actifs dans un essai mais uniquement en l'absence de métabolisation. Les tests de réparation de l'ADN bactérien n'étant pas à cette époque considérés comme fiable à 100 %, après cette étude le doute persistait encore sur la génotoxicité possible de certains de ces colorants[27].
Remarques :
- aux doses où elle est injectée comme fluorophore (associé à un « ligand de ciblage ») dans certains outils pour diagnostiquer le cancer in vivo, la fluorescéine n'atteint pas les seuils de toxicité calculés pour l'obtention d'autorisation de la FDA[28] ;
- de nombreux tests toxicologiques sont basés sur la fluorescence. Or, il existe des interactions de tous les nanomatériaux (ou nanomédicaments ?) avec la plupart des tests de dépistage fluorimétrique in vitro, dont en inhibant l'émission de fluorescence du colorant fluorescéine[29].
Écotoxicité
[modifier | modifier le code]L'écotoxicité est encore discutée et pourrait varier selon les taxons, l'âge des organismes, la durée et concentration d'exposition, des synergies avec d'autres composés ou polluants, etc. Son écotoxicité directe aux faibles doses habituellement rencontrées dans les expériences de traçage de l'eau est réputée faible. La toxicité de ses produits de dégradation (qui pourraient être plus toxiques que la molécule-mère) n'est étudiée que depuis peu (Gombert et al., 2017, cités par C.J. Cooksey en 2017)[30]. Les différentes formes de la fluorescéine sont dégradées par la lumière et par certains microorganismes (de l'eau, du sédiment ou du sol) ; la mesure de l'hydrolyse du diacétate de fluorescéine dans un échantillon de sol ou de sédiment est d'ailleurs parfois utilisée pour mesurer l'activité microbienne totale dans ces substrats[31]. Comme l'hydrolyse complète du diacétate de fluorescéine nécessite les trois principaux groupes d'enzymes (estérases, protéases et lipases), le dosage hydrolytique du diacétate de fluorescéine (FDAase) a été proposé comme mesure holistique de l'activité microbienne totale, par Schnürer et Rosswall en 1982[32].
De nombreux tests basiques d'écotoxicité (aiguë à chronique) sont basés sur les effets des molécules testées sur un microcrustacé (filtreur) aquatique d'eau douce très commun : la daphnie (Daphnia pulex)[33]. En écotoxicologie, un paramètre important est la reprotoxicité[33].
Pour une exposition chronique de dix jours à la fluorescéine en condition « statique », on constate une baisse (dose-dépendante) du nombre moyen de descendants viables produits par les daphnies exposées[33]. Sans tuer les adultes, cette molécule peut affecter le potentiel reproducteur d'organismes exposés. Cependant selon Walthall et Stark (1991), quand le produit est fortement dilué dans l'eau, « le risque qu'ils représentent pour des populations sauvages après des applications à grande échelle semble minime », d'autant que le colorant se décompose assez vite quand il est exposé à la lumière solaire[33].
La fluorescéine se lie aux protéines, y compris dans certains tissus vivants mis à vif (on utilise même cette propriété pour détecter des lésions cornéennes[34] et des ulcères cutanés chez des poissons d'élevage (dont par exemple la truite arc-en-ciel (Oncorhynchus mykiss), le poisson-chat (Ictalurus punctatus), le poisson rouge (Carassius auratus) et le bar rayé hybride (Morone saxatilis mâle X Morone chrysops femelle))[35]. Des doses infimes dans l'eau (0,10 mg/ml d'eau durant trois minutes suffisent) rendent visibles avec précision des lésions et ulcérations de la peau du poisson invisibles à l'œil nu ; des poissons apparemment cliniquement sains révèlent ainsi des ulcérations traduisant des blessures lors de leur manipulation, des parasitoses, etc.[35]. Une autre étude, sur le Tilapia du Nil (Oreochromis niloticus) et le poisson-chat à petites écailles (Clarias gariepinus), a conclu que ce colorant est inoffensif pour le Tilapia du Nil jusqu'à 0,5 mg de fluorescéine/ml d'eau pour une exposition de moins de 15 min, 0,10 mg/ml durant 5 min suffisant à détecter des abrasions cutanées très petites.
Pour faciliter la manipulation nécessaire au bilan clinique des poissons, ceux-ci sont souvent endormis avec de la tricaïne (mésylate de tricaïne), or cet anesthésique (le plus utilisé) interagit avec la fluorescéine : il peut d'une part causer des dommages importants aux poissons, et d'autre part « éteindre la fluorescence émise par la fluorescéine retenue dans les ulcères cutanés », et donc fausser le test par des faux-négatifs ; ceci a été démontré chez le flétan du Pacifique (Hippoglossus stenolepis), le goberge du Groenland (Theragra chalcogramma) et la sole nordique (Lepidopsetta polyxystra) en examinant la fluorescence des lésions épidermiques induites expérimentalement.
Une expérience a consisté à exposer des bars d'élevage sains ou expérimentalement ulcérés à une dose « élevée » de fluorescéine dans leur eau, ce qui, selon les deux auteurs de l'expérience n'a pas eu d'effet apparent sur leur santé ou survie à court terme[35].
En tant que traceur d'eaux souterraines très utilisé (en zone karstique notamment), cette molécule peut réapparaître à des concentrations encore significativement élevées dans des sources hydrauliquement situées en aval du point d'injection où peuvent vivre des espèces rares, menacées ou protégées[36]. En 2012, une étude a testé sa toxicité (en expositions statiques de 24[Quoi ?], et à diverses concentrations) pour l'escargot menacé Taylorcocha serpenticola via une « espèce de substitution », l'escargot cendré Fluminicola fuscus (avec des témoins sans fluorescéine à des températures similaires à celles de l'habitat concerné)[36]. La concentration létale médiane était de 377 mg/L pour l'espèce de substitution ; ce qui laisse penser que les risques pour les mollusques en contact avec l'eau colorée sont « probablement faibles »[36].
Certaines fermes aquacoles consomment de grandes quantités d'eau douce ou d'eau de mer « souterraines ». Elles ont besoin de mieux comprendre l'état et les mouvements de cette ressource souterraine, en utilisant entre autres des colorants fluorescents comme la fluorescéine. Ce faisant, des poissons ou crevettes d'élevage peuvent y être ponctuellement exposés[37]. Dans ce contexte, la toxicité aiguë de la fluorescéine a été évaluée pour le turbot (Scophthalmus maximus) aux concentrations de 0,5, 0,7, 0,9, 1,1 et 1,3 mg) à 14 °C durant 24, 48 ou 96 h. Résultat : la dose tuant 50 % des poissons (CL50) était de 997,1 ± 11,4 mg/L (moyenne ± écart type) après une exposition de 24, 48 ou 96 h. Le système nerveux central du turbot est affecté par la molécule[37] ; et l'autopsie montrait une coloration brun-vert de certains tissus avec congestion encéphalique. Cette CL50 laisse une large marge de sécurité aux doses attendues après dilution (<1 mg/L)[37].
Autre colorant
[modifier | modifier le code]La fluorescéine ne doit pas être confondue avec la pyoverdine[38] naturellement produite en très petite quantité par différents organismes vivants. La pyoverdine est un sidérophore notamment produit par certaines bactéries. Elle est parfois utilisée pour leur identification et caractérisation biologique et moléculaire, comme pour les Pseudomonas spp. fluorescents (dont Pseudomonas syringae) ou Xanthomonas fragariae (qui sont parfois phytopathogènes).
La pyoverdine est une toxine biologique, trouvée sous des formes chimiques légèrement différentes, à laquelle correspondent des récepteurs cellulaires (pouvant accepter différentes formes de pyoverdine). Elle pourrait avoir plusieurs fonctions encore mal comprises. Les pyoverdines ont une affinité chimique pour le fer ferrique (ion Fe3+) supérieure à celle de sidérophores produits par les champignons phytopathogènes, dont par les Fusarium (fusarinines), ce qui confère aux microbes en produisant un avantage compétitif ou adaptatif, leur permettant de devenir « antagonistes » d'autres groupes microbiens moins capables de capter ce fer lorsque sa disponibilité en est limitée.
Par mutations dirigées, des chercheurs ont produit des bactéries mutantes (P. syringae) ne produisant pas de pyoverdine ou ne l'incorporant pas. Ils ont montré que, comme l'enzyme nitrate réductase, la pyoverdine est impliquée dans la compétence rhizosphérique mais également tellurique (capacité à exploiter le sol comme habitat) de P. syringae C7R12 (qui a grâce à la nitrate réductase une compétence saprophyte lui permettant de respirer en conditions d'anoxie). On a montré par ailleurs à la fin des années 1990 que la pyoverdine produite par des bactéries était un bon ligand pouvant complexer d'autres métaux dont des actinides, sous certaines conditions de pH[39]. Un test HPLC a été développé au CRA-W belge, qui a confirmé chez plus de cinq cents souches de P. syringae la constance de la pyoverdine produite[40].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Zhu, H., Derksen, R., Krause, C., Fox, R. et Ozkhan, H., « Fluorescent Intensity of Dye Solutions under Different pH Conditions », Journal of ASTM international, vol. 2, , p. 1-6.
- (de) Adolf Baeyer, « Ueber eine neue Klasse von Farbstoffen », Berichte der deutschen chemischen Gesellschaft, vol. 4, no 2, , p. 555–558 (ISSN 0365-9496, DOI 10.1002/cber.18710040209, lire en ligne
 , consulté le )
, consulté le ) - (en) Christopher Cooksey, « Quirks of dye nomenclature. 9. Fluorescein », Biotechnic & Histochemistry, vol. 92, no 7, , p. 506–512 (ISSN 1052-0295 et 1473-7760, DOI 10.1080/10520295.2017.1359751, lire en ligne
 , consulté le )
, consulté le ) - « Fluorescéine sodique », Grosseron, consulté le 3 octobre 2023.
- Afssaps, Lettre aux prescripteurs.
- (en) Frederic S. Bongard, Virgil B. Elings et Robert E. Markison, « New uses of fluorescence in the surgical management of necrotizing soft tissue infection », The American Journal of Surgery, vol. 150, no 2, , p. 281–283 (DOI 10.1016/0002-9610(85)90139-4, lire en ligne, consulté le ).
- (en) Anthony SL Kwan, Chris Barry, Ian L McAllister et Ian Constable, « Fluorescein angiography and adverse drug reactions revisited: the Lions Eye experience », Clinical and Experimental Ophthalmology, vol. 34, no 1, , p. 33–38 (ISSN 1442-6404 et 1442-9071, DOI 10.1111/j.1442-9071.2006.01136.x).
- B. J. Jennings et D. E. Mathews, « Adverse reactions during retinal fluorescein angiography », Journal of the American Optometric Association, vol. 65, no 7, , p. 465–471 (ISSN 0003-0244, PMID 7930354, lire en ligne, consulté le ).
- K. A. Kwiterovich, M. G. Maguire, R. P. Murphy et A. P. Schachat, « Frequency of adverse systemic reactions after fluorescein angiography. Results of a prospective study », Ophthalmology, vol. 98, no 7, , p. 1139–1142 (ISSN 0161-6420, PMID 1891225, DOI 10.1016/s0161-6420(91)32165-1, lire en ligne, consulté le ).
- M. Matsuura, F. Ando, K. Fukumoto et I. Kyogane, « [Usefulness of the prick test for anaphylactoid reaction in intravenous fluorescein administration] », Nippon Ganka Gakkai Zasshi, vol. 100, no 4, , p. 313–317 (ISSN 0029-0203, PMID 8644545, lire en ligne, consulté le ).
- P. P. Ellis, M. Schoenberger et M. A. Rendi, « Antihistamines as prophylaxis against side reactions to intravenous fluorescein », Transactions of the American Ophthalmological Society, vol. 78, , p. 190–205 (ISSN 0065-9533, PMID 7257056, PMCID 1312139, lire en ligne, consulté le ).
- Chang-Sue Yang, Chun-Sung Sung, Fenq-Lih Lee et Wen-Ming Hsu, « Management of anaphylactic shock during intravenous fluorescein angiography at an outpatient clinic », Journal of the Chinese Medical Association: JCMA, vol. 70, no 8, , p. 348–349 (ISSN 1726-4901, PMID 17698436, DOI 10.1016/S1726-4901(08)70017-0, lire en ligne, consulté le ).
- (en) Ken-ichiro O'goshi et Jorgen Serup, « Safety of sodium fluorescein for in vivo study of skin », Skin Research and Technology, vol. 12, no 3, , p. 155–161 (ISSN 0909-752X et 1600-0846, DOI 10.1111/j.0909-752X.2006.00147.x).
- (en) « Preface », Journal of Allergy and Clinical Immunology, vol. 101, no 6, , S465 (DOI 10.1016/S0091-6749(18)30566-9, lire en ligne, consulté le ).
- N. el Harrar, B. Idali, S. Moutaouakkil et M. el Belhadji, « [Anaphylactic shock caused by application of fluorescein on the ocular conjunctiva] », Presse Medicale (Paris, France, 1983), vol. 25, no 32, , p. 1546–1547 (ISSN 0755-4982, PMID 8952662, lire en ligne, consulté le ).
- V. Fineschi, G. Monasterolo, R. Rosi et E. Turillazzi, « Fatal anaphylactic shock during a fluorescein angiography », Forensic Science International, vol. 100, nos 1-2, , p. 137–142 (ISSN 0379-0738, PMID 10356782, DOI 10.1016/s0379-0738(98)00205-9, lire en ligne, consulté le ).
- Masahito Hitosugi, Kazunobu Omura, Tomoko Yokoyama et Hitoshi Kawato, « An autopsy case of fatal anaphylactic shock following fluorescein angiography: a case report », Medicine, Science, and the Law, vol. 44, no 3, , p. 264–265 (ISSN 0025-8024, PMID 15296251, DOI 10.1258/rsmmsl.44.3.264, lire en ligne, consulté le ).
- (en) Sarika Juneja et Kavita Sandhu, « Fluoroscein toxicity – Rare but dangerous », Indian Journal of Anaesthesia, vol. 63, no 8, , p. 674 (ISSN 0019-5049, PMID 31462817, PMCID PMC6691649, DOI 10.4103/ija.IJA_164_19, lire en ligne, consulté le ).
- Jacob A.K., Dilger J.A. et Hebl J.R., Status epilepticus and intrathecal fluorescein: Anaesthesia providers beware, Anesth. Analg., 2008, 107:229-31.
- (en) Han Gyu Cha, Jin Geun Kwon et Eun Key Kim, « Intraoperative Detection of Leakage Using Topical Fluorescein Following Free Flap Inset in Head and Neck Reconstruction: », Journal of Craniofacial Surgery, vol. 30, no 4, , e333–e335 (ISSN 1049-2275, DOI 10.1097/SCS.0000000000005259, lire en ligne, consulté le ).
- (en) Jeremy Barr, Jason Ni, Johnathan McGinn et Neerav Goyal, « Topical intranasal fluorescein to localize a cerebrospinal fluid leak: a demonstration », American Journal of Otolaryngology, , p. 102413 (DOI 10.1016/j.amjoto.2020.102413, lire en ligne, consulté le ).
- (en) Rainer Keerl, Rainer K. Weber, Wolfgang Draf et A Wienke, « Use of Sodium Fluorescein Solution for Detection of Cerebrospinal Fluid Fistulas: An Analysis of 420 Administrations and Reported Complications in Europe and the United States », The Laryngoscope, vol. 114, no 2, , p. 266–272 (DOI 10.1097/00005537-200402000-00016).
- (en) Sven Ingelstedt et Bertel Ivstam, « Hypersensitivity to Fluorescein », International Archives of Allergy and Immunology, vol. 1, no 2, , p. 157–159 (ISSN 1018-2438 et 1423-0097, DOI 10.1159/000227857, lire en ligne, consulté le ).
- F. P. Kinsella et D. J. Mooney, « Anaphylaxis following oral fluorescein angiography », American Journal of Ophthalmology, vol. 106, no 6, , p. 745–746 (ISSN 0002-9394, PMID 3195657, DOI 10.1016/0002-9394(88)90716-7, lire en ligne, consulté le ).
- F. Gómez-Ulla, C. Gutiérrez et I. Seoane, « Severe anaphylactic reaction to orally administered fluorescein », American Journal of Ophthalmology, vol. 112, no 1, , p. 94 (ISSN 0002-9394, PMID 1882930, DOI 10.1016/s0002-9394(14)76222-1, lire en ligne, consulté le ).
- (en) R.B. Haveland-Smith, R.D. Combes et B.A. Bridges, « Studies on the genotoxicity of some fluorescein dyes », Mutation Research/Genetic Toxicology, vol. 88, no 1, , p. 1–15 (DOI 10.1016/0165-1218(81)90084-7, lire en ligne, consulté le ).
- (en) Raphael Alford, Haley M. Simpson, Josh Duberman et G. Craig Hill, « Toxicity of Organic Fluorophores Used in Molecular Imaging: Literature Review », Molecular Imaging, vol. 8, no 6, , p. 7290.2009.00031 (ISSN 1536-0121 et 1536-0121, DOI 10.2310/7290.2009.00031, lire en ligne, consulté le ).
- (en) A. Aranda, L. Sequedo, L. Tolosa et G. Quintas, « Dichloro-dihydro-fluorescein diacetate (DCFH-DA) assay: A quantitative method for oxidative stress assessment of nanoparticle-treated cells », Toxicology in Vitro, vol. 27, no 2, , p. 954–963 (DOI 10.1016/j.tiv.2013.01.016, lire en ligne, consulté le ).
- (en) C.J. Cooksey, « Quirks of dye nomenclature. 9. Fluorescein », Biotechnic & Histochemistry, vol. 92, no 7, , p. 506–512 (ISSN 1052-0295 et 1473-7760, DOI 10.1080/10520295.2017.1359751, lire en ligne, consulté le ).
- Kumar, N., Jaiswal, D. et Pandey, J. (2019), Evaluating ecosystem responses to metal pollution in the Ganga River using fluorescein diacetate hydrolytic assay, Plant Archives, 19(2), 3473-3481.
- Schnürer J. et Rosswall T. (1982), Fluorescein diacetate hydrolysis as a measure of total microbial activity in soil and litter, Appl. Environ. Microbiol., 43(6), 1256-1261.
- (en) W.K Walthall et J.D Stark, « The acute and chronic toxicity of two xanthene dyes, fluorescein sodium salt and phloxine B, to Daphnia pulex », Environmental Pollution, vol. 104, no 2, , p. 207–215 (DOI 10.1016/S0269-7491(98)00189-4, lire en ligne, consulté le ).
- Michael W. Davis, Jeana Stephenson et Edward J. Noga, « The effect of tricaine on use of the fluorescein test for detecting skin and corneal ulcers in fish », Journal of Aquatic Animal Health, vol. 20, no 2, , p. 86–95 (ISSN 0899-7659, PMID 18783129, DOI 10.1577/H07-023.1, lire en ligne, consulté le ).
- E.J Noga et P Udomkusonsri, « Fluorescein: a rapid, sensitive, nonlethal method for detecting skin ulceration in fish », Veterinary Pathology, vol. 39, no 6, , p. 726–731 (ISSN 0300-9858, PMID 12450204, DOI 10.1354/vp.39-6-726, lire en ligne, consulté le ).
- (en) Kelly A. Stockton, Christine M. Moffitt, David L. Blew et C. Neal Farmer, « Acute Toxicity of Sodium Fluorescein to Ashy Pebblesnails Fluminicola fuscus », Northwest Science, vol. 86, no 3, , p. 190–197 (ISSN 0029-344X, DOI 10.3955/046.086.0304, lire en ligne, consulté le ).
- H. Pouliquen, M. Algoet, V. Buchet et H. Le Bris, « Acute toxicity of fluorescein to turbot (Scophthalmus maximus) », Veterinary and Human Toxicology, vol. 37, no 6, , p. 527–529 (ISSN 0145-6296, PMID 8588287, lire en ligne, consulté le ).
- « Pyoverdine I - Substance Summary (SID: 47205044) », NIH.gov (consulté le ).
- « Complexation d'actinides par la pyoverdine (ligand produit par la biomasse) », Institut national de physique nucléaire et de physique des particules (in2p3.fr) (consulté le ).
- « Cra-W Département Biotechnologie (mission, personnel,…) » [PDF] (consulté le ).
Voir aussi
[modifier | modifier le code]Liens externes
[modifier | modifier le code]
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Compendium suisse des médicaments : spécialités contenant Fluorescéine
Bibliographie
[modifier | modifier le code]- Bartlett J.D., Ghormley N.R., Jaanus S.D., Rowsey J.J. et Zimmerman T.J., Ophthalmic Dyes. Ophthalmic Drug Facts. Facts and Comparisons, p. 9–11, Wolters Kluwer Co., St. Louis, MO, 1996.
- Berkow J.W., Orth D.H. et Kelley J.S., Fluorescein Angiography: Technique and Interpretation, p. 159, American Academy of Ophthalmology, San Francisco, CA, 1991.
- (en) Chandan Debnath, Mitu Saha, S.A. Hussain et D. Bhattacharjee, « Micellar effect of surfactant on the aggregation pattern of a fluorescent dye in ultra-thin film », Journal of Photochemistry and Photobiology A: Chemistry, vol. 364, , p. 696–704 (DOI 10.1016/j.jphotochem.2018.07.005, lire en ligne, consulté le ).

