رينيوم

| ||||||||||||||||||||||
| المظهر | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
رمادي فلزي | ||||||||||||||||||||||
| الخواص العامة | ||||||||||||||||||||||
| الاسم، العدد، الرمز | رينيوم، 75، Re | |||||||||||||||||||||
| تصنيف العنصر | فلز انتقالي | |||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 7، 6، d | |||||||||||||||||||||
| الكتلة الذرية | 186.207 غ·مول−1 | |||||||||||||||||||||
| توزيع إلكتروني | Xe]; 4f14 5d5 6s2] | |||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2, 8, 18, 32, 13, 2 (صورة) | |||||||||||||||||||||
| الخواص الفيزيائية | ||||||||||||||||||||||
| الطور | صلب | |||||||||||||||||||||
| الكثافة (عند درجة حرارة الغرفة) | 21.02 غ·سم−3 | |||||||||||||||||||||
| كثافة السائل عند نقطة الانصهار | 18.9 غ·سم−3 | |||||||||||||||||||||
| نقطة الانصهار | 3459 ك، 3186 °س، 5767 °ف | |||||||||||||||||||||
| نقطة الغليان | 5869 ك، 5596 °س، 10105 °ف | |||||||||||||||||||||
| حرارة الانصهار | 60.43 كيلوجول·مول−1 | |||||||||||||||||||||
| حرارة التبخر | 704 كيلوجول·مول−1 | |||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 25.48 جول·مول−1·كلفن−1 | |||||||||||||||||||||
| ضغط البخار | ||||||||||||||||||||||
| ||||||||||||||||||||||
| الخواص الذرية | ||||||||||||||||||||||
| أرقام الأكسدة | 7, 6, 5, 4, 3, 2, 1, 0, -1 (أكسيد حمضي ضعيف) | |||||||||||||||||||||
| الكهرسلبية | 1.9 (مقياس باولنغ) | |||||||||||||||||||||
| طاقات التأين | الأول: 760 كيلوجول·مول−1 | |||||||||||||||||||||
| الثاني: 1260 كيلوجول·مول−1 | ||||||||||||||||||||||
| الثالث: 2510 كيلوجول·مول−1 | ||||||||||||||||||||||
| نصف قطر ذري | 137 بيكومتر | |||||||||||||||||||||
| نصف قطر تساهمي | 151±7 بيكومتر | |||||||||||||||||||||
| خواص أخرى | ||||||||||||||||||||||
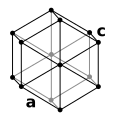
| البنية البلورية | سداسي السطوح | |||||||||||||||||||||
| المغناطيسية | مغناطيسية مسايرة[1] | |||||||||||||||||||||
| مقاومة كهربائية | 193 نانوأوم·متر (20 °س) | |||||||||||||||||||||
| الناقلية الحرارية | 48.0 واط·متر−1·كلفن−1 (300 كلفن) | |||||||||||||||||||||
| التمدد الحراري | 6.2 ميكرومتر/(م·كلفن) | |||||||||||||||||||||
| سرعة الصوت (سلك رفيع) | 4700 متر/ثانية (20 °س) | |||||||||||||||||||||
| معامل يونغ | 463 غيغاباسكال | |||||||||||||||||||||
| معامل القص | 178 غيغاباسكال | |||||||||||||||||||||
| معامل الحجم | 370 غيغاباسكال | |||||||||||||||||||||
| نسبة بواسون | 0.30 | |||||||||||||||||||||
| صلادة موس | 7.0 | |||||||||||||||||||||
| صلادة فيكرز | 2450 ميغاباسكال | |||||||||||||||||||||
| صلادة برينل | 1320 ميغاباسكال | |||||||||||||||||||||
| رقم CAS | 7440-15-5 | |||||||||||||||||||||
| النظائر الأكثر ثباتاً | ||||||||||||||||||||||
| المقالة الرئيسية: نظائر الرينيوم | ||||||||||||||||||||||
| ||||||||||||||||||||||
الرينيوم عنصر كيميائي له الرمز Re، له العدد الذري 75 في الجدول الدوري.[2][3][4]
الاكتشاف
[عدل]ظل العنصر رقم 75 في الجدول الدوري لمندليف غير مكتشفا مع أن العلماء الكيميائين كانو قد توقعوا وجودة نظرا لخلو مكانة وفق ترتيب العدد الذري للعناصر حتي كان عام 1925، في برلين بألمانيا، عندما وجد كل من فالتر نوداك وزوجته إيدا تاك وأوتو بيرغ لعنصر الرينيوم في خامات البلاتين والكولومبيت. كما أعلنوا اكتشافهم للعنصر رقم 43 - والمعروف الآن باسم التكنيشيوم - وكان ذلك من خلال تحليل الأشعة السينية. وقد إعترض الكثيرون على اكتشافاتهم، لكن التجارب المتكررة أثبتت أن العنصر 75 (الرينيوم) قد تم اكتشافه بالفعل.وقد كان بذلك هو العنصر الفلزي الإنتقالي الأخير المكتشف ذا النظير المستقر في الجدول الدوري لمندليف.و يأتي اسم العنصر من الكلمة اللاتينية "Rhenus" التي تعني الراين كما يطلق علي الحجر الذي يوجد فيه الرينيوم باسم حجر الراين.[5][6]
- إيدا تاك مكتشفة عنصر الرينيوم
- أوتو بيرغ مكتشف الرينيوم
- والتر نوداك
التواجد في الطبيعة
[عدل]لا يوجد الرينيوم حرا في الطبيعة، ومعادن الرينيوم غير معروفة.و يوجد الرينيوم بتركيزات صغيرة، وفي صخور البغماتيت والصخور المدمجة مع المعادن مثل الموليبدينوم وكبريتيد النحاس. وتوجد بكميات صغيرة في معادن الجادولينيت والكولومبيت والتانتاليت وفي بعض رواسب البلاتين والنحاس. تحتوي قشرة الأرض على ما يقدر بنحو 0.001٪ من الرينيوم.[7][8]
- الموليبدينوم
- عنصر الرينيوم بدون صهر
- الشكل البلوري للرينيوم
الخصائص
[عدل]الرينيوم معدن نادر جدا وهو فضي لامع. ومقاوم قوي للتآكل والأكسدة وهو ثالث عنصر بعد الكربون والتنجستن في مقياس درجة الإنصهار ويلي كلا من الإيريديوم والأوزميوم والبلاتين في درجة الكثافة.والرينيوم هو واحد من خمسة معادن حرارية (معادن ذات مقاومة عالية للحرارة والتآكل).والمعادن الأخرى المقاومة للصهر هي التنجستن والموليبدينوم والتنتالوم والنيوبيوم. مركبات الرينيوم تشمل كلا من أكاسيد الرينيوم وهاليدات الرينيوم وكبريتيدات الرينيوم.[5][9]
إستخدامات الرينيوم
[عدل]يستخدم الرينيوم مع البلاتين كمحفزات في إنتاج البنزين الخالي من الرصاص والأوكتان العالي. ويستخدم في سبائك المحركات النفاثة وفي سبائك التنغستن والموليبدينوم.و يستخدم على نطاق واسع كخيوط لأجهزة قياس الطيف الكتلي. ويستخدم أيضًا في مواد التلامس الكهربائي. ومحفزات الرينيوم مقاومة بشكل استثنائي للتسمم من النيتروجين والكبريت والفوسفور وهي مفيدة في هدرجة المواد الكيميائية الدقيقة.[5] وسبائك الرينيوم والموليبدينوم فائقة التوصيل الكهربائي وتستخدم المزدوجات الحرارية المصنوعة من الرينيوم والتنجستين لقياس درجات حرارة تصل إلى 2200 درجة مئوية كما يستخدم سلك الرينيوم في مصابيح الفلاش في التصوير الفوتوغرافي.[10]
- جهاز استشراب غازي مزود بمطياف كتلة
- جهاز تلامس كهربائي صغير
- وحدة مقياس حراري دقيقة
- محرك توربيني قيد التجربة
- محرك توربيني جاهز للتركيب
الإنتاج
[عدل]لا يوجد الرينيوم حرًا في الطبيعة أو كمركب في معدن مميز. ولكنة ينتشر على نطاق واسع في جميع أنحاء القشرة الأرضية إلى حد حوالي 0.001 جزء في المليون. ويحتوي بعض الموليبدينوم من 0.002٪ إلى 0.2٪ رينيوم. ويتم إنتاج أكثر من 150 ألف أوقية من الرينيوم سنويًا في الولايات المتحدة. والبلدان الأعلى إنتاجا للرنيوم هي شيلي وكازاخستان، وتستخرجة كل من الولايات المتحدة، أرمينيا، كندا، بيرو وروسيا.
- بيررنات( رباعي أكسيد الرينيوم) الأمونيوم (NH 4 ReO 4 )
- منجم للنحاس السماقي في تشوكيكاماتا ، تشيلي يستخرج منه الرينيوم
- المظهر الفضي من حجر الراين (حجر الرينيوم ) من بركان كودريافي في جزر الكوريل بروسيا
اقرأ أيضاً
[عدل]المراجع
[عدل]- ^ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ "معلومات عن رينيوم على موقع fdasis.nlm.nih.gov". fdasis.nlm.nih.gov. مؤرشف من الأصل في 2019-12-16.
- ^ "معلومات عن رينيوم على موقع snl.no". snl.no. مؤرشف من الأصل في 2016-10-21.
- ^ "معلومات عن رينيوم على موقع chem.nlm.nih.gov". chem.nlm.nih.gov. مؤرشف من الأصل في 2019-12-16.
- ^ ا ب ج "Rhenium". مؤرشف من الأصل في 2021-01-07. اطلع عليه بتاريخ 2021-01-28.
- ^ "Rhenium / Re (Element) - PubChem". مؤرشف من الأصل في 2021-03-02. اطلع عليه بتاريخ 2021-01-28.
- ^ "rhenium – Store norske leksikon". مؤرشف من الأصل في 2016-10-21. اطلع عليه بتاريخ 2021-01-28.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ "Rhenium - an overview / ScienceDirect Topics". مؤرشف من الأصل في 2021-03-02. اطلع عليه بتاريخ 2021-01-28.
- ^ "Rhenium - Element information, properties and uses / Periodic Table". مؤرشف من الأصل في 2021-02-06. اطلع عليه بتاريخ 2021-01-28.
- ^ "Rhenium / Re (Element) - PubChem". مؤرشف من الأصل في 2021-03-02. اطلع عليه بتاريخ 2021-01-28.
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||