Idrossido ferroso

| Idrossido ferroso | |
|---|---|
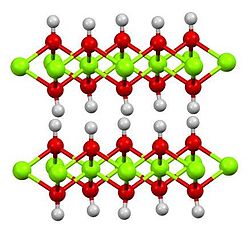 | |
 | |
| Nome IUPAC | |
| idrossido di ferro(II) | |
| Nomi alternativi | |
| idrossido ferroso idrossido di ferro(II) diidrossido di ferro | |
| Caratteristiche generali | |
| Formula bruta o molecolare | Fe(OH)2 |
| Massa molecolare (u) | 89,86 |
| Aspetto | Solido verde scuro |
| Numero CAS | |
| Numero EINECS | 242-456-5 |
| PubChem | 10129897 |
| SMILES | [OH-].[OH-].[Fe+2] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 3,4 g/cm3 |
| Solubilità in acqua | 0.00143 g/l (20 C°) |
| Costante di solubilità a 298 K | 1,64×10−14[1] 8×10−16[2] |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −574 KJ/mol |
| S0m(J·K−1mol−1) | 92 J/(K·mol) |
| Indicazioni di sicurezza | |
L'idrossido ferroso o idrossido di ferro(II) è un composto chimico ignifugo, non tossico, insapore (allappante), originariamente di colore bianco che cambia colore in verde scuro o verde-nero fino al marrone man mano che si ossida all'aria.
Più specificamente, è l'idrossido in cui il ferro assume stato di ossidazione +2.
Sintesi
[modifica | modifica wikitesto]
Doppio scambio
[modifica | modifica wikitesto]Si può ottenere facendo reagire un composto contenente lo ione ossidrile con un altro contenente lo ione Fe2+, come ad esempio idrossido di sodio e cloruro ferroso:[3]
soda caustica e solfato ferroso:
oppure idrossido di potassio e solfato ferroso:
- .
Sintesi elettrolitica
[modifica | modifica wikitesto]Si può ottenere idrossido ferroso tramite elettrolisi di una soluzione di cloruro di sodio in acqua utilizzando elettrodi di ferro.
Gli ioni Cl- e Na+ migrano agli elettrodi, trasformandosi in Cl gassoso e Na metallico.
- .
A questo punto Il sodio sviluppato all'anodo andrà a legarsi con l'acqua di soluzione per formare idrossido di sodio e idrogeno:
- .
Mentre il cloro si legherà al ferro dell'elettrodo formando cloruro ferroso:
- .
Quest'ultimo composto, entrando in contatto con l'idrossido di sodio del catodo si combina generando cloruro di sodio e idrossido ferroso:
- .
L'elettrolisi può continuare scindendo di nuovo il cloruro di sodio ottenuto, fino ad esaurimento dell'acqua di soluzione o degli elettrodi.
Man mano che la reazione procede si noterà che il precipitato da verde lentamente si scurisce diventando marrone scuro.
Depurazione
[modifica | modifica wikitesto]Si passa alla purificazione della sostanza ottenuta dall'idrossido di sodio tramite molteplici lavaggi in cui si aggiunge acqua alla soluzione, si lascia decantare l'idrossido di ferro(II) e si aspira l'acqua di superficie, per poi ripetere varie volte il procedimento.
Conservazione
[modifica | modifica wikitesto]Dopo la depurazione, si può conservare l'idrossido ferroso in un comune congelatore domestico, senza necessariamente separarlo dall'acqua in cui è contenuto.
Degradazione
[modifica | modifica wikitesto]
Se esposto all'acqua, alla luce e soprattutto all'aria, (in presenza di ossigeno) degrada in sostanze secondarie come l'idrossido ferrico. Per preservarne le caratteristiche è sufficiente tenere il composto a basse temperature e non direttamente esposto all'aria.
Usi
[modifica | modifica wikitesto]L'idrossido ferroso viene utilizzato per la depurazione delle acque da composti del selenio.[4]
Microbiologia
[modifica | modifica wikitesto]I batteri ferrofissatori ossidano il catione Fe++ dell'idrossido ferroso con l'ossigeno presente nell'acqua in cui vivono per trarne energia.
- .
Conversione in magnetite
[modifica | modifica wikitesto]Tramite un processo chimico chiamato reazione di Schikorr l'idrossido ferroso viene convertito in magnetite con liberazione di acqua e idrogeno gassoso:
- .
Note
[modifica | modifica wikitesto]- ^ General Chemistry di Pauling - Vedere anche la voce Costante di solubilità.
- ^ Copia archiviata, su bilbo.chm.uri.edu. URL consultato il 23 febbraio 2015 (archiviato dall'url originale il 26 febbraio 2015). - Vedere anche la voce Costante di solubilità.
- ^ http://online.scuola.zanichelli.it/chimicafacile/files/2011/03/Formazione-idrossidi.pdf
- ^ https://www.sciencedirect.com/science/article/pii/S0160412097000329
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file sull'Idrossido ferroso
Wikimedia Commons contiene immagini o altri file sull'Idrossido ferroso








