小分子

分子生物学や薬理学の分野では、小分子(しょうぶんし、英: small molecule)は、生物学的プロセスを調節する可能性のある低分子量(900ダルトン未満[1])の有機化合物で、大きさは1 nm程度である。多くの医薬品は小分子である。核酸やタンパク質などの大きな構造物や多糖の多くは小分子ではないが、それらを構成するモノマー(それぞれリボヌクレオチドまたはデオキシリボヌクレオチド、アミノ酸、単糖)は小分子とみなされることが多い。小分子は、生体機能を解明するための研究ツールとして、また新たな治療薬の開発につながるリードとしても使用される。タンパク質の特定の機能を阻害したり、タンパク質間相互作用を妨害するものもある[2]。
薬理学では通常、「小分子」という用語を、特定の生体高分子に結合してエフェクターとして作用し、標的の活性や機能を変化させる分子に限定している。小分子は、細胞シグナル伝達分子、医療における医薬品、農業における農薬、他の多くの役割として機能する、さまざまな生物学的機能または用途を持っている。これらの化合物には、天然のものと(二次代謝産物など)、人工的なものがある(抗ウイルス薬など)。それらは病気に対して有益な効果があるかもしれないし(医薬品など)、有害なものかもしれない(催奇形物質や発がん性物質など)。
分子量カットオフ
[編集]小分子の分子量の上限は約900ダルトンで、これにより細胞膜を越えて急速に拡散して、細胞内の作用部位に到達できるようになる[1][3]。また、この分子量カットオフは、腸上皮細胞を介した経細胞輸送を可能にするための経口バイオアベイラビリティの必要条件であるが不十分でもある。その分子は腸管透過性に加えて、水への適度な溶解速度と水溶性を持ち、初回通過代謝が中程度~低いことも必要である。分子量が500ダルトン以下であれば臨床的な損耗率が大幅に低下するという観察結果に基づき、経口の小分子医薬品候補に対しては(「リピンスキーの5の法則」の一部として)やや低い分子量カットオフが推奨されている[4][5]。
医薬品
[編集]ほとんどの医薬品は小分子であるが、中にはタンパク質の医薬品もある(例:インスリンなどのバイオ医薬品)。抗体医薬品を除いて、多くのタンパク質は経口投与されると分解されて、ほとんどの場合は細胞膜を通過することができない。小分子は吸収されやすいが、中にはプロドラッグとして投与されるように、経口投与した後にのみ吸収されるものもある。小分子薬(small molecule drugs、SMD)が「大分子」生物製剤よりも優れている点の1つは、生物製剤が一般に注射などの非経口投与を必要とするのに対し、小分子薬の多くは経口投与が可能なことである[6]。
二次代謝産物
[編集]バクテリア、菌類、植物などさまざまな生物が、細胞シグナル伝達、色素形成、および捕食に対する防御などの役割を果たす二次代謝産物(天然物とも呼ばれる)を生成する。二次代謝産物は生物学的に活性な化合物の豊富な供給源であるため、研究ツールや創薬のリードとしてよく利用されている[7]。二次代謝産物の例は次のとおりである。
調査ツール
[編集]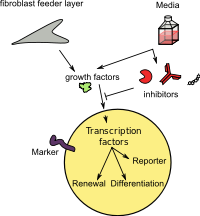
酵素や受容体は、内因性タンパク質によって活性化または阻害されることが多く、この他にも、活性部位またはアロステリック部位に結合できる内因性または外因性の低分子阻害剤や活性化剤によって阻害されることもある。
たとえば、植物テルペンの一種で、催奇形性や発がん性のある酢酸ミリスチン酸ホルボールがある。これは、がんを促進するプロテインキナーゼCを活性化させるため、調査のツールとして有効である[9]。また、遺伝子の発現を制御するため、小分子の人工的な転写因子を作ることにも関心が持たれていて、その例としてレンチノロール(レンチの形をした分子)があげられる。[10]。
リガンドの結合状態は、表面プラズモン共鳴、マイクロスケール熱泳動[11]、二面偏波式干渉法などのさまざまな分析手法を使用して特徴付けることができ、反応親和性や速度論的特性、および誘発されるコンフォメーション変化を定量化することができる。
抗ゲノム治療薬
[編集]小分子抗ゲノム治療薬(Small-molecule Anti-Genomic Therapeutics、SMAT)は、多くの生物兵器に見られるDNAシグネチャーを標的とした生物防御技術のことを指す。SMATは、抗菌、抗ウイルス、抗マラリア活性を単一の治療薬に統合した新しい広域スペクトル薬であり、医師や軍隊に実質的な費用効果と物流面で利点をもたらす[12]。
参照項目
[編集]脚注
[編集]- ^ a b Macielag MJ (2012). “Chemical properties of antibacterials and their uniqueness”. Antibiotic Discovery and Development. pp. 801–2. ISBN 978-1-4614-1400-1. "The majority of [oral] drugs from the general reference set have molecular weights below 550. In contrast the molecular-weight distribution of oral antibacterial agents is bimodal: 340–450 Da but with another group in the 700–900 molecular weight range."
- ^ Arkin MR, Wells JA (April 2004). “Small-molecule inhibitors of protein-protein interactions: progressing towards the dream”. Nature Reviews Drug Discovery 3 (4): 301–17. doi:10.1038/nrd1343. PMID 15060526.
- ^ Veber DF, Johnson SR, Cheng HY, Smith BR, Ward KW, Kopple KD (June 2002). “Molecular properties that influence the oral bioavailability of drug candidates”. J. Med. Chem. 45 (12): 2615–23. doi:10.1021/jm020017n. PMID 12036371.
- ^ Lipinski CA (December 2004). “Lead-and drug-like compounds: the rule-of-five revolution”. Drug Discovery Today: Technologies 1 (4): 337–341. doi:10.1016/j.ddtec.2004.11.007. PMID 24981612.
- ^ Leeson PD, Springthorpe B (November 2007). “The influence of drug-like concepts on decision-making in medicinal chemistry”. Nature Reviews Drug Discovery 6 (11): 881–90. doi:10.1038/nrd2445. PMID 17971784.
- ^ Samanen J (2013). “Chapter 5.2 How do SMDs differ from biomolecular drugs?”. Introduction to Biological and Small Molecule Drug Research and Development: theory and case studies (Kindle ed.). New York: Academic Press. pp. 161–203. doi:10.1016/B978-0-12-397176-0.00005-4. ISBN 978-0-12-397176-0. "Table 5.13: Route of Administration: Small Molecules: oral administration usually possible; Biomolecules: Usually administered parenterally"
- ^ Atta-ur-Rahman, ed (2012). Studies in Natural Products Chemistry. 36. Amsterdam: Elsevier. ISBN 978-0-444-53836-9
- ^ Mfopou JK, De Groote V, Xu X, Heimberg H, Bouwens L (May 2007). “Sonic hedgehog and other soluble factors from differentiating embryoid bodies inhibit pancreas development”. Stem Cells 25 (5): 1156–65. doi:10.1634/stemcells.2006-0720. PMID 17272496.
- ^ Voet JG, Voet D (1995). Biochemistry. New York: J. Wiley & Sons. ISBN 978-0-471-58651-7
- ^ Koh JT, Zheng J (September 2007). “The new biomimetic chemistry: artificial transcription factors”. ACS Chem. Biol. 2 (9): 599–601. doi:10.1021/cb700183s. PMID 17894442.
- ^ Wienken CJ, Baaske P, Rothbauer U, Braun D, Duhr S (2010). “Protein-binding assays in biological liquids using microscale thermophoresis”. Nat Commun 1 (7): 100. Bibcode: 2010NatCo...1..100W. doi:10.1038/ncomms1093. PMID 20981028.
- ^ Levine DS (2003年). “Bio-defense company re-ups”. San Francisco Business Times. 2006年9月6日閲覧。
外部リンク
[編集]- Small Molecule Libraries - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス