Alanin

| Alanin | |||
|---|---|---|---|
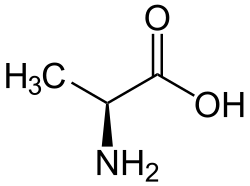 | |||
| Systematisk navn | |||
| 2-Aminopropanoisk syre | |||
| Identifikatorer | |||
| CAS-nummer | |||
| SMILES | O=C(O)C(N)C | ||
| Kjemiske egenskaper | |||
| Formel | HO2CCH(CH3)NH2 | ||
| Molar masse | 125,1 g/mol | ||
| Utseende | Hvitt pulver | ||
| Tetthet | 1424 kg/m3 | ||
| Smeltepunkt | 258 °C | ||
| Løselighet | 167.2 g/L (i vann 25 °C) | ||
| pKa | 2,34 9,87 | ||
Alanin (Ala eller A), HO2CCH(CH3)NH2, er en av de 20 aminosyrene som er byggesteiner i proteiner. Den tilhører gruppen nøytrale, hydrofobe, upolare aminosyrer og er nest etter glycin den enkleste og minst karakteristiske sidekjede. Dets genetiske kodoner er GCU, GCC, GCA og GCG.
Biokjemisk karakteristikk
[rediger | rediger kilde]Alanin er ikke en essensiell aminosyre, men kan dannes i kroppen ved tilførsel av andre aminosyrer. I en undersøkelse av 1150 ulike proteiner utgjorde alanin 7,8 % av aminosyrene[1]
Metabolisme
[rediger | rediger kilde]Alanin dannes i størst grad ved reduktiv aminering av pyrodruesyre. Siden transaminering sreaksjoner er fritt reversible og pyrodruesyre passerer fritt gjennom cellene, kan, alanin can lett dannes så lenge aminogrupper er tilgjengelige, og alaninmetabolismen er tett knyttet sammen med de sentrale metabolske prosesse3ne: glykolyse, glukoneogenese, og sitronsyresyklus. Slik oppstår alanin også sammen med melkesyre ved anarobe betingelser, og danner glukose fra protein via alaninsyklus.
Kjemisk syntese
[rediger | rediger kilde]Se også
[rediger | rediger kilde]Referanser
[rediger | rediger kilde]- ^ Doolittle, R.F. “Redundancies in protein sequences” s. 599–623, i Fasman, G.D. (red.) Prediction of Protein Structures and the Principles of Protein Conformation, Plenum, New York ISBN 0306431319.

