Рилменидин
 Из Википедии, бесплатной энциклопедии
Из Википедии, бесплатной энциклопедии
| Рилменидин | |
|---|---|
 | |
| Химическое соединение | |
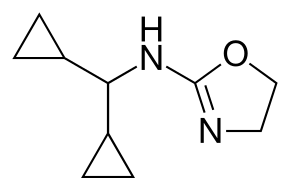
| ИЮПАК | N-(дициклопропилметил)-4,5-дигидро-1,3-оксазол-2-амин |
| Брутто-формула | C10H16N2O |
| Молярная масса | 180.251 г/моль |
| CAS | 54187-04-1 |
| PubChem | 68712 |
| DrugBank | 11738 |
| Состав | |
| Классификация | |
| АТХ | C02AC06 |
| Способы введения | |
| орально | |
| Другие названия | |
| Оксаминозолин | |
Рилменидин, оксазолин, замещённый в положении 2 аминодициклопропилметильной группой, обладающий антигипертензивными свойствами, поскольку является специфическим агонистом центральных и периферических имидазолиновых (I1) рецепторов.[1]
Рилменидин менее эффективен, чем клонидин, зато обладает в 30 раз большей селективностью, чем клонидин, в отношении имидазолиновых рецепторов по сравнению с α2-адренорецепторами.[2] Более низкое сродство рилменидина к α2-адренорецепторам может быть причиной меньшего седативного и других побочных эффектов. Это, в сочетании с его эффективностью в снижении артериального давления и более длительным периодом полураспада, сделало его гораздо более терапевтически полезным. Он продаётся под торговыми марками Альбарел[3], Hyperium, Iterium и Tenaxum. Поскольку рилменидин даже при длительном применении не влиял на регуляцию глюкозы как при инсулинзависимом, так и при инсулиннезависимом сахарном диабете и не изменял параметры липидного обмена, его рекомендуют для снижения давления у больных диабетом.[4] Тем не менее, следует помнить что опасным побочным эффектом длительного приёма антигипертензивных средств, и в том числе рилменидина, может быть повышение внутричерепного давления, даже если оно сопровождается снижением центрального артериального давления.
Возбуждение центральных имидазолиновых рецепторов в сосудодвигательном центре продолговатого мозга сопровождается уменьшением симпатической импульсации к сосудам и сердцу, что приводит к снижению артериального давления и общего периферического сопротивления сосудов (ОПСС), уменьшению частоты серде́чных сокраще́ний (ЧСС).[5] Отчасти антигипертензивное действие обусловлено стимуляцией альфа2-адренергических рецепторов на мембранах нейронов в ядрах солитарного тракта. Снижает активность ренина и содержание норадреналина, ангиотензина II и альдостерона. Стимуляция периферических I1-имидазолиновых рецепторов в почках, надпочечниках, поджелудочной железе, жировой ткани и каротидных клубочках сопровождается рядом дополнительных эффектов. Возбуждение I1-имидазолиновых рецепторов в почках вызывает уменьшение реабсорбции натрия и воды, в надпочечниках — торможение высвобождения катехоламинов из хромаффинных клеток, в поджелудочной железе — увеличение секреции инсулина в ответ на нагрузку глюкозой, в адипоцитах — усиление липолиза, в каротидных клубочках — повышение чувствительности к понижению артериального давления и гипоксии/гиперкапнии.
По данным двойных слепых плацебо-контролируемых исследований и сравнительных исследований с эталонными препаратами обладает антигипертензивной активностью в терапевтических дозах (1 мг/сут однократно или 2 мг/сут в 2 приёма) при мягкой и умеренной степени артериальной гипертензии. Дозозависимо понижает систолическое артериальное давление (сАД) и диастолическое артериальное давление (дАД) (в покое и при физической нагрузке), действует в положении больного как лёжа, так и стоя. Оказывает пролонгированное фармакологическое действие, значимый гипотензивный эффект сохраняется в течение 24 ч после приёма в дозе 1 мг. При длительном применении не отмечается ослабления гипотензивного эффекта, а внезапная отмена не сопровождается развитием рикошетной гипертензии. Не нарушает физиологической реакции, проявляющейся изменением ЧСС в ответ на физическую нагрузку. В терапевтических дозах практически не влияет на сократимость миокарда, сердечный выброс, сердечные электрофизиологические индексы, почечный кровоток, характеристики клубочковой фильтрации и объем фильтрационной фракции.[6]
Несмотря на то, что рилменидин является независимым от mTORC1 индуктором аутофагии,[7] он в отличие от рапамицина оказался неэффективным для лечения миопатических проявлений поскольку при лечении рилменидином активация аутофагии происходит без одновременного усиления биогенеза лизосом.[8]
Рилменидин увеличивал продолжительность жизни Caenorhabditis elegans и повышал их стрессоустойчивость, воздействуя на I1-имидазолиновый рецептор nish-1. При этом ограничение калорийности диеты, генетическое снижение функции TORC1 или лечение рапамицином не приводили к дальнейшему увеличению продолжительности жизни. Более того, у мышей, получавших рилменидин в тканях печени и почек наблюдались транскрипционные изменения, сходные с теми что наблюдаются при ограничении калорийности питания, что свидетельствует о геропротекторных свойствах рилменидина.[9]
Примечания[править | править код]
- ↑ Nikolic, K., & Agbaba, D. (2012). Imidazoline antihypertensive drugs: selective i1‐imidazoline receptors activation. Cardiovascular Therapeutics, 30(4), 209-216. PMID 21884004 DOI: 10.1111/j.1755-5922.2011.00269.x
- ↑ Gomez, R. E., Ernsberger, P., Feinland, G., & Reis, D. J. (1991). Rilmenidine lowers arterial pressure via imidazole receptors in brainstem C1 area. European journal of pharmacology, 195(2), 181-191. PMID: 1651861 DOI: 10.1016/0014-2999(91)90534-w
- ↑ Альбарел, таблетки 1 мг. Дата обращения: 5 марта 2023. Архивировано 5 марта 2023 года.
- ↑ Meredith, P. A., & Reid, J. L. (2004). Efficacy and tolerability of long-term rilmenidine treatment in hypertensive diabetic patients: a retrospective analysis of a general practice study. American Journal of Cardiovascular Drugs, 4, 195-200. PMID: 15134471 DOI: 10.2165/00129784-200404030-00006
- ↑ Sabharwal, R., El Accaoui, R. N., Weiss, R. M., Davis, M. K., Abboud, F. M., & Chapleau, M. W. (2015). Inhibition of sympathetic activity by rilmenidine reverses angiotensin II-induced hypertension, blood pressure variability and cardiac remodeling. Autonomic Neuroscience: Basic and Clinical, 192, 23. https://doi.org/10.1016/j.autneu.2015.07.320
- ↑ [Электронная энциклопедия лекарств 2023]
- ↑ Perera, N. D., Sheean, R. K., Lau, C. L., Shin, Y. S., Beart, P. M., Horne, M. K., & Turner, B. J. (2018). Rilmenidine promotes MTOR-independent autophagy in the mutant SOD1 mouse model of amyotrophic lateral sclerosis without slowing disease progression. Autophagy, 14(3), 534-551.
- ↑ Civiletto, G., Dogan, S. A., Cerutti, R., Fagiolari, G., Moggio, M., Lamperti, C., ... & Zeviani, M. (2018). Rapamycin rescues mitochondrial myopathy via coordinated activation of autophagy and lysosomal biogenesis. EMBO molecular medicine, 10(11), e8799. PMID: 30309855 PMCID: PMC6220341 DOI: 10.15252/emmm.201708799
- ↑ Bennett, D. F., Goyala, A., Statzer, C., Beckett, C. W., Tyshkovskiy, A., Gladyshev, V. N., ... & de Magalhães, J. P. (2023). Rilmenidine extends lifespan and healthspan in Caenorhabditis elegans via a nischarin I1‐imidazoline receptor. Aging Cell, e13774. PMID 36670049 PMC 9924948 doi:10.1111/acel.13774