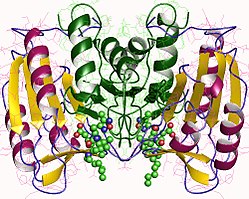
カスパーゼ-3
 ウィキペディアから無料の百科事典
ウィキペディアから無料の百科事典
カスパーゼ-3(英: caspase-3)は、カスパーゼ-8、カスパーゼ-9と相互作用するカスパーゼであり、ヒトではCASP3遺伝子にコードされる。CASP3のオルソログ[4]は、全ゲノムデータが利用可能な哺乳類の多数で同定されている。オルソログは、鳥類、爬虫類、両生類、真骨類にも存在している。
CASP3タンパク質は、カスパーゼ(cysteine-aspartic acid protease)ファミリーのメンバーである[5]。カスパーゼの連続的な活性化は、アポトーシスの実行期(execution phase)に中心的な役割を果たす。カスパーゼ-3は不活性な酵素前駆体として存在し、保存されたアスパラギン酸残基でタンパク質分解によるプロセシングが行われることで大小2つのサブユニットが生じ、それらが二量体化して活性型酵素が形成される。カスパーゼ-3はアミロイドβ(A4)前駆体タンパク質の切断に関与する主要なカスパーゼで、アルツハイマー病における神経細胞死と関係している[6]。この遺伝子の選択的スプライシングによって2種類の転写産物が生成されるが、コードされるタンパク質は同じである[7]。


カスパーゼ-3は、既知のすべてのカスパーゼに共通した典型的な特徴の多くを備えている。例えば、その活性部位にはシステイン残基(Cys163)とヒスチジン残基(His121)が存在し、特定の4アミノ酸配列中のアスパラギン酸のC末端側でのペプチド結合の切断が安定化される[9][10]。この特異性によってカスパーゼの選択性はかなり高くなり、グルタミン酸と比較してアスパラギン酸に対する選択性は20,000倍となる[11]。細胞内のカスパーゼ-3の重要な特徴は、プロカスパーゼと呼ばれる酵素前駆体として存在していることであり、生化学的な変化によって活性化が引き起こされるまでは不活性な状態である[12]。
基質特異性[編集]
通常条件下では、カスパーゼは基質中の4ペプチド配列を認識し、アスパラギン酸残基の後のペプチド結合を加水分解する。カスパーゼ-3とは類似した基質特異性を持ち、Asp-x-x-Aspという4ペプチドを認識する[13]。C末端側のアスパラギン酸は絶対に必要であるが、他の3つの位置の多様性はある程度許容される[14]。カスパーゼの基質特異性は、阻害剤や薬剤のデザインに広く利用されている[15]。
構造[編集]
カスパーゼ-3(CPP32、Yama、apopainとしても知られる[16][17][18])は、32 kDaの酵素前駆体として産生され、17 kDaと 12 kDaのサブユニット(p17とp12)へと切断される。プロカスパーゼが特定の残基で切断されると、活性型のヘテロ四量体が形成される。まずp17とp12のβシートが連結されてヘテロ二量体を形成し、その後他のヘテロ二量体と相互作用することで、12本のストランドからなるβシートがαヘリックスで囲まれた、カスパーゼに特徴的な構造が形成される[12][19]。ヘテロ二量体同士がhead-to-tail型に並んだ際、活性部位は分子の両端に形成される。Cys163とHis121はp17サブユニットに存在している[19]。
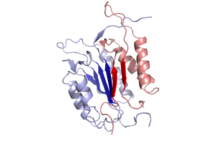
機構[編集]
カスパーゼ-3の触媒部位には、Cys163のスルフヒドリル基とHis121のイミダゾール環が存在する。His121は重要なアスパラギン残基のカルボニル基を安定化し、Cys163は最終的なペプチド結合の切断の際に攻撃を行う。Cys163とGly238は、水素結合によって基質-酵素複合体の四面体型遷移状態を安定化する機能も持つ[19]。In vitroでは、カスパーゼ-3は DEVDG(Asp-Glu-Val-Asp-Gly)配列の2つ目のアスパラギン酸残基のC末端側(DとGの間)での切断に対する選択性があることが判明している[11][19][20]。カスパーゼ-3は幅広いpHで活性があり、他の実行型カスパーゼの多くよりもわずかに高い(塩基性側の)範囲である。この幅広さは、カスパーゼ-3が正常な条件下でもアポトーシス条件下でも十分に活性があることを示している[21]。
活性化[編集]
カスパーゼ-3は、外因性(デスリガンド)経路か内因性(ミトコンドリア)経路かに関わらずアポトーシスを引き起こした細胞で活性化される[12][22]。カスパーゼ-3が酵素前駆体として存在しているとは必要不可欠であり、そうした調節がなければカスパーゼ活性によって無差別に細胞死が引き起こされる[23]。実行型(エフェクター)カスパーゼであるため、アポトーシスシグナル伝達イベントが発生して誘導型(イニシエーター)カスパーゼによって切断されるまで、カスパーゼ-3の酵素前駆体は事実上活性を持たない[24]。そうしたイベントの1つがグランザイムBの誘導であり、細胞傷害性T細胞の標的となった細胞でイニシエーターカスパーゼを活性化させる[25][26]。この外因性因子による活性化によってアポトーシス経路に特徴的なカスパーゼカスケードが誘導され、そこではカスパーゼ-3が主要な役割を果たす[10]。内因性因子による活性化では、ミトコンドリアのシトクロムcが、カスパーゼ-9、Apaf-1、ATPと協働してプロカスパーゼ-3のプロセシングを行う[20][26][27]。これらの分子はin vitroでカスパーゼ-3を活性化するのには十分であるが、in vivoでは他の調節タンパク質が必要である[27]。
阻害[編集]
カスパーゼを阻害する方法の1つは、cIAP1、cIAP2、XIAP、ML-IAPを含むアポトーシス阻害因子を介して行われる[19]。XIAPは、カスパーゼ-3の活性化に直接関係しているカスパーゼ-9に結合して阻害を行う[27]。しかしカスパーゼカスケード中では、カスパーゼ3はカスパーゼ-9を特定の部位で切断することで、XIAPによるカスパーゼ-9への活性阻害のための結合を防ぎ、XIAPの活性を阻害する[28]。
マンゴスチン(Garcinia mangostana)のエキスは、アミロイドβ処理されたヒトの神経細胞でカスパーゼ-3の活性化を阻害することが示されている[29]。
生物学的機能[編集]
カスパーゼ-3は、アポトーシスにおける典型的な役割と同様、脳の正常な発生に必須であり、クロマチンの凝縮とDNAの断片化を担う[20]。カスパーゼの断片であるp17の血中濃度の上昇は、直近の心筋梗塞のサインとなる[30]。また、カスパーゼ-3が胚性幹細胞や造血幹細胞の分化に関与している可能性が示されている[31]。
相互作用[編集]
カスパーゼ-3は次に挙げる因子と相互作用することが示されている。
出典[編集]
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000031628 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “ENSG00000164305_CASP3”. www.orthomam.univ-montp2.fr. 2020年5月14日閲覧。
- ^ “Human ICE/CED-3 protease nomenclature”. Cell 87 (2): 171. (October 1996). doi:10.1016/S0092-8674(00)81334-3. PMID 8861900.
- ^ “Involvement of caspases in proteolytic cleavage of Alzheimer's amyloid-beta precursor protein and amyloidogenic A beta peptide formation”. Cell 97 (3): 395–406. (April 1999). doi:10.1016/s0092-8674(00)80748-5. PMID 10319819.
- ^ “Entrez Gene: CASP3 caspase 3, apoptosis-related cysteine peptidase”. 2020年5月14日閲覧。
- ^ “Construction and analysis of a modular model of caspase activation in apoptosis”. Theoretical Biology & Medical Modelling 5 (1): 26. (2008). doi:10.1186/1742-4682-5-26. PMC 2672941. PMID 19077196.
- ^ “Apoptosis: an overview”. British Medical Bulletin 53 (3): 451–65. (1997). doi:10.1093/oxfordjournals.bmb.a011623. PMID 9374030.
- ^ a b “Zinc is a potent inhibitor of the apoptotic protease, caspase-3. A novel target for zinc in the inhibition of apoptosis”. The Journal of Biological Chemistry 272 (30): 18530–3. (July 1997). doi:10.1074/jbc.272.30.18530. PMID 9228015.
- ^ a b “Internally quenched fluorescent peptide substrates disclose the subsite preferences of human caspases 1, 3, 6, 7 and 8”. The Biochemical Journal 350 (2): 563–8. (September 2000). doi:10.1042/0264-6021:3500563. PMC 1221285. PMID 10947972.
- ^ a b c “Caspases: opening the boxes and interpreting the arrows”. Cell Death and Differentiation 9 (1): 3–5. (January 2002). doi:10.1038/sj.cdd.4400963. PMID 11803369.
- ^ “Plasticity of S2-S4 specificity pockets of executioner caspase-7 revealed by structural and kinetic analysis”. The FEBS Journal 274 (18): 4752–65. (September 2007). doi:10.1111/j.1742-4658.2007.05994.x. PMID 17697120.
- ^ “Structural and kinetic analysis of caspase-3 reveals role for s5 binding site in substrate recognition”. Journal of Molecular Biology 360 (3): 654–66. (July 2006). doi:10.1016/j.jmb.2006.05.041. PMID 16781734.
- ^ “Caspases: structure-guided design of drugs to control cell death”. Mini Reviews in Medicinal Chemistry 8 (11): 1154–62. (October 2008). doi:10.2174/138955708785909899. PMID 18855730.
- ^ “CPP32, a novel human apoptotic protein with homology to Caenorhabditis elegans cell death protein Ced-3 and mammalian interleukin-1 beta-converting enzyme”. The Journal of Biological Chemistry 269 (49): 30761–4. (December 1994). PMID 7983002.
- ^ “Yama/CPP32 beta, a mammalian homolog of CED-3, is a CrmA-inhibitable protease that cleaves the death substrate poly(ADP-ribose) polymerase”. Cell 81 (5): 801–9. (June 1995). doi:10.1016/0092-8674(95)90541-3. PMID 7774019.
- ^ “Identification and inhibition of the ICE/CED-3 protease necessary for mammalian apoptosis”. Nature 376 (6535): 37–43. (July 1995). doi:10.1038/376037a0. PMID 7596430.
- ^ a b c d e “Caspases: pharmacological manipulation of cell death”. The Journal of Clinical Investigation 115 (10): 2665–72. (October 2005). doi:10.1172/JCI26252. PMC 1236692. PMID 16200200.
- ^ a b c “Emerging roles of caspase-3 in apoptosis”. Cell Death and Differentiation 6 (2): 99–104. (February 1999). doi:10.1038/sj.cdd.4400476. PMID 10200555.
- ^ “Biochemical characteristics of caspases-3, -6, -7, and -8”. The Journal of Biological Chemistry 272 (41): 25719–23. (October 1997). doi:10.1074/jbc.272.41.25719. PMID 9325297.
- ^ “Apoptosis and cancer: mutations within caspase genes”. Journal of Medical Genetics 46 (8): 497–510. (August 2009). doi:10.1136/jmg.2009.066944. PMID 19505876.
- ^ “Mechanisms of caspase activation”. Current Opinion in Cell Biology 15 (6): 725–31. (December 2003). doi:10.1016/j.ceb.2003.10.009. PMID 14644197.
- ^ “A constitutively active and uninhibitable caspase-3 zymogen efficiently induces apoptosis”. The Biochemical Journal 424 (3): 335–45. (December 2009). doi:10.1042/BJ20090825. PMC 2805924. PMID 19788411.
- ^ “Apoptosis: live or die--hard work either way!”. Hormone and Metabolic Research 33 (9): 511–9. (September 2001). doi:10.1055/s-2001-17213. PMID 11561209.
- ^ a b “Novel procaspase-3 activating cascade mediated by lysoapoptases and its biological significances in apoptosis”. Advances in Enzyme Regulation 41 (1): 237–50. (2001). doi:10.1016/S0065-2571(00)00018-2. PMID 11384748.
- ^ a b c “Mitochondrial activation of apoptosis”. Cell 116 (2 Suppl): S57–9, 2 p following S59. (January 2004). doi:10.1016/S0092-8674(04)00031-5. PMID 15055583.
- ^ “Caspase 3 attenuates XIAP (X-linked inhibitor of apoptosis protein)-mediated inhibition of caspase 9”. The Biochemical Journal 405 (1): 11–9. (July 2007). doi:10.1042/BJ20070288. PMC 1925235. PMID 17437405.
- ^ “Protective effect of mangosteen extract against beta-amyloid-induced cytotoxicity, oxidative stress and altered proteome in SK-N-SH cells”. Journal of Proteome Research 9 (5): 2076–86. (May 2010). doi:10.1021/pr100049v. PMID 20232907.
- ^ “Serum caspase-3 p17 fragment is elevated in patients with ST-segment elevation myocardial infarction: a novel observation”. Journal of the American College of Cardiology 57 (2): 220–1. (January 2011). doi:10.1016/j.jacc.2010.08.628. PMID 21211695.
- ^ “Rehabilitation of a contract killer: caspase-3 directs stem cell differentiation”. Cell Stem Cell 2 (6): 515–6. (June 2008). doi:10.1016/j.stem.2008.05.013. PMID 18522841.
- ^ “Caspase-2 induces apoptosis by releasing proapoptotic proteins from mitochondria”. The Journal of Biological Chemistry 277 (16): 13430–7. (April 2002). doi:10.1074/jbc.M108029200. PMID 11832478.
- ^ “Molecular ordering of the Fas-apoptotic pathway: the Fas/APO-1 protease Mch5 is a CrmA-inhibitable protease that activates multiple Ced-3/ICE-like cysteine proteases”. Proceedings of the National Academy of Sciences of the United States of America 93 (25): 14486–91. (December 1996). doi:10.1073/pnas.93.25.14486. PMC 26159. PMID 8962078.
- ^ Selvakumar, P.; Sharma, RK. (May 2007). “Role of calpain and caspase system in the regulation of N-myristoyltransferase in human colon cancer (Review).”. Int J Mol Med 19 (5): 823–7. doi:10.3892/ijmm.19.5.823. PMID 17390089.
- ^ “Casper is a FADD- and caspase-related inducer of apoptosis”. Immunity 6 (6): 751–63. (June 1997). doi:10.1016/S1074-7613(00)80450-1. PMID 9208847.
- ^ “MRIT, a novel death-effector domain-containing protein, interacts with caspases and BclXL and initiates cell death”. Proceedings of the National Academy of Sciences of the United States of America 94 (21): 11333–8. (October 1997). doi:10.1073/pnas.94.21.11333. PMC 23459. PMID 9326610.
- ^ “The dependence receptor DCC (deleted in colorectal cancer) defines an alternative mechanism for caspase activation”. Proceedings of the National Academy of Sciences of the United States of America 98 (6): 3416–21. (March 2001). doi:10.1073/pnas.051378298. PMC 30668. PMID 11248093.
- ^ “Presence of a pre-apoptotic complex of pro-caspase-3, Hsp60 and Hsp10 in the mitochondrial fraction of jurkat cells”. The EMBO Journal 18 (8): 2040–8. (April 1999). doi:10.1093/emboj/18.8.2040. PMC 1171288. PMID 10205158.
- ^ “Hsp60 accelerates the maturation of pro-caspase-3 by upstream activator proteases during apoptosis”. The EMBO Journal 18 (8): 2049–56. (April 1999). doi:10.1093/emboj/18.8.2049. PMC 1171289. PMID 10205159.
- ^ “Protein kinase CK2 inhibitor 4,5,6,7-tetrabromobenzotriazole (TBB) induces apoptosis and caspase-dependent degradation of haematopoietic lineage cell-specific protein 1 (HS1) in Jurkat cells”. The Biochemical Journal 364 (Pt 1): 41–7. (May 2002). doi:10.1042/bj3640041. PMC 1222543. PMID 11988074.
- ^ “Caspase-mediated cleavage of actin-binding and SH3-domain-containing proteins cortactin, HS1, and HIP-55 during apoptosis”. Biochemical and Biophysical Research Communications 288 (4): 981–9. (November 2001). doi:10.1006/bbrc.2001.5862. PMID 11689006.
- ^ “IAP-family protein survivin inhibits caspase activity and apoptosis induced by Fas (CD95), Bax, caspases, and anticancer drugs”. Cancer Research 58 (23): 5315–20. (December 1998). PMID 9850056.
- ^ “An anti-apoptotic protein human survivin is a direct inhibitor of caspase-3 and -7”. Biochemistry 40 (4): 1117–23. (January 2001). doi:10.1021/bi001603q. PMID 11170436.
- ^ “Caspase-mediated cleavage of TRAF3 in FasL-stimulated Jurkat-T cells”. Journal of Leukocyte Biology 69 (3): 490–6. (March 2001). PMID 11261798.
- ^ “TRAF1 is a substrate of caspases activated during tumor necrosis factor receptor-alpha-induced apoptosis”. The Journal of Biological Chemistry 276 (11): 8087–93. (March 2001). doi:10.1074/jbc.M009450200. PMID 11098060.
- ^ “Ubiquitin-protein ligase activity of X-linked inhibitor of apoptosis protein promotes proteasomal degradation of caspase-3 and enhances its anti-apoptotic effect in Fas-induced cell death”. Proceedings of the National Academy of Sciences of the United States of America 98 (15): 8662–7. (July 2001). doi:10.1073/pnas.161506698. PMC 37492. PMID 11447297.
- ^ “The anti-apoptotic activity of XIAP is retained upon mutation of both the caspase 3- and caspase 9-interacting sites”. The Journal of Cell Biology 157 (1): 115–24. (April 2002). doi:10.1083/jcb.200108085. PMC 2173256. PMID 11927604.
- ^ “Structural basis for the inhibition of caspase-3 by XIAP”. Cell 104 (5): 791–800. (March 2001). doi:10.1016/S0092-8674(01)00274-4. PMID 11257232.
- ^ “The c-IAP-1 and c-IAP-2 proteins are direct inhibitors of specific caspases”. The EMBO Journal 16 (23): 6914–25. (December 1997). doi:10.1093/emboj/16.23.6914. PMC 1170295. PMID 9384571.
- ^ “X-linked IAP is a direct inhibitor of cell-death proteases”. Nature 388 (6639): 300–4. (July 1997). doi:10.1038/40901. PMID 9230442.
- ^ “X-linked inhibitor of apoptosis protein (XIAP) inhibits caspase-3 and -7 in distinct modes”. The Journal of Biological Chemistry 276 (29): 27058–63. (July 2001). doi:10.1074/jbc.M102415200. PMID 11359776.
- ^ “Identification of NRF2, a member of the NF-E2 family of transcription factors, as a substrate for caspase-3(-like) proteases”. Cell Death and Differentiation 6 (9): 865–72. (September 1999). doi:10.1038/sj.cdd.4400566. PMID 10510468.
関連文献[編集]
- “Caspases: the executioners of apoptosis”. The Biochemical Journal 326 (Pt 1): 1–16. (August 1997). doi:10.1042/bj3260001. PMC 1218630. PMID 9337844.
- Cytostatic p21 G protein-activated protein kinase gamma-PAK. Vitamins & Hormones. 62. (2001). pp. 167–98. doi:10.1016/S0083-6729(01)62004-1. ISBN 9780127098623. PMID 11345898
- “Structure and function of HIV-1 auxiliary regulatory protein Vpr: novel clues to drug design”. Current Drug Targets. Immune, Endocrine and Metabolic Disorders 4 (4): 265–75. (December 2004). doi:10.2174/1568008043339668. PMID 15578977.
- “The Vpr protein from HIV-1: distinct roles along the viral life cycle”. Retrovirology 2 (1): 11. (2006). doi:10.1186/1742-4690-2-11. PMC 554975. PMID 15725353.
- “Reversible glutathiolation of caspase-3 by glutaredoxin as a novel redox signaling mechanism in tumor necrosis factor-alpha-induced cell death”. Circulation Research 100 (2): 152–4. (February 2007). doi:10.1161/01.RES.0000258171.08020.72. PMID 17272816.
関連項目[編集]
外部リンク[編集]
- ペプチダーゼとその阻害因子に関するMEROPSオンラインデータベース: C14.003
- Apoptosis & Caspase 3 – The Proteolysis Mapのアニメーション