中毒性表皮壊死症
 ウィキペディアから無料の百科事典
ウィキペディアから無料の百科事典
| 中毒性表皮壊死症 | |
|---|---|
 | |
| Toxic epidermal necrolysis | |
| 概要 | |
| 診療科 | 皮膚科学 |
| 分類および外部参照情報 | |
| ICD-10 | L51.2 |
| ICD-9-CM | 695.15 |
| OMIM | 608579 |
| DiseasesDB | 4450 |
| eMedicine | emerg/599 med/2291 derm/405 |
| Patient UK | 中毒性表皮壊死症 |
| MeSH | D004816 |
中毒性表皮壊死症(ちゅうどくせいひょうひえししょう、Toxic epidermal necrolysis、TEN)はライエル症候群(Lyell's syndrome)[1]としても知られる重篤な皮膚障害で、通常医薬品の副作用として発生する[2]。全身の皮膚表皮が真皮と分離して重篤な感染症を招く。死亡率は20〜40%で、死因の多くは敗血症[3]と続発性の多臓器不全である。治療はまず原因と思われる薬剤の投与を全て中止する事と、集中治療室などでの支持療法(対症療法)である[4][5]。
TENの発生率は毎年100万人当り0.4〜1.9人である[6]。TENはスティーブンス・ジョンソン症候群(SJS)と連続した概念である。体表面の3割以上に病変があるとTENとされ、1割以下の場合はSJSとされる。その中間の、1〜3割に病変がある場合は“SJS/TEN”と呼ばれる[7][8]。多形紅斑(EM)とTEN/SJSを一元的に捉えようと議論された事が過去にあるが、現在では異なる概念とされている[6][9][10]。
兆候と症状
[編集]前駆症状
[編集]TENは最終的に広範囲の皮膚紅斑、壊死、皮膚・粘膜の表層剥離に至るが、それに先立って多くの場合インフルエンザ様症状(咳嗽、鼻水、発熱、食欲不振、不快感)を経験する。薬剤の使用歴は平均で症状発現前14日間(1〜4週間)であるが、再曝露(薬物の再使用)後48時間で再発する事もある[11]。
皮膚症状
[編集]初期の皮膚症状は体躯の赤紫色で黒ずんだ平坦な斑であり、そこから拡大して行き、大きな水疱を形成する。病変部の皮膚は壊死し始め、または弛み、大きく剥離する[4]。
粘膜症状
[編集]TENを発症するほぼ全ての人で、口腔、眼、外陰部にも症状が現れる。有痛性の痂皮とびらんが粘膜表面に形成される[12]。口腔内の水疱やびらんのため、食事が困難となり、経鼻胃管または経皮内視鏡的胃瘻造設術が必要となる。眼は腫脹し、痂皮を生じ、潰瘍が生成して失明に至る危険がある。眼に関する最も重篤な症状は結膜炎である[13]。
病因
[編集]TENの病因として最多のものは薬剤性であり、80〜95%とされる[6]。
TENを最も引き起こしやすい薬剤は:
そのほか、肺炎マイコプラズマ 感染症、デングウイルス感染症でTENが発生した例も報告されている。画像診断に用いる造影剤や骨髄や臓器の移植もTENの発生に関連があると指摘されている[2][6]。
薬剤以外の要因として、溶連菌の関与を指摘する報告がある[14]。
HIV
[編集]HIV-陽性の患者はその他の場合よりも1,000倍、SJS/TENのリスクが高いが、その理由は定かではない[4]。
遺伝学的因子
[編集]一部の遺伝子型がTENリスクと相関している。例を挙げると、一部のHLA抗原、HLA-B*1502[15]、HLA-A*3101[16]、HLA-B*5801[17]は特定の薬剤でのTEN発症リスクが高い。
発症機序
[編集]TENにおける免疫系の役割は明らかではないが、一部の免疫細胞(細胞傷害性CD8+ T細胞)は角化細胞の死と続発性の皮膚剥離の主因である。角化細胞は表皮深部に存在し、皮膚細胞を支えている。CD8+ T細胞が薬剤やその代謝物で過剰に活性化されて角化細胞を攻撃しているのではないかとの仮説が立てられる。すなわちCD8+ T細胞がパーフォリン、グランザイムB、グラヌリシン、腫瘍壊死因子α、Fasリガンドなどの分子を大量に放出し、角化細胞を死滅させ、TENを呈するというものである[6]。
診断
[編集]TENの診断は臨床的知見と組織学的知見の両方に基づく。早期のTENは非特異的薬剤反応と似ているので、臨床家は早い内にTENの可能性を念頭に置く必要がある。口腔、眼、性器の粘膜炎はほとんどの患者に現れるので、TENの診断に結び付く症状だと言える。ニコルスキー徴候(穏やかに横方向に力を加えると基底層から真皮乳頭層が分離する)およびアスボー・ハンセン徴候(水疱に圧を掛けると横方向に拡がる)もTENに見られる現象である[4]。
TENの死亡率が高いため、転帰を改善するためには迅速な治療が必要であり、早期TENを診断可能な血中バイオマーカーの発見が待たれている。血清グラヌリシンや血清HMGB1などが早期臨床試験で良好な結果を示している[4]。
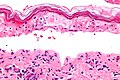
組織学的概要
[編集]TENの確定診断では、しばしば生検での確認が必要である。組織学的には、早期TENでは壊死した角質細胞を散在性に認める。より進行したTENでは、角質細胞全層の壊死が見られ、真皮乳頭層において表皮が乖離し、真皮への炎症性浸潤所見は乏しい。表皮の組織学的壊死の所見は感度は高いがTENに特異的ではない[4]。
- 表皮の壊死融解・弱拡大
- 表皮の壊死融解・強拡大
鑑別診断
[編集]- ブドウ球菌性熱傷様皮膚症候群
- 薬剤誘発性線状IgA水疱性皮膚症
- 移植片対宿主病
- 急性汎発性発疹性膿疱症
- 紅皮症
- DRESS症候群(薬剤過敏症症候群)
- 全身性麻疹様発疹[18]
治療
[編集]治療の第一歩は発生因子の除去であり、多くの場合被疑薬の投与中止である。その後速やかに熱傷センターまたは集中治療室に収容し、支持療法と栄養維持を開始する[4]。皮膚や粘膜以外の合併症として多臓器不全(肝臓、腎臓など)が起こる。従って全身状態を観察しながら治療が行われる。
主な治療法は[19]、
2016年6月時点では、補助的全身療法の使用を勧める文献はない。免疫グロブリン大量点滴静注療法(IVIG)は、in vitro でFas-FasLを介する角化細胞のアポトーシスをブロックする[22]。だが、TENの治療でIVIGを実施すべきか否かについては意見が分かれている[23]。より一般化された結論を導くには、疾患の重症度、IVIGの投与量、IVIGの投与時期を管理された臨床試験を複数実施しなければならない[4]。TENにおけるIVIGの意義を明らかにするために、より大きく質の高い臨床試験が必要とされている。
その他の数多の補助的全身療法、ステロイド系抗炎症薬、シクロスポリン、シクロホスファミド、血漿分離交換法、ペントキシフィリン、アセチルシステイン、ウリナスタチン、インフリキシマブ、顆粒球コロニー刺激因子(白血球減少関連時)が試されて来た。ステロイド使用の是非については結果は統一的でなく、他の治療法のエビデンスは不足している[4]。
予後
[編集]TENの死亡率は概算で22〜40%である[19]。皮膚を失った患者は真菌や細菌に易感染性の状態であり、敗血症を来して死に至り得る[2]。死因は感染または呼吸困難(肺炎または気管内皮障害による)である。顕微鏡を用いた組織検査(特に単核細胞の浸潤の程度と一般的な炎症の程度)は個々の患者の予後診断に有用である[24]。
重症度スコア
[編集]TEN重症度スコア(Severity of Illness Score for Toxic Epidermal Necrolysis、SCORTENスコア)がTENの重症度診断と死亡率予測に用いられる[25]。
下記の条件に一致したらそれぞれ1点とする[26]:
スコア毎の死亡率
[編集]- 0-1点 ― 3.2%
- 2点 ― 12.2%
- 3点 ― 35.3%
- 4点 ― 58.3%
- ≥5点 ― 90%
注意すべき点は、このスコアは第1日目と第3日目で最も有効である事と、呼吸器系のリスクを考慮していない事である[26]。
長期合併症
[編集]TENの急性期を乗り切った後も、皮膚および眼に症状が残ることが多い。皮膚合併症は、瘢痕、発疹性色素細胞性母斑、外陰膣狭窄、性交痛である。眼の合併症は、TEN患者の20〜79%に残り、急性期に眼の症状が無かった場合にも現れ得る。その代表的な症状はドライアイ、羞明、瞼球癒着、角膜瘢痕または乾皮症、結膜下線維症、睫毛乱生症、視力の低下、失明である[26]。
出典
[編集]- ^ Rapini, Ronald P.; Bolognia, Jean L.; Jorizzo, Joseph L. (2007). Dermatology: 2-Volume Set. St. Louis: Mosby. ISBN 1-4160-2999-0
- ^ a b c d Garra, GP (2007). "Toxic Epidermal Necrolysis". Emedicine.com. Retrieved on December 13, 2007.
- ^ 小川寛恭、横田治、関啓輔、小倉真治、前川信博「敗血症の原因としてBacterial Translocationが示唆された中毒性表皮壊死症の1症例」第11巻第4号、2004年、doi:10.3918/jsicm.11.439。
- ^ a b c d e f g h i Schwartz, RA; McDonough, PH; Lee, BW (August 2013). “Toxic epidermal necrolysis: Part II. Prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment.”. Journal of the American Academy of Dermatology 69 (2): 187.e1-16; quiz 203–4. doi:10.1016/j.jaad.2013.05.002. PMID 23866879.
- ^ http://www.genome.gov/27560487
- ^ a b c d e Schwartz, RA; McDonough, PH; Lee, BW (August 2013). “Toxic epidermal necrolysis: Part I. Introduction, history, classification, clinical features, systemic manifestations, etiology, and immunopathogenesis.”. Journal of the American Academy of Dermatology 69 (2): 173.e1-13; quiz 185–6. doi:10.1016/j.jaad.2013.05.003. PMID 23866878.
- ^ “Stevens-Johnson syndrome and toxic epidermal necrolysis: Pathogenesis, clinical manifestations, and diagnosis”. UpToDate. Wolters Kluwer. 21 November 2014閲覧。
- ^ Bastuji-Garin, S; Rzany, B; Stern, RS; Shear, NH; Naldi, L; Roujeau, JC (January 1993). “Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome, and erythema multiforme.”. Archives of dermatology 129 (1): 92–6. doi:10.1001/archderm.129.1.92. PMID 8420497.
- ^ “Erythema multiforme. A heterogeneous pathologic phenotype”. Minerva Stomatol 48 (5): 217–26. (1999). PMID 10434539.
- ^ “Mucosal disease series. Number IV. Erythema multiforme”. Oral Dis 11 (5): 261–7. (2005). doi:10.1111/j.1601-0825.2005.01141.x. PMID 16120111.
- ^ Jordan, MH; Lewis, MS; Jeng, JG; Rees, JM (1991). “Treatment of toxic epidermal necrolysis by burn units: another market or another threat?”. The Journal of burn care & rehabilitation 12 (6): 579–81. doi:10.1097/00004630-199111000-00015. PMID 1779014.
- ^ Roujeau, JC; Stern, RS (10 November 1994). “Severe adverse cutaneous reactions to drugs.”. The New England Journal of Medicine 331 (19): 1272–85. doi:10.1056/nejm199411103311906. PMID 7794310.
- ^ Morales, ME; Purdue, GF; Verity, SM; Arnoldo, BD; Blomquist, PH (October 2010). “Ophthalmic Manifestations of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis and Relation to SCORTEN.”. American journal of ophthalmology 150 (4): 505–510.e1. doi:10.1016/j.ajo.2010.04.026. PMID 20619392.
- ^ 大網毅彦、中西加寿也、大島拓、奥怜子「溶連菌感染の関与が示唆された中毒性表皮壊死症の1例」第19巻第3号、2012年、doi:10.3918/jsicm.19.409。
- ^ Hung, SI; Chung, WH; Jee, SH; Chen, WC; Chang, YT; Lee, WR; Hu, SL; Wu, MT et al. (April 2006). “Genetic susceptibility to carbamazepine-induced cutaneous adverse drug reactions.”. Pharmacogenetics and genomics 16 (4): 297–306. doi:10.1097/01.fpc.0000199500.46842.4a. PMID 16538176.
- ^ McCormack, M; Alfirevic, A; Bourgeois, S; Farrell, JJ; Kasperavičiūtė, D; Carrington, M; Sills, GJ; Marson, T et al. (24 March 2011). “HLA-A*3101 and carbamazepine-induced hypersensitivity reactions in Europeans.”. The New England Journal of Medicine 364 (12): 1134–43. doi:10.1056/nejmoa1013297. PMID 21428769.
- ^ Tohkin, M; Kaniwa, N; Saito, Y; Sugiyama, E; Kurose, K; Nishikawa, J; Hasegawa, R; Aihara, M et al. (February 2013). “A whole-genome association study of major determinants for allopurinol-related Stevens-Johnson syndrome and toxic epidermal necrolysis in Japanese patients.”. The pharmacogenomics journal 13 (1): 60–9. doi:10.1038/tpj.2011.41. PMID 21912425.
- ^ Schwartz, RA; McDonough, PH; Lee, BW (Aug 2013). “Toxic epidermal necrolysis: Part II. Prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment.”. Journal of the American Academy of Dermatology 69 (2): 187.e1-16; quiz 203–4. doi:10.1016/j.jaad.2013.05.002. PMID 23866879.
- ^ a b 中毒性表皮壊死症 難病情報センター
- ^ 浅古佳子、和田秀文、高倉桃子、杉田泰之、相原道子、岡澤ひろみ、川口とし子、池澤善郎「ステロイドパルス療法で救命しえた中毒性表皮壊死症型薬疹の1例」第8号、2002年7月1日、doi:10.11477/mf.1412904028。 (
 要購読契約)
要購読契約) - ^ 奥山泰裕、山田裕道、池田志斈「中毒性表皮壊死症(TEN)に対する血漿交換療法(<特集>皮膚疾患とアフェレシス)」『日本アフェレシス学会雑誌』第27巻第2号、日本アフェレシス学会、2008年5月31日、139-144頁、NAID 110006664588。
- ^ Zajicek, R; Pintar, D; Broz, L; Suca, H; Königova, R (May 2012). “Toxic epidermal necrolysis and Stevens-Johnson syndrome at the Prague Burn Centre 1998-2008.”. Journal of the European Academy of Dermatology and Venereology : JEADV 26 (5): 639–43. doi:10.1111/j.1468-3083.2011.04143.x. PMID 21668825.
- ^ “Toxic epidermal necrolysis: retrospective analysis of 21 consecutive cases managed at a tertiary centre”. Clin. Exp. Dermatol. 35 (8): 853–62. (December 2010). doi:10.1111/j.1365-2230.2010.03826.x. PMID 20456393.
- ^ Quinn AM; Brown, K; Bonish, BK; Curry, J; Gordon, KB; Sinacore, J; Gamelli, R; Nickoloff, BJ (2005). “Uncovering histological criteria with prognostic significance in toxic epidermal necrolysis”. Arch Dermatol 141 (6): 683–7. doi:10.1001/archderm.141.6.683. PMID 15967913.
- ^ Schwartz, RA; McDonough, PH; Lee, BW (August 2013). “Toxic epidermal necrolysis: Part II. Prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment.”. Journal of the American Academy of Dermatology 69 (2): 187.e1-16; quiz 203–4. doi:10.1016/j.jaad.2013.05.002. PMID 23866879.
- ^ a b c DeMers, G; Meurer, WJ; Shih, R; Rosenbaum, S; Vilke, GM (December 2012). “Tissue plasminogen activator and stroke: review of the literature for the clinician.”. The Journal of emergency medicine 43 (6): 1149–54. doi:10.1016/j.jemermed.2012.05.005. PMID 22818644.