窒化亜鉛
 ウィキペディアから無料の百科事典
ウィキペディアから無料の百科事典
| 窒化亜鉛 Zinc nitride | |
|---|---|
 | |
| 識別情報 | |
| CAS登録番号 | 1313-49-1 |
| 特性 | |
| 化学式 | Zn3N2 |
| モル質量 | 244.15 g/mol[1] |
| 外観 | 灰色の粉末[1] |
| 密度 | 6.22 g/cm3, 固体[1] |
| 水への溶解度 | 不溶(分解) |
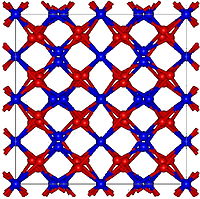
| 構造 | |
| 結晶構造 | 立方晶, cI80 |
| 空間群 | Ia-3, No. 206[1][2] |
| 危険性 | |
| EU分類 | not listed |
| NFPA 704 | |
| 関連する物質 | |
| その他の陰イオン | 硝酸亜鉛 硫化亜鉛 |
| その他の陽イオン | 窒化リチウム 窒化鉄 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
窒化亜鉛(ちっかあえん、英: Zinc nitride)は、亜鉛の窒化物。化学式はZn3N2。純粋なものは立方晶型の結晶構造をとる[1][2]。1940年に、Juzaらにより初めて合成された。
性質
[編集]窒化亜鉛は、亜鉛アミド(亜鉛ジアミン)を嫌気的環境下で200℃に加熱し、熱分解することで得られる[3] その際、副生物としてアンモニアが生じる[4]。
亜鉛とアンモニアを315℃に加熱することによっても得られる。その場合には、副生物として水素が生じる[3][5]。
窒化亜鉛は水と激しく反応し、酸化亜鉛とアンモニアを生じる[3][4]。
塩酸に可溶で[6]、リチウムとは電気化学的・可逆的に反応する[7]。窒化リチウムや窒化マグネシウム同様、融点は高い。[8]
用途
[編集]窒化亜鉛の薄膜は可視及び近赤外領域で光透過性があり、光機能素子材料としての利用が研究されている。
脚注
[編集]- ^ a b c d e Sangeeta, D. (1997). Inorganic Materials Chemistry Desk Reference. CRC Press. p. 278. ISBN 978-0-8493-8900-9 2007年9月30日閲覧。
- ^ a b Partin, D.E., D.J. Williams, and M. O'Keeffe (1997). “The Crystal Structures of Mg3N2and Zn3N2”. Journal of Solid State Chemistry 132 (1): 56–59. doi:10.1006/jssc.1997.7407 2007年5月3日閲覧。.
- ^ a b c Roscoe, Henry Enfield, and Carl Schorlemmer (1907) [1878]. A Treatise on Chemistry: Volume II, The Metals (4th ed.). London: Macmillan. pp. 650–51 2007年11月1日閲覧。
- ^ a b Bloxam, Charles Loudon (1903). Chemistry, inorganic and organic (9th ed.). Philadelphia: P. Blakiston's Son & Co.. p. 380 2007年10月31日閲覧。
- ^ Lowry, Martin Thomas (1922). Inorganic Chemistry. Macmillan. p. 872 2007年11月1日閲覧。
- ^ Comey, Arthur Messinger, Dorothy A. Hahn (February 1921). A Dictionary of Chemical Solubilities: Inorganic (2nd ed.). New York: Macmillan. p. 1124 2007年11月1日閲覧。
- ^ Amatucci, G.G., and N. Pereira (2004). “Nitride and Silicide Negative Electrodes”. In Gholam-Abbas Nazri and Gianfranco Pistoia. Lithium Batteries: Science and Technology. Kluwer Academic Publishers. p. 256. ISBN 978-1-4020-7628-2 2007年11月1日閲覧。
- ^ Grolier Incorporated (1994). Academic American Encyclopedia. Danbury, Connecticut: Grolier Inc.. p. 202. ISBN 0717220532 2007年11月1日閲覧。
参考文献
[編集]- Futsuhara M., Yoshioka K., and Takai O. (1998-06-08). “Structural, electrical and optical properties of zinc nitride thin films prepared by reactive rf magnetron sputtering”. Thin Solid Films (Elsevier) 322 (1): 274–81. doi:10.1016/S0040-6090(97)00910-3.
- Lyutaya, M.D., and S.A. Bakuta (February 1980). “Synthesis of the nitrides of Group II elements”. Powder Metallurgy and Metal Ceramics (Springer) 19 (2): 118–22. doi:10.1007/BF00792038.



